
| A、標準狀況下,22.4LH2O含有的原子總數為3NA |
| B、常溫常壓下,含有NA個氖原子的氖氣體積約為22.4L |
| C、4g金屬鈣變成鈣離子時失去的電子數目為0.1NA |
| D、2L0.5mol?L-1的氯化鎂溶液中所含的離子總數為3NA |
| m |
| M |
| m |
| M |
| 4g |
| 40g/mol |


 七彩題卡口算應用一點通系列答案
七彩題卡口算應用一點通系列答案科目:高中化學 來源: 題型:
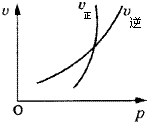
| A、N2O3(g)?NO2(g)+NO(g); 恒容時加入N2O3,平衡正向移動 |
| B、N2(g)+3H2(g)?2NH3(g); 將氨氣液化分離后,有利于加快正反應速率 |
| C、4NH3(g)+5O2(g)?4NO(g)+6H2O(g); 加大氧氣濃度,能提高氨氣平衡轉化率 |
| D、2SO2(g)+O2(g)?2SO3(g); 增大壓強,平衡常數不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、標況下,11.2 L氯氣完全溶于1 L水中,所得溶液中Cl-和ClO-兩種粒子數之和為NA |
| B、80mL 10mol?L-1 鹽酸與足量MnO2加熱反應,產生Cl2分子數為0.2NA |
| C、含有4 NA個碳碳σ鍵的金剛石,其質量為24 g |
| D、含0.1 mol FeCl3的溶液完全水解后得到的膠體粒子個數為0.1 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、任何化學反應都伴隨有能量變化 |
| B、△H>0表示放熱反應,△H<0表示吸熱反應 |
| C、化學鍵的斷裂會放出能量 |
| D、反應物總能量比生成物總能量高的反應是吸熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、加催化劑,V正、V逆都發生變化,且變化的倍數相等,平衡不移動 |
| B、加壓,V正、V逆都增大,且V正增大的倍數大于V逆增大的倍數,平衡正移 |
| C、降溫,V正、V逆都減小,且V逆減小的倍數小于V正減小的倍數,平衡逆移 |
| D、減少氨氣的濃度,V正不變,V逆減小,且平衡向正反應方向移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 選項 | 異常情況 | 可能的原因 |
| ① | 蒸發結晶時,蒸發皿破裂 | 將溶液蒸干或酒精燈燈芯碰到蒸發皿底部 |
| ② | 分液時,分液漏斗中的液體很難滴下 | 沒有打開分液漏斗頸上的玻璃塞或塞上的凹槽與漏斗上的小孔沒有對齊 |
| ③ | 萃取時,振蕩溶液,靜置不分層 | 萃取劑加得太多 |
| ④ | 蒸餾時,發現冷凝管破裂 | 沒有通冷凝水或先加熱后通冷凝水 |
| A、① | B、② | C、③ | D、④ |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 實驗 編號 | T/K | 催化劑的用量/g | 酸性KMnO4溶液的濃度/mol?L-1 | 實驗目的 |
| ① | 298 | 0.5 | 0.010 | a.實驗①和②探究酸性KMnO4溶液的濃度對該反應速率的影響; b.實驗①和 c.實驗①和 |
| ② | ||||
| ③ | ||||
| ④ |
| 實驗編號 | 溶液褪色所需時間 t/min | ||
| 第1次 | 第2次 | 第3次 | |
| ① | 14.0 | 13.0 | 11.0 |
| ② | 6.0 | 7.0 | 7.0 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com