
���}Ŀ���������P�x�ӷ���ʽ���_����( )
A.̼����c��ˮ�⣺HCO3��+H2O![]() H3O++CO32��
H3O++CO32��
B.�����\��Һ�м�Ba(OH)2��Һ�{��(ji��)pH=12��Al3++SO42-+4OH-+Ba2+�TBaSO4�� +AlO2-+2H2O
C.��偠tˮ���е������}�ü��A��Һ̎����CaSO4��CO32�D=CaCO3��SO42�D,
D.Al(OH)3����ʽ��x��Al(OH)3=H����AlO2��+H2O
���𰸡�C
��������
A. ԓ������ʾ����HCO3������x�^�̣�̼����c��ˮ�ⷴ����![]() ��A�e�`��
��A�e�`��
B. �����\��Һ�м�Ba(OH)2��Һ�{��(ji��)pH=12�ķ���ʽ��Al3++2SO42-+4OH-+2Ba2+�T2BaSO4�� +AlO2-+2H2O��B�e�`��
C. CaCO3���ܽ���С��CaSO4����ͨ�^�������D�����F(xi��n)偠tˮ����̎��������ʽ���_��C���_��
D. Al(OH)3����ʽ��x�鲻��ȫ��x����x����ʽ��Al(OH)3 ![]() H����AlO2��+H2O��D�e�`��
H����AlO2��+H2O��D�e�`��
�ʴ��xC��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� С�W��10��犑����}ϵ�д�
С�W��10��犑����}ϵ�д�
| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��һ���l���£����ݷe���2.0L�������У�Fe��CO2�l(f��)�����·����� CO2��g�� + Fe��s�� ![]() FeO��s�� + CO��g��������ʼ�r�������м���1mol CO2��5.0 min�������Ț��w������ƽ����������32���t�@�Εr�g������CO2��=_____________��
FeO��s�� + CO��g��������ʼ�r�������м���1mol CO2��5.0 min�������Ț��w������ƽ����������32���t�@�Εr�g������CO2��=_____________��
�������f�������_����_______
a ����Ϛ��w���ܶȲ�׃�r�f�������_����ƽ��
b ��Ϛ��w��ƽ�����������|����׃�r�f�������_����ƽ��
c ƽ����Ƴ�������̼�r������������һֱ�pСֱ�������µ�ƽ��
d ƽ���sС�������w�e�����淴�����ʲ�׃��ƽ�ⲻ�Ƅ�
�ڴ������_��ƽ����ٳ���һ�����Ķ�����̼��ƽ����_________�Ƅӣ��x������������ ����������������������������̼���D����________�����������������pС��������׃������CO�����|����____���x���������������pС��������׃������
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ����k��Ni-Cd���ɳ��늳��ڬF(xi��n)���������ЏV�����á�늽��|��Һ��KOH��Һ��늳ط����飺Cd +2NiO(OH)+2H2O![]() Cd(OH)2+2Ni(OH)2���������P��k늳ص��f�����_����
Cd(OH)2+2Ni(OH)2���������P��k늳ص��f�����_����
A. ����^���ǻ��W���D������ܵ��^��
B. ��늕rꖘO������Cd(OH)2��2e��="=" Cd + 2OH-
C. ��늕r늳Ȳ�OH - �����O�Ƅ�
D. ��늕r�cֱ���Դ���O���B��늘O�ϰl(f��)��Ni(OH)2�D����NiO(OH)�ķ���
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ����2molSO2��1molO2��������w�e��׃�������㶨�����]�����У���һ���ض��°l(f��)�����·�����2SO2(g)+O2(g)![]() 2SO3(g) ��H��0���������M�е��r�gt1�c�r�_��ƽ���B(t��i)���y�û�Ϛ��w�����|������2.1mol��ԇ�ش����І��}��
2SO3(g) ��H��0���������M�е��r�gt1�c�r�_��ƽ���B(t��i)���y�û�Ϛ��w�����|������2.1mol��ԇ�ش����І��}��
��1����ƽ��r�������w�e��aL������ԓ������ƽ�ⳣ��(sh��)�飺K=__________���ú�a�Ĵ���(sh��)ʽ��ʾ��
��2�������M�е�t1�r��SO2���w�e�֔�(sh��)��_______________��
��3������t1�r����һ�����Ě�⣨Ar����SO2�����|������________����������pС����׃������
��4������t1�r���أ������_��ƽ���B(t��i)����ƽ�������К��w�Ŀ����|����____2.1mol�����������������=�����������f��ԭ��____________��
��5����t1�_��ƽ������������w�e����׃�����ټ���0.2molSO2��0.1molO2��1.8molSO3���˕rv��________v�� �����������������=������
��6��һ���ض��£��������ݷe��ͬ�ĺ������]�����а���ͬ��ʽͶ�뷴����l(f��)������2SO2(g)+O2(g)![]() 2SO3(g)���������şᣩ���y�÷��������P��(sh��)��(j��)���£�
2SO3(g)���������şᣩ���y�÷��������P��(sh��)��(j��)���£�
����1 | ����2 | ����3 | |
�����ض�T/K | 700 | 700 | 800 |
������Ͷ���� | 2 mol SO2��1 mol O2 | 4 mol SO3 | 2 mol SO2��1 mol O2 |
ƽ��v��(SO2)/ mol��L��1��s��1 | v1 | v2 | v3 |
ƽ��c(SO3)/mol��L��1 | c1 | c2 | c3 |
ƽ���wϵ������p/Pa | p1 | p2 | p3 |
���|��ƽ���D������ | ��1(SO2) | ��2(SO3) | ��3(SO2) |
ƽ�ⳣ��(sh��)K | K1 | K2 | K3 |
�á���������������=���������ЙM���ϣ�
c2______2c1��v1______v2��K1_____K3��p2____2p3����1(SO2)_____��3(SO2)����2(SO3)����3(SO2)_______1
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��25���r���ϳɰ��ķ����ữ�W����ʽ�飺N2(g)��3H2(g) ![]() 2NH3(g) ��H=��92.4 kJ/mol���������P�f�����_����( )
2NH3(g) ��H=��92.4 kJ/mol���������P�f�����_����( )
A.��1 mol N2��3 mol H2����һ���w�e�����]�����г�ַ����ɷų�92.4 kJ�ğ���
B.�x��ߜظ߉��l��������ߺϳɰ��Įa���Ƿ�����������ԭ��ָ�����H���a��
C.���ںϳɰ��_ƽ��r�pС������ʹ�����淴�����ʜpС����ƽ�������Ƅ�
D.��һ���w�e�������кϳɰ��r���������ȵĚ��w�ܶȲ���׃���f�������_�����Wƽ���B(t��i)
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��ijͬ�W����Y�ϵ�֪25���r�����������x����(sh��)���±�:
�� | HCOOH | HClO | H2CO3 | H2C2O4 | H2S |
��x����(sh��)(Ka) | 1.8��10-4 | 3��10-8 | K1=4.4��10-7 K2=4.7��10-11 | K1=5.4��10-2 K2=5.4��10-5 | K1=1.3��10-7 K2=7.1��10-15 |
��(j��)�˻ش����ׂ����}:
(1)��λͬ�W����(j��)���Д�(sh��)��(j��)�������ׂ���������ʽ
�ף�![]()
�ң�![]()
����![]()
����![]()
�����������Գɹ��M�е���______(��ͬ�W��̖)��
(2)��ͬ�W���C�� HCOOH �����ᣬ�������·���һ�����C������_______(����̖)��
�������y��HCOONa��Һ��pH����7
����HCOOH ��Һ����늌����ݺܰ�
��HCOOH�cNa2S�ܰl(f��)�������a�����u����ζ�Ě��w
������pHӋ�y�ó����� 0.1 mol/L HCOOH ��Һ��pH=1.37
��HCOONa��H3PO4���������� HCOOH
��pH=2��HCOOH��Һϡ���100���y��pH�s��3.4
(3)��ͬ�Wȡ10.00 mL 0.1 mol/L H2C2O4���Ҝ�����0.1 mol/L NaOH ��Һ�M�еζ�����ʹ�Ú��x�ӝ�ȱO(ji��n)�y�x�M�Ќ��r�O(ji��n)�أ�����X�@ʾ pH=7����(w��n)���rֹͣ�ζ����˕r�y������NaOH ��Һ�w�e��V mL��
��ԓ����ʹ��________��ȡ10.00 mL 0.1 mol/L H2C2O4(��x�����Q)��
��V____10.00 mL(����>����="����<��)��
���ζ��Y������Һ�������x�ӝ���ɴ�С�飺_________(�����x�ӝ�ȷ�̖������>���B��)��
����ͬ�W�c��ͬ�W��ͬ�ӌ�������0.1 mol/L H2C2O4�Q��0.1 mol/L H2S��Һ����ͬ�W���Y������Һc(HS-)___ c(S2-)(��">""<"����=��)��
(4)��֪���Ը��i��⛿Ɍ����������ɶ�����̼�������� HCOOH ��Һ��ijKMnO4��Ʒ�M�м��Ȝy��(�s�|����������)��ȡ0.200 g KMnO4��Ʒ(M=158 g/mol)���F��ƿ���ܽⲢ�ữ����0.100 mol/L�Ę˜�HCOOH��Һ�M�еζ����ζ����K�c�r���� HCOOH ��Һ20.00 mL��
���� KMnO
���_���_���ζ��K�c���Д����_________��
��ԓ��Ʒ��KMnO4�ļ��Ȟ� _______(�ðٷ֔�(sh��)��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ������ϩ��һ�N��Ҫ�Ļ���ԭ�ϣ������l(w��i)���M�����H���Y�о��C���������°�����γ������텢��������ϩ��2B��°�������С�
(1)���I(y��)�Ͽ����ұ���Ó�䷽���Ƃ䱽��ϩ���䷴��ԭ�����£�
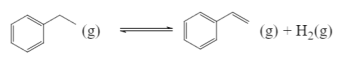
�����ݷe�̶���2L�����]�����ȳ���2mol![]() ��������m����(�w�e���Ժ��Բ�Ӌ)����һ���ضȉ������_ʼ�������É���Ӌ�O(ji��n)�y�����ȉ�����׃�����£�
��������m����(�w�e���Ժ��Բ�Ӌ)����һ���ضȉ������_ʼ�������É���Ӌ�O(ji��n)�y�����ȉ�����׃�����£�
�����r�g/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
����/MPa | 12.6 | 13.68 | 14.55 | 15.22 | 15.6 | 15.75 | 15.75 |
����(j��)���Д�(sh��)��(j��)Ӌ��ԓ�ض�����ƽ�ⳣ��(sh��)Kp_____(Ӌ��Y������λ����ƽ��։�����ƽ����Ӌ�㣬�։�=���������|�����֔�(sh��))��
�����H���a�г��ں㉺�l����?li��n)���ߜ�ˮ�������鷴���wϵ��ϡጄ�(ˮ���ⲻ���ӷ���)����һ��������900K�ėl���£�����ϩ�Įa���S��![]() �������_________(�������������pС��������׃��)���S���������M�У����a���e̼ʹ�������Ԝp����ˮ����߀�����ڻ֏ʹ������ԣ�ԭ����__________(�û��W����ʽ��ʾ)��
�������_________(�������������pС��������׃��)���S���������M�У����a���e̼ʹ�������Ԝp����ˮ����߀�����ڻ֏ʹ������ԣ�ԭ����__________(�û��W����ʽ��ʾ)��
(2)�о��������ٴ�߲���������܉�������x���Դ���������ϩ���ɱ���ȩ(�Y����ʽ��![]() )����ԓ����ԭ���OӋ������ȼ��늳أ��t늳�ؓ�O��늘O����ʽ��____________����ԓ늳����Ę˜ʠ�r��11.2 L��O2���t���·����Փ���D����ӵ����|������________��
)����ԓ����ԭ���OӋ������ȼ��늳أ��t늳�ؓ�O��늘O����ʽ��____________����ԓ늳����Ę˜ʠ�r��11.2 L��O2���t���·����Փ���D����ӵ����|������________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��ijͬ�W�M��SO2�����|�����c�ΰ�a��b��c��d̎�քe���в�ͬ��ԇ��������Na2SO3���w�ϵμӔ�(sh��)�Ν�H2SO4���������c�ΰ����w�����B(y��ng)��һ�Εr�g���^�쵽�Č��F(xi��n)�������ʾ�������f�����_���ǣ� ��
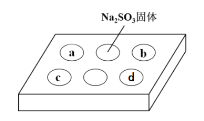
��̖ | ԇ�� | ���F(xi��n)�� |
a | Ʒ�t��Һ | �tɫ��ȥ |
b | ����KMnO4��Һ | ��ɫ��ȥ |
c | NaOH��Һ����2�η�̪�� | �tɫ��ȥ |
d | H2S��Һ | �Sɫ���� |
A.�ڝ������cNa2SO3���w�����У���������F(xi��n)�ď�������
B.a��b������SO2����Ư����
C.c��ֻ���ܰl(f��)��������SO2+2OH-=SO32-+H2O
D.d���SO2����������
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ������ͬ�ض���(T��500K)������ͬ�w�e�ļס��҃��������ұ����w�e��׃���������г���1gSO2��1gO2���������г���2gSO2��2gO2�����Д������e�`���ǣ� ��
A.���W�������ʣ���>��B.ƽ��rO2�ĝ�ȣ���>��
C.ƽ��rSO2���D���ʣ���>��D.ƽ��rSO2���w�e�֔�(sh��)����>��
�鿴�𰸺ͽ���>>
����ʡ��(li��n)�W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com