
【題目】合成氣(主要成分為CO、CO2和H2)是重要的化工原料,可利用合成氣在催化劑存在下直接制備二甲醚(CH3OCH3)。
己知:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-49.0kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.0kJ·mol-1
CO2(g)+H2(g)![]() CO(g)+H2O(g) △H2=+41.1 kJ·mol-1
CO(g)+H2O(g) △H2=+41.1 kJ·mol-1
2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H3=-24.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H3=-24.5 kJ·mol-1
(1)工業上用CO2和H2在一定條件下反應直接制備二甲醚,主反應為: 2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)
①要使該反應速率和產率都增大,應該采取的措施是__________,減少副反應,大幅度提高二甲醚在產物中所占比率的關鍵因素是__________。
②一定條件下.上述主反應達到平衡狀態后,若改變反應的某一個條件,下列變化能說明平衡一定向正反應方向移動的是__________(單選,填標號)。
a.逆反應速率先增大后減小 b.H2的轉化率增大
c.反應物的體積百分含量減小 d.容器中的![]() 變小
變小
③在某壓強下,制備二甲醚的反應在不同溫度、不冋投料比時CO2的轉化率如圖(a)所示。T1溫度下,將6molCO2和12molH2充入10L的密閉容器中, 5 min后反應達到平衡狀態,則05 min內的平均反應速率v(CH3OCH3)=_____________;KA、 KB、 KC三者之間的大小關系為_______________。

(2)在適當條件下由CO和H2直接制備二甲醚,另一產物為水蒸氣。
①該反應的熱化學方程式是_________________。
②co的轉化率、二甲醚的產率與反應溫度的關系如圖(b)所示,請解釋溫度低于290℃時, CO轉化率較高而CH3OCH3產率較低的原因可能是___________。

(3)用甲醇,二甲醚混合液與CO在催化劑條件下還可合成醋酸。常溫下,醋酸的Ka=1.8×10-5,向 0.1 mol/L 醋酸溶液中滴加NaOH溶液至 =
=![]() 時,混合溶液的pH=__________,醋酸鈉水解反應的平衡常數值為__________。
時,混合溶液的pH=__________,醋酸鈉水解反應的平衡常數值為__________。
【答案】 加壓 催化劑 b 0.036mol·L-1·min-1 KA=KC>KB 2CO(g)+4H2(g)==CH3OCH3(g)+H2O(g) ΔH=-204.7kJ·mol-1 CO的轉化均為放熱反應,溫度較低時轉化率較高,但CO轉化為中間產物較多,轉化為目標產物較少 5 5.6×10-10
【解析】(1)①已知:ⅰ、CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H1=-49.0kJ·mol-1,ⅱ、2CH3OH(g)
CH3OH(g)+H2O(g)△H1=-49.0kJ·mol-1,ⅱ、2CH3OH(g)![]() CH3OCH3(g)+H2O(g)△H3=-24.5 kJ·mol-1,根據蓋斯定律可知ⅰ×2+ⅱ即得到2CO2(g)+6H2(g)
CH3OCH3(g)+H2O(g)△H3=-24.5 kJ·mol-1,根據蓋斯定律可知ⅰ×2+ⅱ即得到2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g)△H=-122.5 kJ·mol-1,即該反應是放熱的體積減小的可逆反應,所以要使該反應速率和產率都增大,應該采取的措施是加壓,減少副反應,大幅度提高二甲醚在產物中所占比率的關鍵因素是催化劑。②a.逆反應速率先增大后減小說明平衡向逆反應方向進行,a錯誤;b.H2的轉化率增大說明平衡一定向正反應方向移動,b正確;c.反應物的體積百分含量減小平衡不一定向正反應方向進行,c錯誤;d.容器中的
CH3OCH3(g)+3H2O(g)△H=-122.5 kJ·mol-1,即該反應是放熱的體積減小的可逆反應,所以要使該反應速率和產率都增大,應該采取的措施是加壓,減少副反應,大幅度提高二甲醚在產物中所占比率的關鍵因素是催化劑。②a.逆反應速率先增大后減小說明平衡向逆反應方向進行,a錯誤;b.H2的轉化率增大說明平衡一定向正反應方向移動,b正確;c.反應物的體積百分含量減小平衡不一定向正反應方向進行,c錯誤;d.容器中的![]() 變小平衡不一定向正反應方向進行,d錯誤,答案選b;③T1溫度下,將6molCO2和12molH2充入10L的密閉容器中,根據圖像可知平衡時CO2轉化率是0.6,則消耗CO2是3.6mol,生成二甲醚是1.8mol,濃度是0.18mol/L,所以05 min內的平均反應速率v(CH3OCH3)=0.18mol/L÷5min=0.036mol·L-1·min-1;正反應放熱,溫度越低CO2轉化率越高,平衡常數越大,溫度是T1<T2,由于平衡常數只與溫度有關系,所以KA、 KB、 KC三者之間的大小關系為KA=KC>KB。(2)①己知:ⅲ、2CO2(g)+6H2(g)
變小平衡不一定向正反應方向進行,d錯誤,答案選b;③T1溫度下,將6molCO2和12molH2充入10L的密閉容器中,根據圖像可知平衡時CO2轉化率是0.6,則消耗CO2是3.6mol,生成二甲醚是1.8mol,濃度是0.18mol/L,所以05 min內的平均反應速率v(CH3OCH3)=0.18mol/L÷5min=0.036mol·L-1·min-1;正反應放熱,溫度越低CO2轉化率越高,平衡常數越大,溫度是T1<T2,由于平衡常數只與溫度有關系,所以KA、 KB、 KC三者之間的大小關系為KA=KC>KB。(2)①己知:ⅲ、2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g)△H=-122.5 kJ·mol-1,ⅳ、CO2(g)+H2(g)
CH3OCH3(g)+3H2O(g)△H=-122.5 kJ·mol-1,ⅳ、CO2(g)+H2(g)![]() CO(g)+H2O(g) △H2=+41.1 kJ·mol-1,根據蓋斯定律可知ⅲ+ⅳ×2即得到熱化學方程式是2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g) ΔH=-204.7kJ·mol-1。②由于CO的轉化均為放熱反應,溫度較低時轉化率較高,但CO轉化為中間產物較多,所以轉化為目標產物較少;(3)根據醋酸的電離平衡常數表達式
CO(g)+H2O(g) △H2=+41.1 kJ·mol-1,根據蓋斯定律可知ⅲ+ⅳ×2即得到熱化學方程式是2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g) ΔH=-204.7kJ·mol-1。②由于CO的轉化均為放熱反應,溫度較低時轉化率較高,但CO轉化為中間產物較多,所以轉化為目標產物較少;(3)根據醋酸的電離平衡常數表達式 可知c(H+)=
可知c(H+)=  =10-5mol/L,所以混合溶液的pH=5,醋酸鈉水解反應的平衡常數值為
=10-5mol/L,所以混合溶液的pH=5,醋酸鈉水解反應的平衡常數值為![]() =5.6×10-10。
=5.6×10-10。


 考前必練系列答案
考前必練系列答案科目:高中化學 來源: 題型:
【題目】H2CO3 和 H2C2O4 都是二元弱酸,不同 pH 環境下它們不同形態的粒子的組成百分率如圖所示:

下列說法正確的是
A. 在 pH 為 6.37 及 10.25 時,溶液中 c(H2CO3)=c(HCO3-)=c(CO32-)
B. 反應 HCO3-+H2O![]() H2CO3+OH-的平衡常數為 10-7.63
H2CO3+OH-的平衡常數為 10-7.63
C. 0.1 molL-1 NaHC2O4 溶液中 c(HC2O4-)+2c(C2O42-)+c(H2C2O4) =0.1 molL-1
D. 往 Na2CO3 溶液中加入少量草酸溶液,發生反應:CO32-+H2C2O4=HCO3-+HC2O4-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I、依據事實,寫出下列反應的熱化學方程式。
(1)在25 ℃、101 kPa下,1 g甲烷燃燒生成CO2和液態水時放熱55.625 kJ。則表示甲烷燃燒熱的熱化學方程式為________________________。
(2)若適量的N2和O2完全反應,每生成23 g NO2需要吸收16.95 kJ熱量,則表示該反應的熱化學方程式為______________。
(3)在25 ℃、101 kPa條件下,C(s)、H2(g)、CH3COOH(1)的燃燒熱分別為393.5 kJ/mol、285.8 kJ/mol、870.3 kJ/mol,則2C(s)+2H2(g)+O2(g)===CH3COOH(1)的反應熱ΔH為________。
II、鋅錳干電池是應用最普遍的電池之一。其基本反應為:
X極:Zn-2e-===Zn2+
Y極:2MnO2+2NH![]() +2e-===Mn2O3+2NH3+H2O
+2e-===Mn2O3+2NH3+H2O
(1)X是電池的________(填“正”或“負”,下同)極,Y是電池的________極。
(2)該電池總反應的離子方程式為:_______________________。
(3)若反應消耗16.25gZn,則電池中轉移電子的物質的量為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A~H八種短周期主族元素在周期表中的相對位置如下圖所示,已知C元素形成的單質有“國防金屬”的美譽,E的最高價氧化物對應的水化物能與E的最簡單氫化物反應生成離子化合物。

(1)寫出B、G對應的元素符號______________ 。
(2)D元素在周期表中的位置為______________。
(3)B、E、F的簡單離子半徑由大到小的順序為______________(寫離子符號)。
(4)上述元素所形成的氣態單質中能用于飲用水消毒的是______________(寫化學式)。
(5)B的單質在F的單質中燃燒的火焰顏色為______________,所形成化合物的電子式為______________。
(6)C元素的單質可以在D和F組成的一種氣態化合物中燃燒,寫出該反應的化學方程式________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,濃度均為1.0mol/L的HX溶液、HY溶液、HY和 NaY的混合溶液,分別加水稀釋,稀釋后溶液的pH隨濃度的變化如圖所示,下列敘述正確的是( )
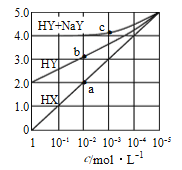
A. HX是強酸,溶液每稀釋10倍,pH始終增大1
B. 常溫下HY的電離常數為1.0×10-4
C. 溶液中水的電離程度:a點大于b點
D. c 點溶液中:c(Na+)>c(Y-)>c(HY)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物I的分子式為C6H10O4,75%的A溶液常用于醫療消毒,與I相關的反應如下:

根據以上信息回答下列問題。
(1)寫出A中所含官能團的名稱_______;B的結構簡式_______。
(2)寫出D→E的化學方程式_______。
(3)寫出F的同分異構體的結構簡式(不要求環狀)_______。
(4)工業上用B與O2在催化劑條件下生產環氧乙烷,寫出該反應的化學方程式_______。
(5)若1molG可以和2molNaHCO3反應,則I可能的結構簡式為_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列除雜質的方法不正確的是 ( )
A. 銅粉中混有鐵粉:加入過量鹽酸充分反應,過濾
B. CO2中混有HCl:將其通入NaOH溶液,洗氣
C. NaHCO3溶液中混有少量Na2CO3:往該溶液中通入過量CO2氣體
D. FeCl2溶液中混有少量FeCl3:加入Fe粉
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】能源是經濟增長與社會發展的重要物質基礎,美國馬奇蒂博士對世界一次能源替代趨勢曾作如下預測:

回答下列問題:
(1)上圖化石能源中屬于較清潔的能源是_________
(2)核電廠的燃料一般由0.71%235U99.28%238U及0.0058%234U組成
①235U238U234U三種核素之間的關系是______________
②235g核素![]() 發生裂變反應:
發生裂變反應: ![]() ,凈產生的中子
,凈產生的中子![]() 數為_______
數為_______
(3)下圖是氫能的制備及利用的途徑之一,涉及能量轉化方式有___________(填代號)

a光能→化學能 b電能→化學能 c化學能→電能
(4)目前實現煤的綜合利用的主要途徑是煤的干餾煤的氣化和液化
①煤的干餾屬于變化______________(填物理或化學)
②煤的氣化過程發生的主要反應是____________
(5)可燃冰屬于新能源,我國是全球第一個成功穩定開采可燃冰的國家某種可燃冰(甲烷水合物)晶體中,平均每46個水分子構成8個分子籠,每個分子籠可容納1個甲烷分子或水分子,若這8個分子籠中有6個容納的是甲烷分子,另外2個被水分子填充,則這種可燃冰的平均組成可表示為____________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為探究Ba(NO3)2和BaCl2的性質,某課外小組同學進行下列實驗。
(1)甲組同學向Ba(NO3)2溶液中通入SO2,有白色沉淀生成。向BaCl2溶液中通入SO2,無明顯現象。
①向Ba(NO3)2溶液中通入SO2產生的沉淀為___________(填化學式)。
②若向通入SO2的BaCl2溶液中再加入H2O2,也可產生白色沉淀,則該反應的離子方程式為________________。
(2)乙組同學向BaCl2溶液中同時通入NH3和SO2,然后滴入Na2CrO4溶液,沉淀由____(填“白色”或“黃色”,下同)轉變為_____。[巳知:BaCrO4為黃色固體,Ksp(BaCrO4)sp(BaSO3)]
(3)已知25 ℃時,Ksp(BaSO3)=5.5×10-7,Ksp(BaSO4)= 1.1×10-10,則該溫度下,反應:
BaSO3(s) +SO42-(aq)![]() BaSO4(s) +SO32-(aq)的平衡常數為__________。
BaSO4(s) +SO32-(aq)的平衡常數為__________。
(4)向Ba(NO3)2溶液中加入少量稀硫酸調至溶液pH為2.5,加入少量新制的納米鐵粉,充分反應后,加入NaOH溶液調至堿性,產生白色沉淀。一段時間后沉淀變為灰綠色,最后變為紅褐色,將懸濁液微熱,可產生使濕潤的紅色石蕊試紙變藍的氣體。則納米鐵粉與Ba(NO3)2酸性溶液發生的主要反應的離子方程式為_______________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com