
甲醇燃料分為甲醇汽油和甲醇柴油。工業上合成甲醇的方法很多。
(1)一定條件下發生反應:
①CO2(g) +3H2(g) =CH3OH(g)+H2O(g) ? △H1????
②2CO(g) +O2(g) =2CO2(g)?? △H2
③2H2(g)+O2(g) =2H2O(g)????????? △H3
則CO(g) + 2H2(g)  CH3OH(g) 的△H=??????????????? 。
CH3OH(g) 的△H=??????????????? 。
(2)在容積為2L的密閉容器中進行反應: CO(g)+2H2(g) CH3OH(g) ,其他條件不變,在300℃和500℃時,物質的量n(CH3OH) 與反應時間t的變化曲線如圖所示。該反應的△H???? 0 (填>、<或=)。
CH3OH(g) ,其他條件不變,在300℃和500℃時,物質的量n(CH3OH) 與反應時間t的變化曲線如圖所示。該反應的△H???? 0 (填>、<或=)。

(3)若要提高甲醇的產率,可采取的措施有____________(填字母)。
A.縮小容器體積
B.降低溫度
C.升高溫度
D.使用合適的催化劑
E.將甲醇從混合體系中分離出來
(4)CH4和H2O在催化劑表面發生反應CH4+H2O CO+3H2,T℃時,向1 L密閉容器中投入1 mol CH4和1 mol H2O(g),5小時后測得反應體系達到平衡狀態,此時CH4的轉化率為50% ,計算該溫度下的平衡常數???? (結果保留小數點后兩位數字)。
CO+3H2,T℃時,向1 L密閉容器中投入1 mol CH4和1 mol H2O(g),5小時后測得反應體系達到平衡狀態,此時CH4的轉化率為50% ,計算該溫度下的平衡常數???? (結果保留小數點后兩位數字)。
(5)以甲醇為燃料的新型電池,其成本大大低于以氫為燃料的傳統燃料電池,目前得到廣泛的研究,如圖是目前研究較多的一類固體氧化物燃料電池工作原理示意圖。回答下列問題:

①B極的電極反應式為????????????????????? 。
②若用該燃料電池做電源,用石墨做電極電解硫酸銅溶液,當電路中轉移1mole- 時,實際上消耗的甲醇的質量比理論上大,可能原因是????????????????????? 。
(6)25℃時,草酸鈣的Ksp=4.0×10-8,碳酸鈣的Ksp=2.5×10-9。向20ml碳酸鈣的飽和溶液中逐滴加入8.0×10-4 mol·L-1的草酸鉀溶液20ml,能否產生沉淀?????? (填“能”或“否”)。
(1)△H1+ △H2 -
△H2 - △H3
△H3
(2 <
(3)ABE
(4)6.75?
(5)① CH3OH + 3O2- -6e-= CO2+ 2H2O;?
②甲醇不完全被氧化,生成C或CO? 或 電池能量轉化率達不到100% (6)否
【解析】
試題分析:(1)①+  ②—
②— ③。整理可得:CO(g) + 2H2(g)
③。整理可得:CO(g) + 2H2(g) CH3OH(g) 的△H=△H1+
CH3OH(g) 的△H=△H1+ △H2 -
△H2 - △H3。(2)由圖像可以看出:升高溫度,平衡時CH3OH的含量降低,說明升高溫度,化學平衡向逆反應方向移動,根據平衡移動原理,升高溫度化學平衡向吸熱反應方向移動,逆反應方向為吸熱反應,所以正反應為放熱反應。因此△H<0. (3)若要提高甲醇的產率,應該使平衡正向移動。由于該反應的正反應為氣體體積縮小的放熱反應,根據平衡移動原理,降低溫度、增大壓強(即縮小容器體積)增大反應物的濃度或把甲醇從反應體系中分離出來。因此選項為A、B、E。(4)根據反應方程式CH4+H2O
△H3。(2)由圖像可以看出:升高溫度,平衡時CH3OH的含量降低,說明升高溫度,化學平衡向逆反應方向移動,根據平衡移動原理,升高溫度化學平衡向吸熱反應方向移動,逆反應方向為吸熱反應,所以正反應為放熱反應。因此△H<0. (3)若要提高甲醇的產率,應該使平衡正向移動。由于該反應的正反應為氣體體積縮小的放熱反應,根據平衡移動原理,降低溫度、增大壓強(即縮小容器體積)增大反應物的濃度或把甲醇從反應體系中分離出來。因此選項為A、B、E。(4)根據反應方程式CH4+H2O CO+3H2中各種物質的相互關系及甲烷的轉化率可知:當反應達到平衡時,c(CH4)=0.5mol/L;c(H2O)=0.5mol/L;c(CO)=0.5mol/L;c(H2)=1.5mol/L.化學平衡狀態是可逆反應達到平衡狀態時,各種生成物濃度冪指數的乘積一各種反應物濃度冪指數乘積的比,所以
CO+3H2中各種物質的相互關系及甲烷的轉化率可知:當反應達到平衡時,c(CH4)=0.5mol/L;c(H2O)=0.5mol/L;c(CO)=0.5mol/L;c(H2)=1.5mol/L.化學平衡狀態是可逆反應達到平衡狀態時,各種生成物濃度冪指數的乘積一各種反應物濃度冪指數乘積的比,所以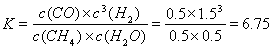 。(5)①通入甲醇的電極B為原電池的負極, B極的電極反應式為CH3OH + 3O2- -6e-= CO2+ 2H2O; 通入氧氣的電極為正極,正極發生反應:O2+ 4e-= 2O2- . ②當電路中轉移1mole- 時,實際上消耗的甲醇的質量比理論上大,可能原因是甲醇不完全被氧化,生成C或CO或電池能量轉化率達不到100%等。(6)碳酸鈣的Ksp=2.5×10-9,則c(Ca2+)·c(CO32-)=Ksp, c(Ca2+)=Ksp1/2=(2.5×10-9)1/2=5×10-5. 當向20ml碳酸鈣的飽和溶液中逐滴加入8.0×10-4 mol·L-1的草酸鉀溶液20ml 時,c(Ca2+)·c(C2O42-)=(1/2×5×10-5) ×(1/2×8.0×10-4)=10-8,小于草酸鈣的Ksp=4.0×10-8。所以不能產生草酸鈣沉淀。
。(5)①通入甲醇的電極B為原電池的負極, B極的電極反應式為CH3OH + 3O2- -6e-= CO2+ 2H2O; 通入氧氣的電極為正極,正極發生反應:O2+ 4e-= 2O2- . ②當電路中轉移1mole- 時,實際上消耗的甲醇的質量比理論上大,可能原因是甲醇不完全被氧化,生成C或CO或電池能量轉化率達不到100%等。(6)碳酸鈣的Ksp=2.5×10-9,則c(Ca2+)·c(CO32-)=Ksp, c(Ca2+)=Ksp1/2=(2.5×10-9)1/2=5×10-5. 當向20ml碳酸鈣的飽和溶液中逐滴加入8.0×10-4 mol·L-1的草酸鉀溶液20ml 時,c(Ca2+)·c(C2O42-)=(1/2×5×10-5) ×(1/2×8.0×10-4)=10-8,小于草酸鈣的Ksp=4.0×10-8。所以不能產生草酸鈣沉淀。
考點:考查原電池、電解池的反應原理及電極式的書寫、熱化學方程式的書寫、反應熱與化學平衡常數的計算、外界條件對化學平衡的影響等知識。


科目:高中化學 來源:中學教材全解 高中化學 必修 化學與技術 (配山東科學技術出版社實驗教科書) 山東科學技術出版社實驗教科書 題型:043
內燃機是將化學能轉化為機械能的裝置,根據燃料不同可分為汽油機和柴油機等類型.汽油機和柴油機的工作原理均為利用燃料燃燒產生大量的氣體和熱能,推動活塞進行往復運動.汽油機和柴油機工作原理的區別在于壓縮的工作物質和點火方式不同:汽油是將汽油霧化后和空氣混合,利用活塞下行吸入氣缸,然后活塞上行將其壓縮,到一定體積(活塞幾乎上行到頂端)后采用火花塞(俗稱火嘴,一種采用高壓放電產生火花的裝置)打火,從而點燃混合氣體使之體積劇烈膨脹推動活塞下行,當活塞下行到底部時,活門打開,利用二次的壓力排出氣體,完成一個循環過程;而柴油機則是吸入空氣進行壓縮,到一定程度產生高溫高壓后,噴入霧化的柴油,由于此時壓縮空氣的溫度已經超過柴油的燃點,柴油立即燃燒推動活塞運行.柴油機的壓縮比遠高于汽油機(這也是柴油機效率高于汽油機的原因之一).根據上述信息回答下列問題:
(1)內燃機推動活塞往復的直線運動要通過連桿和________轉換為圓周運動,從而驅動車輛和其他機械進行運轉.
(2)某196柴油機的壓縮比為1∶20,已知室溫27℃,大氣壓強1.01×105 Pa,測得壓縮到最大限度時,氣缸內壓強為3.03×106 Pa,此時混合氣體的溫度是________.
(3)檢測發動機尾氣發現,汽油機尾氣中氮的氧化物(以NOx表示)含量遠遠高于柴油機尾氣,請解釋原因,并寫出相關的化學方程式.
(4)鑒于石油儲量,且汽油機和柴油機排出的尾氣都嚴重污染大氣,科學家們正在努力嘗試采用其他燃料,已經成功的方案是采用甲醇(可以通過煤液化工藝制得)來部分替代汽油.試寫出甲醇在汽缸中燃燒的化學方程式.
(5)近日《羊城晚報》登載了這樣一條新聞:某摩登少女駕摩托車上街購物,不幸遭遇飛賊搶劫,開走她的摩托車.此時少女迅速從手袋中拿出一小物件,對著已逃出幾十米開外的摩托車一按按鈕.只見遠處疾馳的摩托車立即熄火停車而將飛賊拋出老遠.你認為這種“遙控停車裝置”最可能的原理是什么?(請用最簡潔的文字回答,不超過20字).
查看答案和解析>>
科目:高中化學 來源:2013-2014學年河北省高三3月摸底考試理綜化學試卷(解析版) 題型:填空題
甲醇燃料分為甲醇汽油和甲醇柴油。工業上合成甲醇的方法很多。
(1)一定條件下發生反應:
CO2(g) +3H2(g) =CH3OH(g)+H2O(g)? △H1
2CO (g) +O2(g) =2CO2(g)?? △H2
2H2(g)+O2(g) =2H2O(g)??? △H3
則 CO(g) + 2H2(g)  CH3OH(g) 的△H=??????????????? 。
CH3OH(g) 的△H=??????????????? 。
(2)在容積為2L的密閉容器中進行反應:CO(g)+2H2(g) CH3OH(g) ,其他條件不變,在300℃和500℃時,物質的量n(CH3OH) 與反應時間t的變化曲線如圖所示。該反應的△H???? 0 (填>、<或=)。
CH3OH(g) ,其他條件不變,在300℃和500℃時,物質的量n(CH3OH) 與反應時間t的變化曲線如圖所示。該反應的△H???? 0 (填>、<或=)。

(3)若要提高甲醇的產率,可采取的措施有____________(填字母)。
A.縮小容器體積
B.降低溫度
C.升高溫度
D.使用合適的催化劑
E.將甲醇從混合體系中分離出來
(4)CH4和H2O在催化劑表面發生反應CH4+H2O CO+3H2,T℃時,向1 L密閉容器中投入1 mol CH4和1 mol H2O(g),5小時后測得反應體系達到平衡狀態,此時CH4的轉化率為50% ,計算該溫度下的平衡常數????? (結果保留小數點后兩位數字)。
CO+3H2,T℃時,向1 L密閉容器中投入1 mol CH4和1 mol H2O(g),5小時后測得反應體系達到平衡狀態,此時CH4的轉化率為50% ,計算該溫度下的平衡常數????? (結果保留小數點后兩位數字)。
(5)以甲醇為燃料的新型電池,其成本大大低于以氫為燃料的 傳統燃料電池,目前得到廣泛的研究,如圖是目前研究較多的一類固體氧化物燃料電池工作原理示意圖。回答下列問題:
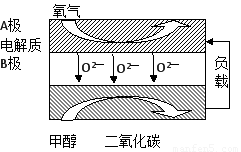
①B極的電極反應式為????????????????????? 。
②若用該燃料電池做電源,用石墨做電極電解硫酸銅溶液,當電路中轉移1mole- 時,實際上消耗的甲醇的質量比理論上大,可能原因是????????????????????? 。
(6)25℃時,草酸鈣的Ksp=4.0×10-8,碳酸鈣的Ksp=2.5×10-9。向20ml碳酸鈣的飽和溶液中逐滴加入8.0×10-4 mol·L-1的草酸鉀溶液20ml,能否產生沉淀?????? (填“能”或“否”)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com