
【題目】硫代硫酸鈉(Na2S2O3)俗稱保險粉,可用于照相業作定影劑,也可用于紙漿漂白作脫氯劑等。實驗室可通過如下反應制取:2Na2S+Na2CO3+4SO2===3Na2S2O3+CO2。
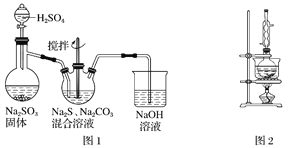
(1)用圖1所示裝置制取Na2S2O3,其中NaOH溶液的作用是________________________。如將分液漏斗中的H2SO4改成濃鹽酸,則三頸燒瓶內除生成Na2S2O3外,還有________(填化學式)雜質生成。
(2)為測定所得保險粉樣品中Na2S2O3·5H2O的質量分數,可用標準碘溶液進行滴定,反應方程式為2Na2S2O3+I2===2NaI+Na2S4O6。
①利用KIO3、KI和HCl可配制標準碘溶液。寫出配制時所發生反應的離子方程式:_______________________________________________________________________。
②準確稱取一定質量的Na2S2O3·5H2O樣品于錐形瓶中,加水溶解,并滴加________作指示劑,用所配制的標準碘溶液滴定。滴定時所用的玻璃儀器除錐形瓶外,還有________。
③若滴定時振蕩不充分,剛看到溶液局部變色就停止滴定,則會使樣品中Na2S2O3·5H2O的質量分數的測量結果________(填“偏高”、“偏低”或“不變”)。
(3)本實驗對Na2S的純度要求較高,利用圖2所示的裝置可將工業級的Na2S提純。已知Na2S常溫下微溶于酒精,加熱時溶解度迅速增大,雜質不溶于酒精。提純步驟如下,請填寫實驗操作。
①將已稱量好的工業Na2S放入圓底燒瓶中,并加入一定質量的酒精和少量水;
②按圖2所示組裝所需儀器,向冷凝管中通入冷卻水,水浴加熱;
③待________________時,停止加熱,將燒瓶取下;
④____________________________________________________________________;
⑤____________________________________________________________________;
⑥將所得固體洗滌、干燥,得到Na2S·9H2O晶體。
【答案】 吸收SO2等尾氣,防止污染空氣 NaCl IO+5I-+6H+===3I2+3H2O 淀粉溶液 酸式滴定管 偏低 燒瓶中固體不再減少 趁熱過濾 將所得濾液冷卻結晶,過濾
【解析】試題分析:(1)用圖1所示裝置制取Na2S2O3,其中NaOH溶液的作用是吸收多余的二氧化硫氣體,防止污染空氣;如將分液漏斗中的H2SO4改成濃鹽酸,因為濃鹽酸易揮發,HCl與反應物反應生成NaCl,則三頸燒瓶內除Na2S2O3生成外,還有NaCl生成;
(2)①利用KIO3、KI和HCl可配制標準碘溶液,碘酸根離子與碘離子在酸性條件下發生歧化反應生成碘單質,離子方程式是IO3-+5I-+6H+===3I2+3H2O;
②用標準碘溶液進行滴定Na2S2O3溶液,所以應用淀粉作指示劑,溶液變藍色,說明達到滴定終點;因為碘具有氧化性,所以標準碘溶液應用酸式滴定管盛放,則滴定時所用的玻璃儀器除錐形瓶外,還有酸式滴定管;
③ 若滴定時振蕩不充分,剛看到溶液局部變色就停止滴定,此時并未達到滴定終點,消耗碘溶液的體積偏少,造成樣品中Na2S2O3·5H2O的質量分數偏低;
(3)③因為硫化鈉中的雜質不溶于酒精,所以等到燒瓶中固體不再減少時,說明硫化鈉全部溶液酒精;
④ 因為硫化鈉在酒精中的溶解度隨溫度升高而增大,若溫度降低,則會有部分硫化鈉固體析出,所以此時應趁熱過濾,除去雜質;
⑤ 上步中得到的濾液主要是硫化鈉的酒精溶液,因為溫度降低,硫化鈉的溶解度減小,所以將所得濾液冷卻結晶,過濾,可得到硫化鈉晶體。


科目:高中化學 來源: 題型:
【題目】下列關于自然界中碳循環(如圖)的說法中,不正確的是( ) 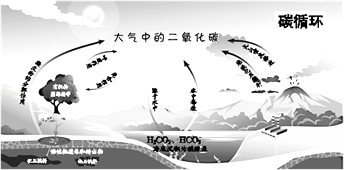
A.呼吸作用涉及氧化還原反應
B.碳循環具有全球性
C.含碳化合物可相互轉化
D.碳元素均被氧化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮的固定對人類的生存發展具有重要意義,科學家一直致力于“人工固氮”的新方法研究。
(1)豆科植物的根瘤菌含有一種固氮酶,能在常溫下將空氣中的氮氣轉化為自身生長所需的含氮化合物,下列說法錯誤的是____(填標號)。
a.固氮酶是一種蛋白質
b.固氮酶能降低固氮反應發生所需的能量
c.固氮酶能使固氮反應的平衡正向移動
d.固氮酶能加快固氮反應的速率
(2)合成氨是目前最重要的固氮方法。下圖為合成氨反應N2(g)+3H2(g) ![]() 2NH3(g)在不同溫度和壓強、使用相同催化劑條件下,初始時氮氣、氫氣的體積之比為1∶3時,平衡混合物中氨的體積分數的變化曲線。
2NH3(g)在不同溫度和壓強、使用相同催化劑條件下,初始時氮氣、氫氣的體積之比為1∶3時,平衡混合物中氨的體積分數的變化曲線。
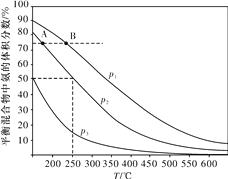
①A、B兩平衡狀態相比較,前者較大的是____(填標號)。
a.平衡常數
b.平衡混合物的平均摩爾質量
c.氫氣的轉化率
d.從反應開始至達到平衡狀態所需要的時間
②圖中p1、p2、p3由大到小的順序為____。
③在250 ℃、p2下,H2的轉化率為____%(結果保留小數點后一位)。
(3)據報道:在常溫、常壓、光照條件下,N2在催化劑(摻有少量Fe2O3的TiO2)表面與水發生反應,生成的主要產物為NH3和一種單質。已知:
①H2(g)+![]() O2(g)===H2O(l) ΔH1=-285.6 kJ/mol
O2(g)===H2O(l) ΔH1=-285.6 kJ/mol
②N2(g)+3H2(g) ![]() 2NH3(g) ΔH2=-92.2 kJ/mol
2NH3(g) ΔH2=-92.2 kJ/mol
寫出此條件下氮氣和水反應的熱化學方程式:___。
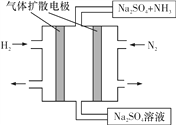
(4)下圖為一種常溫常壓下水溶液中電化學合成氨的實驗裝置示意圖。請據此寫出其正極反應的電極反應式:__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】還原沉淀法是處理含鉻(含Cr2O72﹣和CrO42﹣)工業廢水的常用方法,過程如下:
![]()
己知轉化過程中反應為:2CrO42﹣(aq)+2H+(aq)![]() Cr2O72﹣(aq)+H2O(1)。轉化后所得溶液中鉻元素含量為28.6g/L,CrO42﹣有10/11轉化為Cr2O72﹣。下列說法不正確的是
Cr2O72﹣(aq)+H2O(1)。轉化后所得溶液中鉻元素含量為28.6g/L,CrO42﹣有10/11轉化為Cr2O72﹣。下列說法不正確的是
A. 溶液顏色保持不變,說明上述可逆反應達到達平衡狀態
B. 若用綠礬(FeSO4·7H2O)(M=278)作還原劑,處理1L廢水,至少需要917.4g
C. 常溫下轉化反應的平衡常數K=1×1014,則轉化后所得溶液的pH=6
D. 常溫下Ksp[Cr(OH)3]=1×10﹣32,要使處理后廢水中c(Cr3+)降至1×10﹣5mol/L,應調溶液的pH=5
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D是4種前三周期元素,且原子序數逐漸增大,這四種元素的基態原子的未成對電子數和電子層數相等。請回答下列問題:
(1)D元素的基態原子價電子排布式是:____________________________________;
(2)A、B、C三種元素可以形成化合物A4B2C2,它是廚房調味品之一。1 mol A4B2C2中含有________molσ鍵,其中B原子采用的雜化方式為:_____________;
(3)元素F的原子序數是介于B和C之間的,元素B、C、F的電負性的大小順序是: _______________B、C、F的第一電離能的大小順序是____________(由大到小,用元素符號填空);
(4)隨著科學的發展和大型實驗裝置(如同步輻射和中子源)的建成,高壓技術在物質研究中發揮越來越重要的作用。高壓不僅會引發物質的相變,也會導致新類型化學鍵的形成。近年來就有多個關于超高壓下新型晶體的形成與結構的研究報道。NaCl 晶體在50~300GPa 的高壓下和Na 或Cl2反應,可以形成不同組成、不同結構的晶體。下圖給出其中三種晶體的晶胞(大球為氯原子,小球為鈉原子)。寫出A、B、C 的化學式。A:_______________; B:__________________; C:___________________

(5)磷化硼是一種受到高度關注的耐磨涂料,它可用作金屬的表面保護層。磷化硼可由三溴化硼和三溴化磷在氫氣中高溫反應合成。合成磷化硼的化學反應方程式:BBr3+PBr3+3H2=BP+6HBr
①分別畫出三溴化硼分子和三溴化磷分子的結構。_____________、_________________

磷化硼晶體中磷原子作面心立方最密堆積,硼原子填入部分四面體空隙中。磷化硼的晶胞示意圖如下:

②已知磷化硼的晶胞參數a = 478 pm,計算晶體中硼原子和磷原子的核間距(dB-P)(寫出計算式,不要求計算結果)____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】單質X和Y相互反應生成X2+和Y2-,現有下列敘述其中正確的是( )
①X被氧化 ②X是氧化劑 ③X具有氧化性
④Y2-是還原產物 ⑤Y2-具有還原性 ⑥X2+具有氧化性
A.①②③④B.①④⑤⑥C.②③④D.①③④⑤
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】到目前為止,由化學能轉變的熱能或電能仍然是人類使用最廣泛的能源.
(1)在25℃、101kPa下,16g的甲烷完全燃燒生成CO2和液態水時放出a kJ(a>0)的熱量,則表示甲烷燃燒熱的熱化學方程式為 .
(2)化學反應中放出的熱能(焓變,△H)與反應物和生成物的鍵能(E)有關. ①圖1是N2(g)和H2(g)發生反應生成1mol NH3(g)過程中的能量變化示意圖,該反應過程是(填“放熱”或“吸熱”)過程,請寫出生成2mol NH3的熱化學方程式: . 
②已知:
化學鍵 | H﹣H | N≡N |
鍵能(kJ/mol) | 435 | 943 |
試根據上表及圖1中的數據計算N﹣H鍵的鍵能為kJ/mol.
③若起始時向容器內放入1mol N2和3mol H2 , 10分鐘后N2的轉化率為15%,則該反應進行到此時共放出的熱量為kJ.
(3)①二氧化碳的捕集、利用是我國能源領域的一個重要研究方向.工業上用CO2和H2反應合成二甲醚.已知: CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H1=﹣53.7kJ/mol
CH3OCH3(g)+H2O (g)═2CH3OH(g)△H2=+23.4kJ/mol
則:2CO2(g)+6H2(g)CH3OCH3 (g)+3H2O(g)△H3=kJ/mol.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如表是a~m九種元素在周期表中的位置,請回答下列問題:
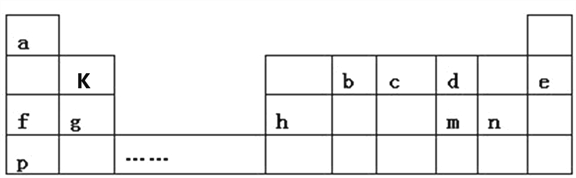
(1)m的陰離子結構示意圖為____________。
(2)b的最高價氧化物的電子式為____________;用電子式表示f2 d2的形成過程_______________________。
(3)d、g、n形成的簡單離子的半徑由大到小的順序為___________(用離子符號填寫)。
(4)f、g、p的最高價氧化物的水化物堿性從強到弱的順序為__________(填化學式)。
(5)p和n兩種元素最高價氧化物的水化物相互反應的化學反應方程式為___________。
(6)c的氫化物和c的最高價氧化物對應水化物之間反應的化學方程式為__________。
(7)k的氧化物與氫氧化鈉溶液反應的離子方程式為________________________。
(8)以上元素組成的物質有下列框圖中的轉化關系,其中甲為10電子微粒。

①丁屬于_____________(選填“離子化合物”或“共價化合物”)。
②請寫出h單質與乙反應的化學方程式_____________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com