
(1)在一定溫度下,向一個(gè)容積不變的容器中,通入2molN2和8molH2及固體催化劑,使之反應(yīng)。已知:N2(g)+3H2(g) 2NH3(g);△H=-92.2kJ·mol-1。平衡時(shí)容器內(nèi)氣體壓強(qiáng)為起始時(shí)的80%。(寫(xiě)出計(jì)算過(guò)程)
2NH3(g);△H=-92.2kJ·mol-1。平衡時(shí)容器內(nèi)氣體壓強(qiáng)為起始時(shí)的80%。(寫(xiě)出計(jì)算過(guò)程)
①平衡時(shí)N2的物質(zhì)的量 , H2的轉(zhuǎn)化率
②達(dá)到平衡時(shí),放出的熱量為 。
(2)在一個(gè)容積為500 mL的密閉容器中,充入5 mol H2和2 mol CO。在一定溫度和一定壓強(qiáng)下,發(fā)生如下反應(yīng):2H2(g)+CO(g)  CH3OH(g),經(jīng)過(guò)5 min后達(dá)到平衡狀態(tài)。若此時(shí)測(cè)得CH3OH蒸氣的濃度為2 mol/L,求:(寫(xiě)出計(jì)算過(guò)程)
CH3OH(g),經(jīng)過(guò)5 min后達(dá)到平衡狀態(tài)。若此時(shí)測(cè)得CH3OH蒸氣的濃度為2 mol/L,求:(寫(xiě)出計(jì)算過(guò)程)
①以H2的濃度變化表示的該反應(yīng)的速率
②達(dá)平衡時(shí)CO的轉(zhuǎn)化率
③該溫度下的K
(1)①1摩爾
②37.5%
③92.2kJ
(2)①v(H2)=0.8 mol/(L·min)
②50%
③0.028
【解析】
試題分析:解:(1)設(shè)反應(yīng)掉的氮?dú)獾奈镔|(zhì)的量為x,即
N2(g) +3H2(g)  2NH3(g)
2NH3(g)
起始的物質(zhì)的量(mol) 2 8 0
轉(zhuǎn)化的物質(zhì)的量(mol) x 3x 2x
平衡的物質(zhì)的量(mol)2-x 8-3x 2x
根據(jù)PV=nRT,所以(10-2x)/10=80%,所以x為1mol,
所以平衡時(shí)N2的物質(zhì)的量為2-1=1mol,
H2的轉(zhuǎn)化率=3x/8=3*1/8*100%=37.5%
達(dá)到平衡時(shí),放出的熱量=1*92.2kJ=92.2kJ
(2)設(shè)反應(yīng)掉的氫氣的物質(zhì)的量為x,即
2H2(g) +
CO(g)  CH3OH(g)
CH3OH(g)
起始的物質(zhì)的量(mol) 5 2 0
轉(zhuǎn)化的物質(zhì)的量(mol) x 0.5x 0.5x
平衡的物質(zhì)的量(mol) 5-x 2-0.5x 0.5x
有因?yàn)镃H3OH蒸氣的濃度為2 mol/L,所以0.5x=2×0.5,所以x=2mol,
所以以H2的濃度變化表示的反應(yīng)速率v(H2)="2/0.5/5=0.8" mol/(L·min),
達(dá)平衡時(shí)CO的轉(zhuǎn)化率=1/2×100%=50%,
K=c(CH3OH)/c2(H2)c(CO)=2/(6*6*2)=0.028。
考點(diǎn):化學(xué)反應(yīng),平衡常數(shù)
點(diǎn)評(píng):本題綜合考查了化學(xué)反應(yīng),平衡常數(shù)的相關(guān)計(jì)算,有一定的綜合性,考查的知識(shí)點(diǎn)比較全面,是一道不錯(cuò)的計(jì)算題


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學(xué)生10分鐘應(yīng)用題系列答案
小學(xué)生10分鐘應(yīng)用題系列答案
| 年級(jí) | 高中課程 | 年級(jí) | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來(lái)源: 題型:
| 1 |
| 3 |
| 1 |
| 3 |
| 1 |
| 3 |
| 1 |
| 3 |
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
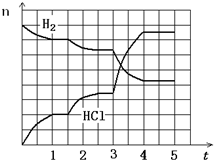 (2013?河?xùn)|區(qū)一模)工業(yè)上高純硅可以通過(guò)下列反應(yīng)制取:
(2013?河?xùn)|區(qū)一模)工業(yè)上高純硅可以通過(guò)下列反應(yīng)制取:| 高溫 |
| c4(HCl) |
| c(SiCl4)?c2(H2) |
| c4(HCl) |
| c(SiCl4)?c2(H2) |
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
| 高溫 |
| c12(HCl) |
| c3(SiCl4)c2(N2)c6(H2) |
| c12(HCl) |
| c3(SiCl4)c2(N2)c6(H2) |
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
| [CO2]3 |
| [CO]3 |
| [CO2]3 |
| [CO]3 |

查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
| c3(CO2) |
| c3(CO) |
| c3(CO2) |
| c3(CO) |
查看答案和解析>>
百度致信 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專(zhuān)區(qū) | 電信詐騙舉報(bào)專(zhuān)區(qū) | 涉歷史虛無(wú)主義有害信息舉報(bào)專(zhuān)區(qū) | 涉企侵權(quán)舉報(bào)專(zhuān)區(qū)
違法和不良信息舉報(bào)電話(huà):027-86699610 舉報(bào)郵箱:58377363@163.com