
| 離子 | 開始沉淀時的pH | 完全沉淀時的pH | 加堿溶解的pH |
| Fe2+ | 7.6 | 9.7 | |
| Fe3+ | 2.7 | 3.7 | |
| Al3+ | 3.8 | 4.7 | >8.5 |
| Mn2+ | 8.3 | 9.8 |
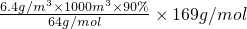 =15210g=15.21kg.
=15210g=15.21kg.

 暑假銜接培優教材浙江工商大學出版社系列答案
暑假銜接培優教材浙江工商大學出版社系列答案 欣語文化快樂暑假沈陽出版社系列答案
欣語文化快樂暑假沈陽出版社系列答案科目:高中化學 來源: 題型:

| 離子 | 開始沉淀時的pH | 完全沉淀時的pH | 加堿溶解的pH |
| Fe2+ | 7.6 | 9.7 | |
| Fe3+ | 2.7 | 3.7 | |
| Al3+ | 3.8 | 4.7 | >8.5 |
| Mn2+ | 8.3 | 9.8 |
查看答案和解析>>
科目:高中化學 來源: 題型:

| 離子 | 開始沉淀時的pH | 完全沉淀時的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
查看答案和解析>>
科目:高中化學 來源: 題型:
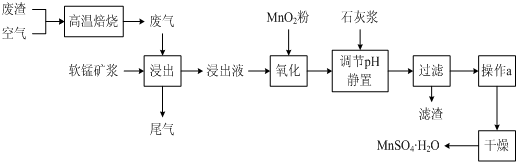
為了回收利用SO2,研究人員研制了利用低品位軟錳礦漿(主要成分是MnO2)吸收高溫焙燒含硫廢渣產生的SO2廢氣,制備硫酸錳晶體的生產流程,其流程示意圖如下:
已知,浸出液的pH<2,其中的金屬離子主要是Mn2+,還含有少量的Fe2+、Al3+等其他金屬離子。有關金屬離子形成氫氧化物沉淀時的pH見下表:
| 離子 | 開始沉淀時的pH | 完全沉淀時的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
請回答下列問題:
(1)寫出浸出過程中主要反應的化學方程式: ________________________。
(2)寫出氧化過程中主要反應的離子方程式: ______________________。
(3)在氧化后的液體中加入石灰漿,并用pH試紙測定調節pH,pH應調節范圍是____________。
(4)濾渣的主要成分有_________________________________________。
(5)下列各組試劑中,能準確測定尾氣中SO2含量的是__________。(填編號)
a. NaOH溶液、酚酞試液 b. 稀H2SO4酸化的KMnO4溶液
c. 碘水、淀粉溶液 d.氨水、酚酞試液
查看答案和解析>>
科目:高中化學 來源:2011屆江西省重點中學協作體高三第二次聯考(理綜)化學部分 題型:填空題
為了回收利用SO2,研究人員研制了利用低品位軟錳礦漿(主要成分是MnO2)吸收高溫焙燒含硫廢渣產生的SO2廢氣,制備硫酸錳晶體的生產流程,其流程示意圖如下:
已知,浸出液的pH<2,其中的金屬離子主要是Mn2+,還含有少量的Fe2+、Al3+等其他金屬離子。有關金屬離子形成氫氧化物沉淀時的pH見下表:
| 離子 | 開始沉淀時的pH | 完全沉淀時的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
 _____。
_____。查看答案和解析>>
科目:高中化學 來源:2010-2011學年江西省協作體高三第二次聯考(理綜)化學部分 題型:填空題
為了回收利用SO2,研究人員研制了利用低品位軟錳礦漿(主要成分是MnO2)吸收高溫焙燒含硫廢渣產生的SO2廢氣,制備硫酸錳晶體的生產流程,其流程示意圖如下:

已知,浸出液的pH<2,其中的金屬離子主要是Mn2+,還含有少量的Fe2+、Al3+等其他金屬離子。有關金屬離子形成氫氧化物沉淀時的pH見下表:
|
離子 |
開始沉淀時的pH |
完全沉淀時的pH |
|
Fe2+ |
7.6 |
9.7 |
|
Fe3+ |
2.7 |
3.7 |
|
Al3+ |
3.8 |
4.7 |
|
Mn2+ |
8.3 |
9.8 |
請回答下列問題:
(1)寫出浸出過程中主要反應的化學方程式: ________________________。
(2)寫出氧化過程中主要反應的離子方程式: ______________________。
(3)在氧化后的液體中加入石灰漿,并用pH試紙測定調節pH,pH應調節范圍是____________。
(4)濾渣的主要成分有_________________________________________。
(5)下列各組試劑中,能準確測定尾氣中SO2含量的是__________。(填編號)
a. NaOH溶液、酚酞試液 b. 稀H2SO4酸化的KMnO4溶液
c. 碘水、淀粉溶液 d. 氨水、酚酞試液
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com