
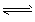 2NH3 (g)。已知加入1mol N2和3mol H2,在恒壓條件下,達到平衡時生成amol NH3。[見下表中編號(1)的一行];在恒容條件下,達到平衡時生成
2NH3 (g)。已知加入1mol N2和3mol H2,在恒壓條件下,達到平衡時生成amol NH3。[見下表中編號(1)的一行];在恒容條件下,達到平衡時生成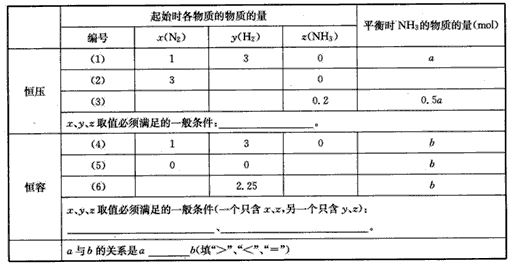
科目:高中化學 來源: 題型:閱讀理解
 生物質資源是一種污染小的可再生能源.生物質的主要轉化途徑及主要產物如圖.
生物質資源是一種污染小的可再生能源.生物質的主要轉化途徑及主要產物如圖.| 容器 | 甲 | 乙 | 丙 |
| 反應物投入量 | 1molCO、2molH2 | 1mol CH3OH | 2molCO、4molH2 |
| CH3OH的濃度(mol/L) | c1 | c2 | c3 |
| 反應的能量變化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
| 平衡常數 | K1 | K2 | K3 |
| 反應物轉化率 | α 1 | α 2 | α 3 |

查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| 1.容器 | 2.甲 | 3.乙 | 4.丙 |
| 5.反應物投入量 | 6.1molCO、2molH2 | 7.l molCH3OH | 8.2molCO、4molH2 |
| 9.CH30H昀濃度(mol/L) | 10.cl | 11.c2 | 12.c3 |
| 13.反應的能量變化 | 14.放出Q1kJ | 15.吸收Q2kJ | 16.放出Q3kJ |
| 17.平衡常數 | 18.Kl | 19.K2 | 20.K3 |
| 21.反應物轉化率 | 22.al | 23.a2 | 24.a3 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| H | + 4 |
| O | - 2 |
| H | + 4 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
(16分)生物質資源是一種污染小的可再生能源。生物質的主
(1)下列有關說法正確的是 。
a.生物質能,本質上能量來源于太陽能
b.由纖維素水解獲得的乙醇作燃料是利用了生物質能
c.生物質裂解獲得的汽油、柴油等屬于純凈物
d.由植物秸桿等厭氧發酵獲得的沼氣,主要成分是甲烷
(2)由生物質能獲得的CO和H2,可以合成甲醇和二甲醚(CH3OCH3)及許多烴類物質。當兩者1∶1催化反應,其原子利用率達100%,合成的物質可能是 。
a.汽油 b.甲醇 c.甲醛 d.乙酸
(3)甲醇是一種重要的化工原料,工業上合成甲醇的反應:
CO(g)+2H2(g)CH3OH(g) △H= -90.8kJ·mol-1。
若在溫度、容積相同的3個密閉容器中,按不同方式投入反應物,保持恒溫、恒容,測得反應達到平衡時的有關數據如下:
| 容器 | 甲 | 乙 | 丙 |
| 反應物投入量 | 1molCO 、2molH2 | 1mol CH3OH | 2molCO、4molH2 |
| CH3OH的濃度(mol/L) | c1 | c2 | c3 |
| 反應的能量變化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
| 平衡常數 | K1 | K2 | K3 |
| 反應物轉化率 | α 1 | α 2 | α 3 |
下列說法正確的是 。
a. c1 = c2 b. 2Q1 = Q3 c. K1=K3 d. α2+ α3< 100%
(4)在一定溫度和壓強下,CO和H2催化合成二甲醚的反應為:
3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)
①若一體積可變的密閉容器中充入3 mol H2、3 mol CO、1 mol CH3OCH3、1 mol CO2,經一定時間達到平衡,并測得平衡時混合氣體密度是同溫同壓下起始時的1.6倍。則:①反應開始時正、逆反應速率的大小:v(正)____v(逆)(填“ >”、“ < ”或“=”),理由是
。平衡時n(CH3OCH3)= mol。
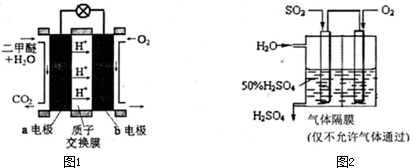
②右圖為綠色電源“直接二甲醚燃料電池”的工作原理示意圖。
b電極是 極;a電極的反應式為 。
查看答案和解析>>
科目:高中化學 來源:2012屆度本溪市高二下學期期末化學試卷 題型:填空題
(14分)生物質資源是一種污染小的可再生能源。生物質的主要轉化途徑及主要產物如下圖。

(1)下列有關說法正確的是 。
a.生物質能,本質上能量來源于太陽能
b.由纖維素水解獲得的乙醇作燃料是利用了生物質能
c.生物質裂解獲得的汽油、柴油等屬于純凈物
d.由植物秸桿等厭氧發酵獲得的沼氣,主要成分是甲烷
(2)由生物質能獲得的CO和H2,可以合成甲醇和二甲醚(CH3OCH3)及許多烴類物質。當兩者1∶1催化反應,其原子利用率達100%,合成的物質可能是 。
a.汽油 b.甲醇 c.甲醛 d.乙酸
(3)甲醇是一種重要的化工原料,工業上合成甲醇的反應: CO(g)+2H2(g) CH3OH(g) △H= -90.8kJ·mol-1。
CH3OH(g) △H= -90.8kJ·mol-1。
若在溫度、容積相同的3個密閉容器中,按不同方式投入反應物,保持恒溫、恒容,測得反應達到平衡時的有關數據如下:
|
容器 |
甲 |
乙 |
丙 |
|
反應物投入量 |
1molCO 、2molH2 |
1mol CH3OH |
2molCO、4molH2 |
|
CH3OH的濃度(mol/L) |
c1 |
c2 |
c3 |
|
反應的能量變化 |
放出Q1 kJ |
吸收Q2 kJ |
放出Q3 kJ |
|
平衡常數 |
K1 |
K2 |
K3 |
|
反應物轉化率 |
α 1 |
α 2 |
α 3 |
下列說法正確的是 。
a. c1 = c2 b. 2Q1 = Q3 c. K1=K3 d. α2+ α3< 100%
(4)在一定溫度和壓強下,CO和H2催化合成二甲醚的反應為:
3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)
CH3OCH3(g)+CO2(g)
①若一體積可變的密閉容器中充入3 mol H2、3 mol CO、1 mol CH3OCH3、1 mol CO2,經一定時間達到平衡,并測得平衡時混合氣體密度是同溫同壓下起始時的1.6倍。則:①反應開始時正、逆反應速率的大小:v(正)____v(逆)(填“ >”、“ < ”或“=”),理由是
。平衡時n(CH3OCH3)= mol。
②下圖為綠色電源“直接二甲醚燃料電池”的工作原理示意圖。

b電極是 極;a電極的反應式為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com