
【題目】在80℃時,將0.4mol的四氧化二氮氣體充入2L已抽空的固定容積的密閉容器中,隔一段時間對該容器內的物質進行分析,得到如下數據:反應進行至100s后將反應混合物的溫度降低,發現氣體的顏色變淺.
時間(s) | 0 | 20 | 40 | 60 | 80 | 100 |
C(N2O4) | 0.20 | a | 0.10 | c | d | e |
C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
(1)該反應的化學方程式為 , 表中bc(填“<”、“=”、“>”).
(2)20s時,N2O4的濃度為 mol/L,0~20s內N2O4的平均反應速率為 .
(3)該反應的平衡常數表達式K= , 在80℃時該反應的平衡常數K值為(保留2位小數).
(4)在其他條件相同時,該反應的K值越大,表明建立平衡時 .
A.N2O4的轉化率越高
B.NO2的產量越大
C.N2O4與NO2的濃度之比越大
D.正反應進行的程度越大.
【答案】
(1)N2O4?2NO2;>
(2)0.14;0.003mol/L?s
(3)![]() ;0.54
;0.54
(4)A,B,D
【解析】解:(1)將0.4mol的四氧化二氮氣體充入2L已抽空的固定容積的密閉容器中,反應的化學方程式為:N2O42NO2 , 隔一段時間對該容器內的物質進行分析,得到如下數據:反應進行至100s后將反應混合物的溫度降低,發現氣體的顏色變淺,說明反應逆向進行,逆向是放熱反應,正向是吸熱反應;依據化學平衡三段式列式計算分析判斷;進行到40S和進行到60S時;
N2O4 | 2NO2 | ||
起始量(mol) | 0.4 | 0 | |
變化量(mol) | 0.2 | 0.4 | |
40S末(mol) | 0.2 | 0.4 |
得到b=0.2mol/L;
進行到60S和進行到60S時;
N2O4 | 2NO2 | ||
起始量(mol) | 0.4 | 0 | |
變化量(mol) | 0.22 | 0.44 | |
40S末(mol) | 0.18 | 0.44 |
c=0.18 mol/L
計算比較得到,b>c;
故答案為:N2O42NO2;>;
(2.)進行到20S;
N2O4 | 2NO2 | ||
起始量(mol) | 0.4 | 0 | |
變化量(mol) | 0.12 | 0.24 | |
20S末(mol) | 0.28 | 0.24 |
20s時,N2O4的濃度= ![]() =0.14mol/L;
=0.14mol/L;
0~20s內N2O4的平均反應速率= ![]() =0.003mol/Ls;
=0.003mol/Ls;
故答案為:0.14;0.003mol/Ls;
(3)N2O42NO2 , 平衡常數K= ![]() ;
;
80°C平衡狀態和60S是相同平衡狀態,平衡濃度c(NO2)=0.22mol/L,c(N2O4)=0.09mol/L;
平衡常數K= ![]() =
= ![]() =0.54mol/L;
=0.54mol/L;
故答案為: ![]() ;0.54;
;0.54;
(4)反應進行至100s后將反應混合物的溫度降低,發現氣體的顏色變淺,說明反應逆向進行,逆向是放熱反應,正向是吸熱反應;該反應的K值越大,說明平衡正向進行,是溫度降低的原因;
A、平衡正向進行N2O4的轉化率越高,故A正確;
B、平衡正向進行NO2的產量越大,故B正確;
C、依據上述計算分析平衡正向進行,N2O4與NO2的濃度之比越小,故C錯誤;
D、該反應的K值越大,說明平衡正向進行,正反應進行的程度越大,故D正確;
故答案為:ABD.
(1)依據反應條件分析判斷,結合化學平衡的三段式列式計算分析比較;(2)化學平衡的三段式列式計算,結合化學反應速率概念計算0~20s內N2O4的平均反應速率;(3)依據化學方程式和平衡常數概念寫出平衡常數表達式,依據80°C平衡狀態下結合三段式列式計算平衡濃度計算平衡常數.


 新課標同步訓練系列答案
新課標同步訓練系列答案 一線名師口算應用題天天練一本全系列答案
一線名師口算應用題天天練一本全系列答案科目:高中化學 來源: 題型:
【題目】某研究性學習小組欲探究原電池的形成條件,按如圖所示裝置進行實驗并得到下表實驗結果:
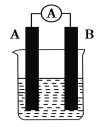
實驗序號 | A | B | 燒杯中的液體 | 靈敏電流表指針是否偏轉 |
1 | Zn | Zn | 乙醇 | 無 |
2 | Zn | Cu | 稀硫酸 | 有 |
3 | Zn | Cu | 稀硫酸 | 無 |
4 | Zn | Cu | 苯 | 無 |
5 | Cu | C | 氯化鈉溶液 | 有 |
6 | Mg | Al | 氫氧化鈉溶液 | 有 |
分析上述實驗,回答下列問題:
(1)實驗2中電流由________極流向________極(填“A”或“B”)。
(2)實驗6中電子由B極流向A極,表明負極是________(填“鎂”或“鋁”)電極。
(3)實驗5表明________(填字母序號,下同)。
A.銅在潮濕空氣中不會被腐蝕
B.銅的腐蝕是自發進行的
(4)分析上表有關信息,下列說法不正確的是________。
A.金屬活動順序表中,活潑性強的金屬一定作負極
B.失去電子的電極是負極
C.燒杯中的液體必須是電解質溶液
D.原電池中,浸入同一電解質溶液中的兩個電極,是活潑性不同的兩種金屬(或其中一種非金屬)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溶液、膠體這兩種分散系的根本區別是( )
A. 是否有丁達爾現象 B. 分散質微粒直徑的大小
C. 能否透過濾紙或半透膜 D. 是否均一、穩定、透明
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在80 ℃時,將0.40 mol的N2O4氣體充入2 L已經抽空的固定容積的密閉容器中,發生如下反應:N2O4![]() 2NO2 ΔH>0,隔一段時間對該容器內的物質進行分析,得到如下數據:
2NO2 ΔH>0,隔一段時間對該容器內的物質進行分析,得到如下數據:
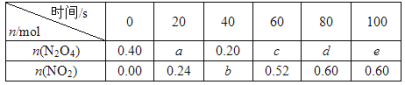
(1)計算20~40 s內用N2O4表示的平均反應速率為_________mol/( L s)。
(2)計算在80℃時該反應的平衡常數K=__________(請注明單位)。
(3)反應進行至100 s后將反應混合物的溫度降低,混合氣體的顏色______(填“變淺”“變深”或“不變”)。
(4)要增大該反應的K值,可采取的措施有_________(填序號)。
A.增大N2O4的起始濃度
B.向混合氣體中通入NO2
C.使用高效催化劑
D.升高溫度
(5)如圖是80℃時容器中N2O4物質的量的變化曲線,請在該圖中補畫出該反應在60℃時N2O4物質的量的變化曲線。
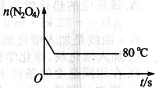
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知Ksp(AgCl)=1.8×10﹣10 , Ksp(AgI)=1.0×10﹣16 . 下列說法錯誤的是( )
A.AgCl不溶于水,不能轉化為AgI
B.在含有濃度均為0.001 mol?L﹣1的Cl﹣、I﹣的溶液中緩慢加入AgNO3稀溶液,首先析出AgI沉淀
C.AgI比AgCl更難溶于水,所以,AgCl可以轉化為AgI
D.常溫下,AgCl若要在NaI溶液中開始轉化為AgI,則NaI的濃度必須不低于 ![]() ×10﹣11mol?L﹣1
×10﹣11mol?L﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知下列兩個反應:
①Fe+H2SO4(稀)===FeSO4+H2↑
②Cu+2H2SO4(濃)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
試回答下列問題:
(1)反應①中________(填元素符號)被氧化,還原產物為________;反應②中________作還原劑,________元素被還原。
(2)當反應①生成2 g H2時,消耗H2SO4的質量是________ g。
(3)反應②中生成32 g SO2氣體時,消耗H2SO4的質量是________ g,其中有________ g H2SO4被還原,轉移電子________ mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列顏色變化與氧化還原反應無關的是( )
A.長期放置的苯酚晶體變紅B.硝酸銀晶體光照后變黑
C.氫氧化亞鐵變灰綠再變紅褐D.二氧化氮氣體冷卻后變淡
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)請配平下列化學方程式。
![]() _____________
_____________
(2)反應物中被氧化的元素_________,還原產物是________。
(3)反應中每生成標況下22.4L ![]() ,轉移_______mol電子。
,轉移_______mol電子。
(4)反應中氧化劑與還原劑物質的量之比____________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com