
分析 (1)6.02×1023個粒子的物質的量為1mol,說明RO4-所帶電荷的物質的量為1mol,則其物質的量為1mol,據此可計算出RO42-的摩爾質量,再結合氧元素的摩爾質量計算出R的摩爾質量;
(2)設A的摩爾質量為M,依據n=$\frac{m}{M}$計算氣體的物質的量,依據同溫同壓下,氣體的體積之比等于物質的量之比計算解答;
(3)根據n=$\frac{V}{{V}_{m}}$=V$\frac{m}{M}$,先由體積計算混合氣體的物質的量,結合二者的質量和摩爾質量、物質的量關系計算各自物質的量,進而可計算各種氣體的質量、體積;
(4)無論NO和氧氣是否完全反應,即無論容器中存在的微粒是什么,但密閉容器中各種元素原子個數不變,據此計算出反應后容器中氮原子和氧原子的個數之比.
解答 解:(1)6.02×1023個粒子的物質的量為1mol,說明RO4-所帶電荷的物質的量為1mol,則其物質的量為1mol,RO42-的摩爾質量為:$\frac{99.5g}{1mol}$=99.5g/mol,則R的摩爾質量為:99.5g/mol-16g/mol×4=35.5g/mol,
故答案為:35.5g/mol;
(2)設A的摩爾質量為M,則2gA氣體的物質的量n=$\frac{2}{M}$,二氧化碳的物質的量n′=$\frac{2}{44}$,同溫同壓下,氣體的體積之比等于物質的量之比,所以MM$\frac{2}{44}$:$\frac{2}{M}$=120:165,解得M=32(g/mol),故答案為:32g/mol;
(3)設CO2、CO的物質的量分別為x、y,
則$\left\{\begin{array}{l}{x+y=\frac{11.2L}{22.4L/mol}}\\{44g/molx+28g/moly=18g}\end{array}\right.$,
x=0.25mol,y=0.25mol,
m(CO2)=0.25mol×44g/mol=11g,V(CO)=0.25mol×22.4L/mol=5.6L,
故答案為:11g;5.6L;
(4)無論NO和氧氣是否完全反應,即無論容器中存在的微粒是什么,但密閉容器中各種元素原子個數不變,
根據N=nNA知,各種元素的原子個數之比等于其物質的量之比,n(N):n(O)=n(NO):[n(NO)+2n(O2)]=amol:(a+2b)mol=a:(a+2b),
故答案為:a:(a+2b).
點評 本題考查物質的量的相關計算,題目難度不大,明確“各種元素原子個數與是否發生反應無關”是解本題關鍵,根據原子守恒解答即可,試題培養了學生的化學計算能力.


科目:高中化學 來源: 題型:選擇題
| 選項 | 不純物質(雜質) | 除雜試劑或分離方法 | 必用儀器 |
| A | 碘水 | 酒精、萃取 | 分液漏斗 |
| B | 二氧化碳(一氧化碳) | 點燃 | |
| C | 硝酸鉀(氯化鈉) | 直接蒸發結晶 | 蒸發皿 |
| D | 乙醇(水) | 生石灰、蒸餾 | 蒸餾燒瓶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
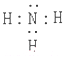 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化合反應 | B. | 分解反應 | C. | 置換反應 | D. | 復分解反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
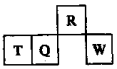 短周期元素R、T、Q、W在元素周期表中的相對位置如圖所示,其中W所處的周期序數是最外層電子數的一半.下列判斷不正確的是( )
短周期元素R、T、Q、W在元素周期表中的相對位置如圖所示,其中W所處的周期序數是最外層電子數的一半.下列判斷不正確的是( )| A. | 最簡單氣態氫化物的熱穩定性:R>Q | |
| B. | 最高價氧化物對應水化物的酸性:Q<W | |
| C. | 含T的鹽溶液一定顯酸性 | |
| D. | 實驗室制備T的氫氧化物可以通過R形成的氫化物通入到T離子的溶液中得到 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 某試樣焰色反應呈黃色,則該試樣一定是鈉的化合物 | |
| B. | 在石油蒸餾裝置中,將溫度計水銀球插入液面以下 | |
| C. | 在雞蛋白溶液中加入濃的Na2SO4溶液,可使蛋白質變性 | |
| D. | 用結晶的方法分離氯化鈉和硝酸鉀的混合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
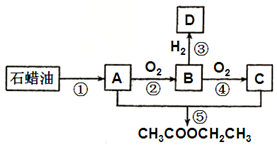 烴A是一種重要的化工原料.已知A在標準狀況下的密度為1.25g•L-1,B可發生銀鏡反應.它們之間的轉化關系如圖:
烴A是一種重要的化工原料.已知A在標準狀況下的密度為1.25g•L-1,B可發生銀鏡反應.它們之間的轉化關系如圖:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 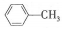 的一溴代物和 的一溴代物和 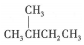 的一溴代物都有4種(不考慮立體異構) 的一溴代物都有4種(不考慮立體異構) | |
| B. | CH3CH=CHCH3分子中的四個碳原子在同一直線上 | |
| C. | 按系統命名法,化合物 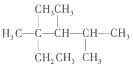 的名稱是2,3,4-三甲基-2-乙基戊烷 的名稱是2,3,4-三甲基-2-乙基戊烷 | |
| D. | 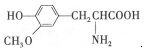 與 與 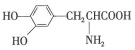 都是α-氨基酸且互為同系物 都是α-氨基酸且互為同系物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 28g N2含有的原子數為NA | |
| B. | 4gCa變成Ca2+失去的電子數為0.1NA | |
| C. | 1molO2的質量等于1mol O的質量 | |
| D. | 24gO2和24gO3所含有的原子數目相等 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com