
【題目】如何除去氯化亞鐵中的氯化鐵,寫出其化學方程式 ,其反應的離子方程式是 .
科目:高中化學 來源: 題型:
【題目】我國市售加碘食鹽中含有碘酸鉀。已知碘酸鉀在酸性條件下是一種較強的氧化劑,可與碘化物、亞硫酸鹽等還原性物質反應。工業生產碘酸鉀的流程如下:
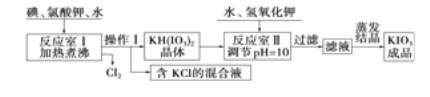
請回答下列問題:
(1)已知反應室Ⅰ發生的反應中,兩種還原產物所得電子數相同,請寫出該反應的化學方程式: 。
(2)反應室Ⅰ需加熱煮沸,其目的是:①加快反應速率,使反應物充分反應:② (請從化學平衡角度解釋)。
(3)已知幾種物質的溶解度見下表:
KCl | KH(IO3)2 | KClO3 | |
溶解度g/100 g水(25 ℃) | 20.8 | 0.8 | 7.5 |
溶解度g/100 g水(80 ℃) | 37.1 | 12.4 | 16.2 |
由上表數據分析可知,操作Ⅰ的名稱為 、 。
(4)在反應室Ⅱ中加入KOH調節溶液的pH=10,其目的是 。
(5)甲同學欲測定成品中碘酸鉀的含量,設計了如下實驗:
①準確稱取1 g樣品,加適量蒸餾水使其完全溶解;
②用稀硫酸酸化上述所得溶液,加入過量KI溶液,充分攪拌;
③以淀粉為指示劑,逐滴加入2.0 mol·L-1的Na2S2O3溶液,當藍色剛好褪去時,消耗Na2S2O3溶液12.00 mL,則成品中KIO3的質量分數為 (列式計算,結果保留三位有效數字)
(已知:KIO3+5KI+3H2SO4===3K2SO4+3I2+3H2O,I2+2Na2S2O3===2NaI+Na2S4O6)。
(6)乙同學又對純凈的NaCl(不含KIO3)進行了下列實驗:
操作步驟 | 實驗現象 |
取1g純凈的NaCl,加3mL水配成溶液。 | 溶液無變化 |
滴入5滴淀粉溶液和1mL 0.1mol/L KI溶液,振蕩。 | 溶液無變化 |
然后再滴入1滴1mol/L的H2SO4,振蕩。 | 溶液變藍色 |
①請推測實驗中產生藍色現象的可能原因,用離子方程式表示 。
②根據乙同學的實驗結果推測,甲同學的實驗結果會 (填“偏大”,“偏小”或“無影響”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氨、硫、氯及其化合物對環境有著重要的影響,在化工生產和日常生活中的用途也十分廣泛,如用做漂白劑、沉淀劑、農藥、化肥等。
(1)以N2 和H2 為原料合成氫氣為: N2(g) + 3 H2(g) ![]() 2NH3(g) △H=Q kJmol—1。已知鍵鍵能為946 kJmol—1 ,H-H鍵鍵能為436kJ mol—1,N-H鍵鍵能為391kJ mol—1,則Q=_______。
2NH3(g) △H=Q kJmol—1。已知鍵鍵能為946 kJmol—1 ,H-H鍵鍵能為436kJ mol—1,N-H鍵鍵能為391kJ mol—1,則Q=_______。
(2)將體積均為560 mL(標準狀況下)的SO2 和Cl2 同時緩慢通A水中,得到1.0 L溶液,則溶液pH=_______。
(3)物質的量濃度相等的NH4HSO3溶液和NaHSO3 溶液中,陰離子的電離程度較小的是__________(填化學式),原因是___________ 。
(4)用惰性電極電解NaHSO3 溶液的裝置如圖所示,則I是___________(填化學式,下同),陽極區放出的混合氣體的成分為___________。
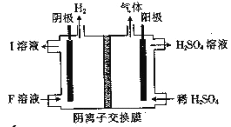
(5)氨水是一種常見的沉淀劑。向1.0 L 2.0×10—4molL—1的MgCl2 溶液中通入(不考慮溶液體積的變化),有白色沉淀生成。
①寫出生成白色沉淀的離子方程式____________________.
②當反應中開始有白色沉淀出現時,通人的體積(標準狀況)為___________mL。
(已知實驗條件下NH3.H2O的電離平衡常數為1.8×l0—5,Ksp=[Mg(OH)2]=1.8×l0—11)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】

(1)A中固體試劑是 ;B中所盛溶液溶質是 ;C中所盛溶液溶質是 (填字母)
a.醋酸鈉 b.碳酸氫鈉 c.苯酚鈉 d.碳酸鈉
(2)寫出C中反應的離子方程式是: ;
(3)有同學認為沒有B裝置,也可以驗證酸性的強弱,你認為這種說法合理嗎?說出你的理由: 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學小組用右圖所示裝置驗證鹵素單質氧化性的相對強弱。下列說法不正確的是( )
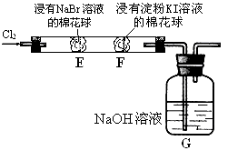
A.E處棉花球變成黃色,說明Cl2的氧化性比Br2強
B.F處棉花球變成藍色,說明Br2的氧化性比I2強
C.E處發生反應的離子方程式為:Cl2+ 2Br-=2Cl-+ Br2
D.G裝置中NaOH溶液與Cl2反應的離子方程式為:2OH- + Cl2 = ClO-+ Cl-+ H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NH3是一種重要的化工原料,也是造成水體富營養化及氮氧化物污染的重要因素之一。
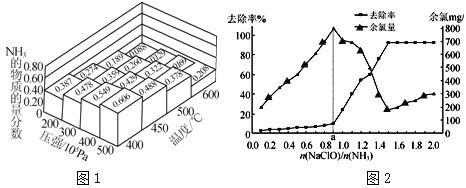
(1)N2和H2以物質的量之比為1∶3在不同溫度和壓強下發生反應:N2+3H2![]() 2NH3,測得平衡體系中NH3的物質的量分數如圖1。
2NH3,測得平衡體系中NH3的物質的量分數如圖1。
①為提高原料氣的轉化率,工業上采取的合理措施有 (填字母)。
a. 采用常溫條件
b. 使用適當的催化劑
c. 將原料氣加壓
d. 將氨液化并不斷移出
②圖1中所示的平衡體系中NH3的物質的量分數為0.549和0.488時,該反應的平衡常數分別為K1、K2,則K1 K2。(填“>”“<”或“=”)
(2)氨氮是造成水體富營養化的重要因素之一,用次氯酸鈉水解生成的次氯酸將水中的氨氮(用NH3表示)轉化為氮氣除去,涉及的相關反應如下:
反應①:NH3+HClO===NH2Cl+H2O
反應②:NH2Cl+HClO===NHCl2+H2O
反應③:2NHCl2+H2O===N2+HClO+3HCl
已知在水溶液中NH2Cl較穩定,NHCl2不穩定易轉化為氮氣。在其他條件一定的情況下,改變![]() (即NaClO溶液的投入量),溶液中次氯酸鈉對氨氮去除率及余氯量 (溶液中+1價氯元素的含量)的影響如圖2所示。
(即NaClO溶液的投入量),溶液中次氯酸鈉對氨氮去除率及余氯量 (溶液中+1價氯元素的含量)的影響如圖2所示。
①反應中氨氮去除效果最佳的n(NaClO)/n(NH3)值約為 。
②a點之前氨氮去除率較低的原因為 。
(3)電解硝酸工業的尾氣NO可制備NH4NO3,其工作原理如圖3。
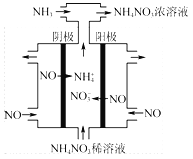
①電解過程(虛線內)發生反應的離子方程式為 。
②將電解生成的HNO3全部轉化為NH4NO3,則通入的NH3與實際參加反應的NO的物質的量之比至少為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列描述不涉及化學變化的是
A.鐵粉作袋裝食品的抗氧化劑 B.二氧化硫作紙漿的漂白劑
C.氫氟酸作普通玻璃的刻蝕劑 D.有機溶劑作食用油的萃取劑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫單質及其化合物在工農業生產中有著重要的應用。
(1)已知25℃時:SO2(g)+2CO(g)=2CO2(g)+1/x Sx(s) △H=akJ/mol
2COS(g)+SO2(g)=2CO2(g)+3/x Sx(s) △H=bkJ/mol。
則COS(g)生成CO(g)與Sx(s)反應的熱化學方程式是 。
(2)雌黃(As2S3)是提取砷的主要礦物原料。已知As2S3可以和濃HNO3反應,當生成0.6mol的H3AsO4時,反應中轉移電子的數目為3NA,則As2S3和濃HNO3反應的方程式是
(3)向等物質的量濃度Na2S、NaOH混合溶液中滴加稀鹽酸至過量。其中H2S、HS、S2的分布分數(平衡時某物種的濃度占各物種濃度之和的分數)與滴加鹽酸體積的關系如下圖所示(忽略滴加過程H2S氣體的逸出)。
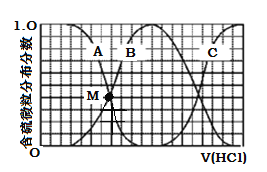
①曲線B表示 的分布分數。
②滴加過程中,溶液中微粒濃度大小關系正確的是 (填字母)。
A.c(Na+)= c(HS)+2c(S2)
B.3c(H2S)+2c(HS)+c(S2)+c(H+)=c(OH)
C.3c(Na+)=[c(H2S)+c(HS)+c(S2)]
③NaHS溶液呈堿性,當滴加鹽酸至M點(A、B曲線的交叉點)時,溶液中各離子濃度由大到小的順序為
(4)工業上用硫碘開路循環聯產氫氣和硫酸的工藝流程如下圖所示:
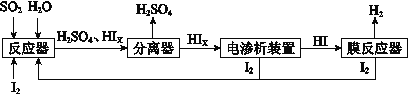
①寫出反應器中發生反應的化學方程式是 。
②電滲析裝置如下圖所示
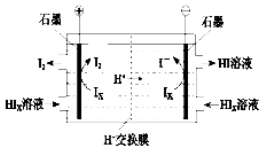
寫出陽極的電極反應式 。
該裝置中發生的總反應的化學方程式是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com