
【題目】苯和甲苯相比較,下列敘述中不正確的是( )
A. 都能使高錳酸鉀酸性溶液褪色B. 都屬于芳香烴
C. 都能在空氣中燃燒D. 都能發生取代反應
科目:高中化學 來源: 題型:
【題目】X、Y、Z、W均為短周期元素,在周期表中位置如圖,Y原子的最外層電子數是其次外層電子數的3倍。下列說法正確的是

A. X、Y、Z的原子半徑大小:X>Y>Z
B. Y、Z的氣態氫化物中,前者更穩定
C. Z、W的最高價氧化物對應水化物的酸性,前者更強
D. X、W的氣態氫化物相互反應,生成物中既含離子鍵又含共價鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】苯佐卡因是局部麻醉藥,常用于手術后創傷止痛、潰瘍痛等,其結構簡式為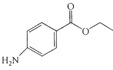 。下列關于苯佐卡因的敘述正確的是
。下列關于苯佐卡因的敘述正確的是
A. 分子式為C9H14NO2
B. 苯環上有2個取代基,且含有硝基的苯佐卡因的同分異構體有9種
C. 1mol該化合物最多與4mol氫氣發生加成反應
D. 分子中將氨基轉化成硝基的反應為氧化反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】空間實驗室“天宮一號”的供電系統中有再生氫氧燃料電池(RFC),RFC是一種將水電解技術與氫氧燃料電池技術相結合的可充電電池。下圖為RFC工作原理示意圖,有關說法正確的是
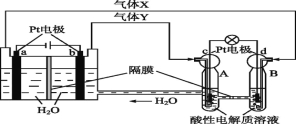
A.當有0.1 mol電子轉移時,a極產生1.12 L O2(標準狀況下)
B.b極上發生的電極反應是:4H2O+4e- =2H2↑+4OH-
C.c極上進行還原反應,B中的H+可以通過隔膜進入A
D.d極上發生的電極反應是:O2+4H++4e- =2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一氯甲烷(CH3Cl)是一種重要的化工原料,常溫下它是無色有毒氣體,微溶于水,易溶于乙醇、CCl4等。
(1)甲組同學在實驗室用下圖所示裝置模擬催化法制備和收集一氯甲烷。
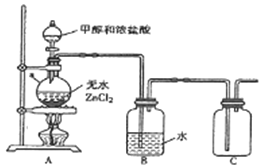
①儀器a的名稱為___________。
②無水ZnCl2為催化劑,a瓶中發生反應的化學方程式為_____________。
③裝置B的主要作用是_____________。
(2)乙組同學選用甲組A、B裝置和下圖所示的部分裝置檢驗CH3Cl中的氯元素。
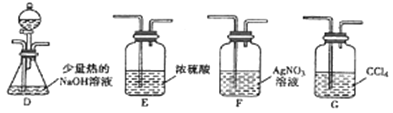
①乙組同學的實驗裝置中,依次連接的合理順序為A→B→_____→_____→_____。
②通入一段時間的CH3Cl氣體,打開裝置D中分液漏斗的活塞先后加入兩種試劑,觀察實驗現象。分液漏斗中先后加入的試劑是_______________。
③能證明CH3Cl中含有氯元素的實驗現象是____________。
(3)查閱資料可知:AgNO3的乙醇溶液可以檢驗CH3Cl中的鹵素原子。相關數據如下表:
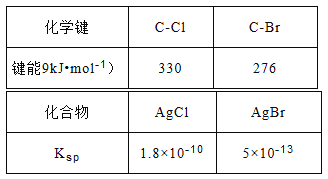
將CH3Cl和CH3Br的混合氣體通入AgNO3的乙醇溶液中,先出現淡黃色沉淀。請依據表中數據解釋原因__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與生活密切相關。下列說法不正確的是
A.過氧化鈉可用作潛水艇中的供氧劑 B.氧化鋁可用于制造耐火坩堝
C.明礬可用作自來水消毒劑 D.鐵粉作食品袋內的脫氧劑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、M、W為五種短周期元素,X、Y、Z是原子序數依次遞增的同周期元素,且最外層電子數之和為15,X與Z可形成XZ2分子;丫與M形成的氣態化合物在標準狀況下的密度為0.76g·L-1; W的質子數是X、Y、Z、M四種元素質子數之和的![]() ,下列說法正確的是
,下列說法正確的是
A. 原子半徑:W>Z>Y>X>M
B. YZ2溶于水形成的溶液具有較強的氧化性
C. 由X、Y、Z、M四種元素形成的化合物一定既有離子鍵,又有共價鍵
D. 1 molWM溶于足量水中完全反應共轉移2mol電子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期元素A、B、C、D,它們的原子序數依次增大。其中A、C與B、D分別是同主族元素。又知B、D兩元素的原子核中質子數之和是A、C兩元素原子核中質子數和的2倍。這四種元素的單質中有2種氣體,2種固體。
(1)寫出元素符號:A______;B______;
(2)寫出元素D在元素周期表中的位置______;
(3)寫出C元素的單質與B元素的單質在常溫下反應的化學方程式______;
(4)寫出兩種均含有A、B、C、D四種元素的化合物相互作用逸出氣體的離子方程式______;
(5)A、C組成的化合物,常作為野外考察的取氫(H2)劑。該化合物中加入適量的水,即可形成氫氣。寫出制氫化學方程式______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【化學-選修3:物質結構與性質】
南京理工大學化工學院胡炳成教授團隊于2017年1月成功合成世界首個全氮陰離子鹽,使氮原子簇化合物的研究又有了新的突破。請根據材料回答以下問題:
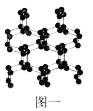
(1)N、O、F三種元素的第一電離能由大到小的順序為____(填元素符號);與N2互為等電子體的全氧離子化學式為_______;具有空間網狀結構的高聚氮結構如圖一所示,則N70的沸點_____(填“>”、“<”或“=”)高聚氮的沸點,原因是_________________;N70和高聚氮屬于_____(選填序號)。
A.同素異形體 B.同分異構體 C.同位素 D.同系物
(2)疊氮化物是研究較早的含全氮陰離子的化合物,如:氫疊氮酸(HN3)、疊氮化鈉(NaN3) 等。疊氮化物能形成多種配合物,在[Co(N3)(NH3)5]SO4,其中鈷顯____價,它的配體是____,SO42-的立體構型為___________。
(3)HN3是一種全氮陰離子酸,可由肼(N2H4)被HNO2氧化制得。下列說法正確的是____。
A.酸性:HNO2>HNO2
B. N2H4分子中N原子均采取sp3雜化
C. NaN3的晶格能小于KN3的晶格能
D.上述生成氫疊氮酸的化學方程式為N2H4+HNO2=2H2O+HN3
(4)N8是一種由全氮陽離子和全氮陰離子構成的特殊物質,已知陽離子由5個氮原子排列成V 形,每個氮原子均達到八電子穩定結構,則陽離子的電子式為_______。
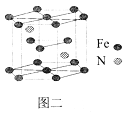
(5)一種氮鐵化合物的結構如圖二所示,若圖中六棱柱的體積為Vcm3, 用NA表示阿伏加德羅常數的值,則該晶體的密度為______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com