
【題目】阿巴卡韋(Abacavir)是一種核苷類逆轉錄酶抑制劑,存在抗病毒功效。關于其合成中間體M(![]() ),下列說法正確的是
),下列說法正確的是
A.與環戊醇互為同系物
B.分子中所有碳原子共平面
C.能使酸性高錳酸鉀溶液和溴水褪色,且原理相同
D.可用碳酸鈉溶液鑒別乙酸和M
 初中學業考試導與練系列答案
初中學業考試導與練系列答案科目:高中化學 來源: 題型:
【題目】汽車尾氣中NO產生的反應為:N2(g)+O2(g)![]() 2NO(g),一定條件下,等物質的量的N2(g)和O2(g)在恒容密閉容器中反應,下圖曲線a表示該反應在溫度T下N2的濃度隨時間的變化,曲線b表示該反應在某一起始反應條件改變時N2的濃度隨時間的變化。下列敘述正確的是:
2NO(g),一定條件下,等物質的量的N2(g)和O2(g)在恒容密閉容器中反應,下圖曲線a表示該反應在溫度T下N2的濃度隨時間的變化,曲線b表示該反應在某一起始反應條件改變時N2的濃度隨時間的變化。下列敘述正確的是:

A. 溫度T下,該反應的平衡常數K=![]()
B. 溫度T下,隨著反應的進行,混合氣體的密度減小
C. 曲線b對應的條件改變可能是加入了催化劑
D. 若曲線b對應的條件改變是溫度,可判斷該反應的△H<0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以鉻酸鉀為原料,電化學法制備重鉻酸鉀的實驗裝置示意圖如圖,下列說法不正確的是( )

A.在陰極室,發生的電極反應為:2H2O+2e-=2OH-+H2↑
B.在陽極室,通電后溶液逐漸由黃色變為橙色,是因為陽極區H+濃度增大,使平衡2CrO42-+2H+![]() Cr2O72-+H2O向右移動
Cr2O72-+H2O向右移動
C.該制備過程總反應的化學方程式為:4K2CrO4+4H2O![]() 2K2Cr2O7+4KOH+2H2↑+O2↑
2K2Cr2O7+4KOH+2H2↑+O2↑
D.測定陽極液中K和Cr的含量,若K與Cr的物質的量之比為d,則此時鉻酸鉀的轉化率為1-0.5d
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫代硫酸鈉(Na2S2O3·5H2O)俗稱“海波”,應用非常廣泛。工業上可以用亞硫酸鈉法(亞硫酸鈉和硫粉通過化合反應)制得,裝置如圖(a)所示。
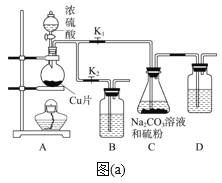
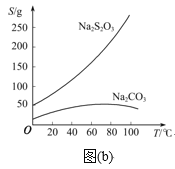
已知:Na2S2O3在酸性溶液中不能穩定存在,有關物質的溶解度曲線如圖(b)所示。
(1)Na2S2O3·5H2O的制備:
步驟1:如圖連接好裝置后,檢查A、C裝置氣密性的操作是_____。
步驟2:加入藥品,打開K1、關閉K2,向圓底燒瓶中加入足量濃硫酸并加熱。裝置B、D的作用是________。
步驟3:C中混合液被氣流攪動,反應一段時間后,硫粉的量逐漸減少。當C中溶液的pH接近7時,打開K2、關閉K1并停止加熱;C中溶液要控制pH的理由是_____。
步驟4:過濾C中的混合液,將濾液經過蒸發濃縮、冷卻結晶、過濾、洗滌、烘干,得到產品。
(2)Na2S2O3性質的檢驗:
向足量的新制氯水中滴加Na2S2O3溶液,氯水顏色變淺,再向溶液中滴加硝酸銀溶液,觀察到有白色沉淀產生,據此認為Na2S2O3具有還原性。該方案是否正確并說明理由:____。
(3)常用Na2S2O3溶液測定廢水中Ba2+濃度,步驟如下:取廢水25.00mL,控制適當的酸度加入足量K2Cr2O7溶液,得BaCrO4沉淀;過濾、洗滌后,用適量稀鹽酸溶解,此時CrO42-全部轉化為Cr2O72-;再加過量KI溶液,充分反應后,加入淀粉溶液作指示劑,用0.010mol·L-1的Na2S2O3溶液進行滴定,反應完全時,消耗Na2S2O3溶液18.00mL。部分反應的離子方程式為:a.Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O;b.I2+2S2O32-=2I-+S4O62-。則該廢水中Ba2+的物質的量濃度為_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某小組設計如圖實驗,欲使甲中試管先出現渾濁,下列操作一定達不到目的的是
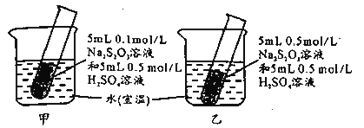
A.向甲燒杯中加入適量CaOB.向甲中試管內滴加適量濃硫酸
C.向乙燒杯中加入適量冰塊D.增大甲裝置所在環境的壓強
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,用0.1 mol·L1 KOH溶液滴定10 mL 0.1 mol·L1 HA(Ka=1.0×105)溶液的滴定曲線如圖所示。下列說法錯誤的是
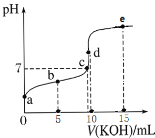
A.a點溶液的pH約為3
B.水的電離程度:d點>c點
C.b點溶液中粒子濃度大小:c(A-)>c(K+)>c(HA)>c(H+)>c(OH-)
D.e點溶液中:c(K+)=2c(A-)+2c(HA)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某硫酸廠產生的燒渣(主要含![]() 、
、![]() 及少量
及少量![]() )可用于制備
)可用于制備![]() 和還原鐵粉,其流程如圖:
和還原鐵粉,其流程如圖:

(1)“酸溶”前需粉碎燒渣,其目的是_________、________。
(2)“濾渣”的主要成分是_________(填化學式)。
(3)“還原”時,![]() 被氧化為
被氧化為![]() 的離子方程式是_________。
的離子方程式是_________。
(4)“焙燒”時,燒渣、無煙煤、![]() 的投料質量比為100∶40∶10,溫度控制在1000℃(溫度對焙燒爐氣含量的影響變化如圖所示):
的投料質量比為100∶40∶10,溫度控制在1000℃(溫度對焙燒爐氣含量的影響變化如圖所示):

添加![]() 的目的是:①脫除
的目的是:①脫除![]() 等;②_________。
等;②_________。
(5)“焙燒”在半封閉裝置中進行,投料層表面蓋有適當厚度的煤層,“焙燒”時間控制在4~4.5小時(焙燒時間對還原鐵粉產率的影響如圖所示),超過5小時后還原鐵粉產率降低的原因是_______。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】天門冬氨酸鋅是一種補鋅劑,可以用![]() 、天門冬氨酸為原料制備。
、天門冬氨酸為原料制備。
(1)![]() 基態核外電子排布式為_______。
基態核外電子排布式為_______。
(2)![]() 的空間構型為________(用文字描述);與
的空間構型為________(用文字描述);與![]() 互為等電子體的一種陽離子的化學式為________。
互為等電子體的一種陽離子的化學式為________。
(3)天門冬氨酸( )分子中氮原子的軌道雜化類型為________;天門冬氨酸_______(填“難溶”或“易溶”)于
)分子中氮原子的軌道雜化類型為________;天門冬氨酸_______(填“難溶”或“易溶”)于![]() 鹽酸。
鹽酸。
(4)ZnO的晶胞結構如圖所示,![]() 的配位數為________。
的配位數為________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度時,CuS、MnS在水中的沉淀溶解平衡曲線如圖所示,下列說法錯誤的是
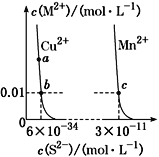
A. 在含有CuS和MnS固體的溶液中c(Cu2+)∶c(Mn2+)=1∶2×10-23
B. 向CuSO4溶液中加入MnS發生反應:
Cu2+(aq)+MnS(s)![]() CuS(s)+Mn2+(aq)
CuS(s)+Mn2+(aq)
C. a點對應的Ksp等于b點對應的Ksp
D. 該溫度下,Ksp(CuS)小于Ksp(MnS)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com