
 已知某種氣態化石燃料含有碳和氫兩種元素.為了測定這種燃料中碳和氫兩種元素的質量分數,可將氣態燃料放入足量的氧氣中燃燒,并使產生的氣體全部通入如圖所示的裝置,得到如表所列的實驗數據(U形管中干燥劑只吸收水蒸氣且假設產生的氣體完全被吸收).
已知某種氣態化石燃料含有碳和氫兩種元素.為了測定這種燃料中碳和氫兩種元素的質量分數,可將氣態燃料放入足量的氧氣中燃燒,并使產生的氣體全部通入如圖所示的裝置,得到如表所列的實驗數據(U形管中干燥劑只吸收水蒸氣且假設產生的氣體完全被吸收).| 實驗前 | 實驗后 | |
| (干燥劑+U形管)的質量 | 101.1g | 102.9g |
| (石灰水+廣口瓶)的質量 | 312.0g | 314.2g |
分析 (1)因為該燃料含C、H、O三種元素,故燃燒產物為CO2和H2O,由題意可知U形管增加的質量為吸收水的質量,廣口瓶增加的質量為生成的CO2質量,生成的正鹽為CaCO3,根據碳原子守恒計算CaCO3的物質的量,再根據m=nM計算CaCO3的質量;
(2)根據水的分子式中H元素質量分數計算;
(3)根據碳元素守恒、結合m=nM計算二氧化碳中C元素質;
(4)由元素守恒,結合(2)(3)中的數據計算.
解答 解:(1)因為該燃料含C、H、O三種元素,故燃燒產物為CO2和H2O,由題意可知U形管增加的質量為吸收水的質量:102.9g-101.1g=1.8g,
廣口瓶增加的質量為生成的CO2質量:314.2g-312.0g=2.2g,CO2的物質的量為:$\frac{2.2g}{44g/mol}$=0.05mol,廣口瓶中生成的正鹽為CaCO3,根據C原子守恒可知生成CaCO3 0.05mol,其質量為:0.05mol×100g/mol=5.0g,
故答案為:1.8;5.0;
(2)水中含H元素質量為:1.8×$\frac{2}{18}$=0.2g,
故答案為:0.2;
(3)生成的0.05mol CO2,含C元素質量為:0.05mol×12g/mol=0.6g,
故答案為:0.6;
(4)根據C、H元素守恒,該燃料中碳、氫元素的質量之比為:m(C):m(H)=0.6g:0.3g=3:1,
故答案為:3:1.
點評 本題考查探究物質組成、測量物質含量,題目難度中等,明確實驗前后各裝置中質量差的含義為解答關鍵,注意掌握質量守恒定律在化學計算中的應用方法,試題培養了學生的分析能力及化學計算能力.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
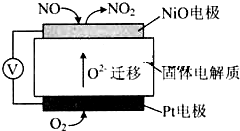 某市對大氣進行監測,發現該市首要污染物為可吸入顆粒物PM2.5(直徑小于等于2.5um的懸浮顆粒物)其主要來源為燃煤、機動車尾氣等.因此,對PM2.5、SO2、NOx等進行研究具有重要意義.請回答下列問題:
某市對大氣進行監測,發現該市首要污染物為可吸入顆粒物PM2.5(直徑小于等于2.5um的懸浮顆粒物)其主要來源為燃煤、機動車尾氣等.因此,對PM2.5、SO2、NOx等進行研究具有重要意義.請回答下列問題:| 離子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 濃度/mol.L | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
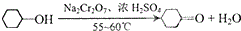 實驗室用Na2Cr2O7氧化環己醇制取環己酮(已知該反應為放熱反應):
實驗室用Na2Cr2O7氧化環己醇制取環己酮(已知該反應為放熱反應):| 物質 | 沸點( ) | 密度(g.cm-3,20) | 溶解性 |
| 環己醇 | 161.1(97.8) | 0.9624 | 能溶于水和乙醚 |
| 環己酮 | 155.6(95) | 0.9478 | 微溶于水,能溶于乙醚 |
| 水 | 100.0 | 0.9982 |
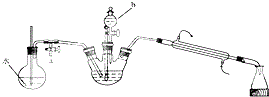
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 放電時負極反應為:Zn-2e-+2OH-=Zn(OH)2 | |
| B. | 放電時每轉移3mol電子,正極有1molK2FeO4被氧化 | |
| C. | 充電時陽極反應為:Fe(OH)3-3e-+5OH-=FeO42-+4H2O | |
| D. | 放電時正極附近溶液的堿性增強 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入5.6g 鐵粉充分反應后,溶液紅色褪去 | |
| B. | 加入40mL水充分振蕩后,靜置,溶液紅色變淺 | |
| C. | 加入10g Fe2(SO4)3固體充分反應后,溶液紅色明顯加深 | |
| D. | 加入20mL 0.001 mol/L KSCN溶液充分反應后,溶液紅色明顯變深 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
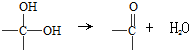
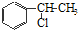 、
、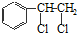 等都是A和Cl2發生反應生成的產物,E是一種發生加聚反應的聚合物物,透光性能好,常用作一些燈飾外殼.過程中一些小分子都已經略去
等都是A和Cl2發生反應生成的產物,E是一種發生加聚反應的聚合物物,透光性能好,常用作一些燈飾外殼.過程中一些小分子都已經略去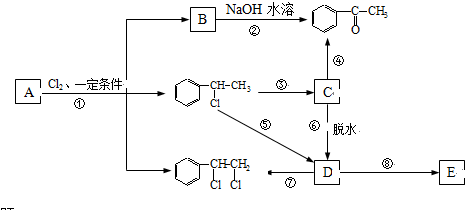
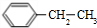 +2Cl2$\stackrel{光照}{→}$
+2Cl2$\stackrel{光照}{→}$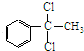 +2HCl,該反應類型為取代反應;
+2HCl,該反應類型為取代反應;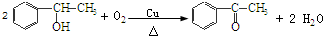 ,該反應類型為氧化反應;
,該反應類型為氧化反應;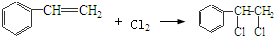 ,該反應類型為加成反應;
,該反應類型為加成反應;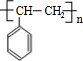 ;
;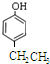 、
、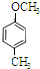 、
、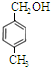 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
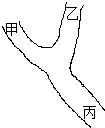 “Y”型河流上游有甲和乙兩家化工廠,它們生產時都向河流排放廢水.經檢測,兩家化工廠排出污水工有6種離子:①K+、②Ag+、③Fe3+、④Cl-、⑤OH-、⑥NO3-.某化學興趣小組在河流下游丙處做離子檢測實驗,你認為該處一定可以檢測到的離子是( )
“Y”型河流上游有甲和乙兩家化工廠,它們生產時都向河流排放廢水.經檢測,兩家化工廠排出污水工有6種離子:①K+、②Ag+、③Fe3+、④Cl-、⑤OH-、⑥NO3-.某化學興趣小組在河流下游丙處做離子檢測實驗,你認為該處一定可以檢測到的離子是( )| A. | ①和⑥ | B. | ①③⑥ | C. | ①③④⑥ | D. | ①②③④⑤⑥ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com