
| A. | 使甲基橙呈紅色的溶液中:Fe2+、Na+、ClO-、SO42- | |
| B. | 在PH=3的溶液中:Mg2+、Al3+、NO3-、Cl- | |
| C. | 由水電離出的c(H+)=10-13mol•L-1的溶液中:Na+、SO32-、AlO2-、Br- | |
| D. | 加入鋁粉后產生大量氫氣的溶液中:NH4+、K+、NO3-、MnO4- |
分析 A.使甲基橙呈紅色的溶液,顯酸性;
B.PH=3的溶液,顯酸性;
C.由水電離出的c(H+)=10-13mol•L-1的溶液,為酸或堿溶液;
D.加入鋁粉后產生大量氫氣的溶液,為非氧化性酸或強堿溶液.
解答 解:A.使甲基橙呈紅色的溶液,顯酸性,Fe2+、H+、ClO-發生氧化還原反應,不能共存,故A錯誤;
B.PH=3的溶液,顯酸性,該組離子之間不反應,可大量共存,故B正確;
C.由水電離出的c(H+)=10-13mol•L-1的溶液,為酸或堿溶液,酸溶液中不能大量存在SO32-、AlO2-,故C錯誤;
D.加入鋁粉后產生大量氫氣的溶液,為非氧化性酸或強堿溶液,堿溶液中不能大量存在NH4+,酸溶液中H+、NO3-、Al發生氧化還原反應不生成氫氣,故D錯誤;
故選B.
點評 本題考查離子的共存,為高頻考點,把握習題中的信息及常見離子之間的反應為解答的關鍵,側重復分解反應、氧化還原反應的離子共存考查,題目難度不大.


科目:高中化學 來源: 題型:填空題
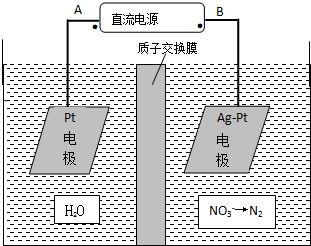 硝酸是一種重要的化工原料,工業上一般以氨氣為原料來制備硝酸.請回答:
硝酸是一種重要的化工原料,工業上一般以氨氣為原料來制備硝酸.請回答:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 A、B、C、D、E五種常見元素的核電荷數依次增大.A的基態原子中有2個未成對電子,B是地殼中含量最多的元素,C是短周期中最活潑的金屬元素,D與C可形成CD型離子化合物,E的基態3d軌道上有2個電子.請回答下列問題:
A、B、C、D、E五種常見元素的核電荷數依次增大.A的基態原子中有2個未成對電子,B是地殼中含量最多的元素,C是短周期中最活潑的金屬元素,D與C可形成CD型離子化合物,E的基態3d軌道上有2個電子.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 檢驗淀粉是否發生水解,將淀粉與稀硫酸溶液共熱,冷卻后,取上層水溶液,用NaOH中和稀硫酸后,再加入Cu(OH)2懸濁液,加熱,觀察是否產生磚紅色沉淀 | |
| B. | 檢驗Fe(NO3)2晶體是否已氧化變質,將Fe(NO3)2樣品溶于稀硫酸后,滴加KSCN溶液,觀察溶液是否變血紅色 | |
| C. | 在酸、堿中和滴定終點時不慎滴入過量標準溶液,可用裝有待測液的滴定管再滴入一定量溶液進行調整 | |
| D. | 實驗室制備氫氧化亞鐵,滴加氫氧化鈉溶液時應將膠頭滴管插入硫酸亞鐵溶液中 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
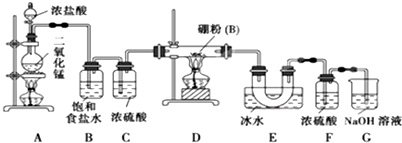
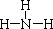 ,寫出甲與足量的氫氧化鈉溶液反應的化學方程式為AlN+NaOH+H2O=NaAlO2+NH3↑,驗證溶液丁中產物陰離子的實驗方法為取少量溶液丁于試管中,逐滴加入稀鹽酸,若先產生白色沉淀后消失,說明為NaAlO2.
,寫出甲與足量的氫氧化鈉溶液反應的化學方程式為AlN+NaOH+H2O=NaAlO2+NH3↑,驗證溶液丁中產物陰離子的實驗方法為取少量溶液丁于試管中,逐滴加入稀鹽酸,若先產生白色沉淀后消失,說明為NaAlO2.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 布洛芬具有解熱鎮痛作用,常規劑量使用時,不良反應發生率低,是國內外包括世界衛生組織公認的用于小兒發熱的經典解熱鎮痛藥.布洛芬的結構簡式如圖:
布洛芬具有解熱鎮痛作用,常規劑量使用時,不良反應發生率低,是國內外包括世界衛生組織公認的用于小兒發熱的經典解熱鎮痛藥.布洛芬的結構簡式如圖: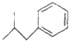 $→_{AlCl_{3}}^{CH_{3}COCl}$A$\stackrel{H_{2}}{→}$
$→_{AlCl_{3}}^{CH_{3}COCl}$A$\stackrel{H_{2}}{→}$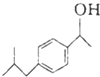 $\stackrel{CO}{→}$布洛芬
$\stackrel{CO}{→}$布洛芬 +
+ $\stackrel{AlCl_{3}}{→}$
$\stackrel{AlCl_{3}}{→}$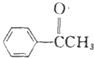 +HCl,請寫出A的結構簡式
+HCl,請寫出A的結構簡式

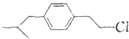 為原料合成布洛芬(用合成路線流程圖表示;無機原料任選,并注明反應條件).
為原料合成布洛芬(用合成路線流程圖表示;無機原料任選,并注明反應條件). .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 規律 | 結論 |
| A | 較強酸可以制取較弱酸 | H2S溶液無法制取H2SO4 |
| B | 反應物濃度越大,反應速率越快 | 常溫下,相同的鋁片中分別加入足量的濃、稀硝酸中,鐵絲在濃硫酸中先反應完 |
| C | 離子反應總是向著某種離子濃度減小的方向進行 | 反應2Na+2CH3COOH═2Na++2CH3COO-+H2↑不能進行 |
| D | 溶解度小的沉淀易向溶解度更小的沉淀轉化 | MgCO3沉淀在水中煮沸,最終轉化為Mg(OH)2沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com