
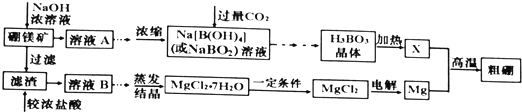
分析 I.硼鎂礦主要成分為Mg2B2O5•H2O,可以看做2MgO•B2O3•H2O,含有少量雜質A12O3和Fe3O4,用濃氫氧化鈉溶液溶解,B2O3、A12O3與氫氧化鈉反應得到NaBO2、NaAlO2,而MgO、Fe3O4不與氫氧化鈉反應,過濾得到濾渣為MgO、Fe3O4,濾液A中為NaBO2、NaAlO2及剩余的NaOH,濃縮后通入過量的二氧化碳,經過系列操作得到H3BO3,加熱得到B2O3,再與Mg發生置換反應反應得到B與MgO.
濾渣與過量的濃鹽酸反應得到溶液B中有MgCl2、FeCl3及未反應的HCl,加入氧化鎂等調節溶液pH,使溶液中鐵離子轉化為氫氧化鐵沉淀,再過濾除去,溶液進行蒸發結晶得到MgCl2•7H2O,在HCl氛圍下加熱分解得到MgCl2,以防止氯化鎂水解,再電解熔融的MgCl2得到金屬Mg及氯氣.(1)中溶液B中含有的鐵元素以Fe3+形式存在,用KSCN溶液進行檢驗;
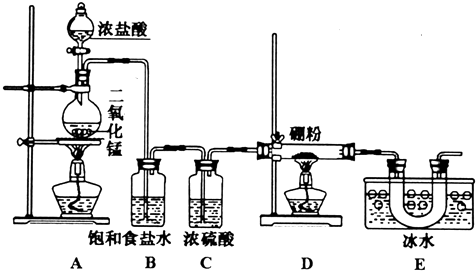
Ⅱ.BCl3在潮濕空氣中易形成白霧,遇水發生水解反應,應在無水環境下進行,裝置A制備氯氣,制備的氯氣中含有揮發出的HCl,由于B與HCl可以發生反應:2B+6HCl(g)$\frac{\underline{\;\;△\;\;}}{\;}$2BCl3+3H2↑,生成的氫氣與氯氣易發生爆炸,B裝置吸收HCl,C裝置由于干燥氯氣,D裝置中B與氯氣反應生成BCl3,由于BCl3的沸點較低,反應得到為氣態BCl3,E裝置利用冰水冷卻收集得到液體BCl3,由于未反應的氯氣會污染環境,需要在E裝置之后添加吸收氯氣裝置,同時防止空氣中的水蒸氣加入D中,防止BCl3發生水解.
解答 解:I.硼鎂礦主要成分為Mg2B2O5•H2O,可以看做2MgO•B2O3•H2O,含有少量雜質A12O3和Fe3O4,用濃氫氧化鈉溶液溶解,B2O3、A12O3與氫氧化鈉反應得到NaBO2、NaAlO2,而MgO、Fe3O4不與氫氧化鈉反應,過濾得到濾渣為MgO、Fe3O4,濾液A中為NaBO2、NaAlO2及剩余的NaOH,濃縮后通入過量的二氧化碳,經過系列操作得到H3BO3,加熱得到B2O3,再與Mg發生置換反應反應得到B與MgO.
濾渣與過量的濃鹽酸反應得到溶液B中有MgCl2、FeCl3及未反應的HCl,加入氧化鎂等調節溶液pH,使溶液中鐵離子轉化為氫氧化鐵沉淀,再過濾除去,溶液進行蒸發結晶得到MgCl2•7H2O,在HCl氛圍下加熱分解得到MgCl2,以防止氯化鎂水解,再電解熔融的MgCl2得到金屬Mg及氯氣.
(1)中溶液B中含有的鐵元素以Fe3+形式存在,用KSCN溶液進行檢驗,具體操作為:取少許溶液B于試管中,滴加幾滴KSCN溶液,溶液變紅色,說明含有Fe元素,
故答案為:取少許溶液B于試管中,滴加幾滴KSCN溶液,溶液變紅色,說明含有Fe元素;
(2)Mg與B2O3得到B與MgO,反應方程式為:3Mg+B2O3$\frac{\underline{\;高溫\;}}{\;}$2B+3MgO,
故答案為:3Mg+B2O3$\frac{\underline{\;高溫\;}}{\;}$2B+3MgO;
(3)MgCl2•7H2O在HCl氛圍下加熱分解得到MgCl2,以防止氯化鎂水解,
故答案為:HCl氛圍、加熱;
Ⅱ.BCl3在潮濕空氣中易形成白霧,遇水發生水解反應,應在無水環境下進行,裝置A制備氯氣,制備的氯氣中含有揮發出的HCl,由于B與HCl可以發生反應:2B+6HCl(g)$\frac{\underline{\;\;△\;\;}}{\;}$2BCl3+3H2↑,生成的氫氣與氯氣易發生爆炸,B裝置吸收HCl,C裝置由于干燥氯氣,D裝置中B與氯氣反應生成BCl3,由于BCl3的沸點較低,反應得到為氣態BCl3,E裝置利用冰水冷卻收集得到液體BCl3,由于未反應的氯氣會污染環境,需要在E裝置之后添加吸收氯氣裝置,同時防止空氣中的水蒸氣加入D中,防止BCl3發生水解.
(4)由上述分析可知,E裝置的作用是:冷卻并收集BCl3,故答案為:冷卻并收集BCl3;
(5)B裝置吸收HCl,若去掉B裝置,B與HCl可以發生反應:2B+6HCl(g)$\frac{\underline{\;\;△\;\;}}{\;}$2BCl3+3H2↑,生成的氫氣與氯氣易發生爆炸,
故答案為:加熱時B與HCl可以發生反應:2B+6HCl(g)$\frac{\underline{\;\;△\;\;}}{\;}$2BCl3+3H2↑,生成的氫氣與氯氣混合易發生爆炸,
故答案為:加熱時B與HCl反應生成的氫氣與氯氣混合易發生爆炸;
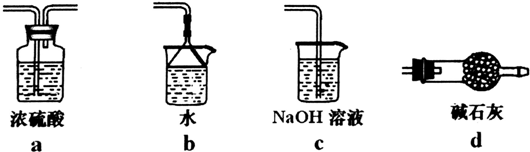
(6)由于未反應的氯氣會污染環境,BCl3遇水發生水解,故需要在E裝置之后添加吸收氯氣裝置,同時防止空氣中的水蒸氣加入D中,防止BCl3發生水解,
a中濃硫酸不能吸收剩余的氯氣,bc均含有水,水蒸氣可以進入E中,導致BCl3發生水解,d中堿石灰可以吸收氯氣與空氣中水蒸氣,故選:d.
點評 本題考查實驗制備方案,側重考查學生對裝置的分析評價、實驗條件的控制等,明確原理是解題關鍵,是對學生綜合能力的考查,注意對題目信息的提取與運用,難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:多選題

| A. | x為強酸,y為弱酸 | |
| B. | 隨著稀釋的進行,y的電離程度減小 | |
| C. | 稀釋前x、y的物質的量濃度相等 | |
| D. | 稀釋后的x、y分別分別與足量的鋅反應,y放出的氫氣多 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 如圖,在盛有稀 H2SO4 的燒杯中放入用導線連接的電極X、Y,外電路中電子流向如圖所示,關于該裝置的下列說法正確的是( )
如圖,在盛有稀 H2SO4 的燒杯中放入用導線連接的電極X、Y,外電路中電子流向如圖所示,關于該裝置的下列說法正確的是( )| A. | 外電路的電流方向為:X→外電路→Y | |
| B. | 若兩電極分別為 Fe 和碳棒,則 X 為碳棒,Y 為 Fe | |
| C. | X 極上發生的是還原反應,Y 極上發生的是氧化反應 | |
| D. | 若兩電極都是金屬,則它們的活動性順序為 X>Y |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 采用加熱蒸發溶劑的方法可以使濃度為4 mol/L的鹽酸溶液的濃度變為8 mol/L | |
| B. | 把100 g 20%的NaCl溶液跟100 g H2O混合后,NaCl溶液的質量分數是10% | |
| C. | 將2.3 g Na投入到97.7g水中充分反應,所得溶液的質量分數為4.0% | |
| D. | 已知某溫度下KNO3的溶解度是31.6 g,該溫度下將20 g KNO3溶解于50 g水中,充分溶解,獲得溶液的質量分數是28.6% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 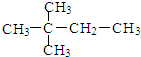 | B. |  | ||
| C. | CH3CH2CH2CH2CH3 | D. | 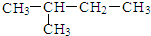 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
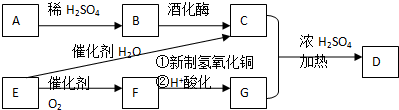
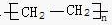 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 二氧化硫具有還原性 | |
| B. | 因為二氧化硫具有漂白性,能使品紅溶液永久褪色 | |
| C. | 大氣中二氧化碳濃度高時能形成酸雨 | |
| D. | 濃硫酸常用作干燥劑,因為濃硫酸具有脫水性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 混合物 | 分離、提純方法 |
| A. | 分離苯和水 | 分液法 |
| B. | 分離乙醇和甲醇 | 蒸餾法 |
| C. | 除去乙炔中H2S氣體 | 用CuSO4溶液洗氣 |
| D. | 除去水中的少量苯酚 | 過濾 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com