
【題目】四溴化鈦(TiBr4)可用作橡膠工業中烯烴聚合反應的催化劑,常溫下為橙黃色固體,熔點:38.3℃,沸點233.5℃,具有潮解性且易發生水解。實驗室利用反應TiO2 +C+ 2Br2 ![]() TiBr4+CO2來制備TiBr4,裝置如圖所示。下列說法錯誤的是
TiBr4+CO2來制備TiBr4,裝置如圖所示。下列說法錯誤的是
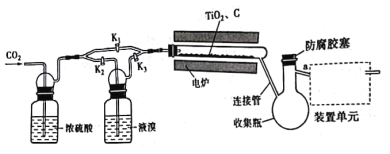
A.開始反應時,活塞的狀態為K1關閉,K2,K3打開
B.為防止連接管堵塞,反應過程中需微熱連接管
C.為達到實驗目的,a應連接盛有NaOH溶液的洗氣裝置
D.反應結束后繼續通入CO2排出裝置中殘留的四溴化鈦及溴蒸氣
 寒假天地重慶出版社系列答案
寒假天地重慶出版社系列答案科目:高中化學 來源: 題型:
【題目】高鐵酸鉀(K2FeO4)是一種環保、高效、多功能飲用水處理劑,制備流程如圖所示:
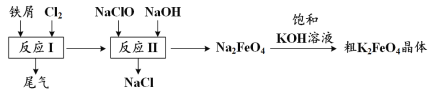
下列敘述不正確的是
A.用K2FeO4對飲用水殺菌消毒的同時,還產生Fe(OH)3膠體吸附雜質凈化水
B.用FeCl2溶液吸收反應I中尾氣后可再利用
C.反應II中氧化劑與還原劑的物質的量之比為3∶2
D.該生產條件下,物質的溶解性:Na2FeO4< K2FeO4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鉀(K)資源豐富,成本低廉,用其制作的鉀離子電池有著超越鋰離子電池的發展前景。我國科研人員在鉀離子電池的研發上做出了巨大的貢獻。如圖是我國某科研團隊研制的一種鉀離子電池充電時的示意圖,下列說法不正確的是( )

A.放電時,外電路電子由電極a流向電極b
B.鉀離子電池電解液一般選擇有機溶劑,但會有一定的安全隱患
C.充電時,每當外電路中轉移1mole-,正極材料會“釋放”39gK+
D.充電時,電極b上的電極反應式為:WS2+xK++xe-=KxWS2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于可逆反應 A(g)+3B(s)2C(g)+2D(g),在不同條件下的化學反應速率如下,其中表示的反應速率最快的是( )
A.v(A)=0.5mol·L-1·min-1B.v(B)=1.0 mol·L-1·min-1
C.v(D)=0.4 mol·L-1·min-1D.v(C)=0.1 mol·L-1·s-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】補鐵劑常用于防治缺鐵性貧血,其有效成分般為硫酸亞鐵、琥珀酸亞鐵、富馬酸亞鐵和乳酸亞鐵等。回答下列問題:
(1)能表示能量最低的亞鐵離子的電子排布式是__(填標號)。
a.[Ar]3d54s2 b.[Ar]3d54s1 c.[Ar]3d64s2 d.[Ar]3d6
(2)琥珀酸即丁二酸(HOOCCH2CH2COOH),在琥珀酸分子中電負性最大的原子是__,碳原子的雜化方式是__;琥珀酸亞鐵中存在配位鍵,在該配位鍵中配位原子是__,中心原子是__。
(3)富馬酸和馬來酸互為順反異構體,其電離常數如下表:
物質名稱 | Ka1 | Ka2 |
富馬酸( | 7.94×10-4 | 2.51×10-5 |
馬來酸( | 1.23×10-2 | 4.68×10-7 |
請從氫鍵的角度解釋富馬酸兩級電離常數差別較小,而馬來酸兩級電離常數差別較大的原因:__。
(4)β-硫酸亞鐵的晶胞結構如圖所示,其晶胞參數為a=870pm、b=680pm、c=479pm,α=β=γ=90°,Fe2+占據晶胞頂點、棱心、面心和體心。在該晶胞中,硫酸根離子在空間上有__種空間取向,晶胞體內硫酸根離子的個數是__,鐵原子周圍最近的氧原子的個數為__;設阿伏加德羅常數的值為NA,則該晶體的密度是__g·cm-3(列出計算表達式)。
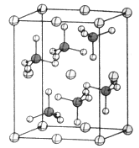
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種用電催化N2還原法制取NH3的反應機理如圖所示,其中*表示吸附在催化劑表面的物種。下列說法正確的是
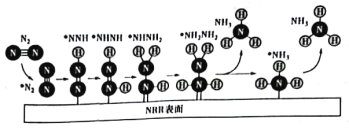
A.兩個氮原子上的加氫過程是分步進行的
B.析氫反應(H++ H+→H2)不會影響NH3的合成
C.NH3從催化劑表而脫附不利于NH3的合成
D.電催化法是一步即能把N2還原為NH3的高效還原法
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列化學用語使用正確的是:( )
A.硫原子的原子結構示意圖:![]()
B.NH3的電子式:![]()
C.原子核內有8個中子的氧原子:![]()
D.CO2的結構式:O—C—O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】冠心平F是降血脂、降膽固醇的藥物,它的一條合成路線如下,A為一元羧酸,10.2g A與足量NaHCO3溶液反應生成2.24L CO2(標準狀況),A的分子式為
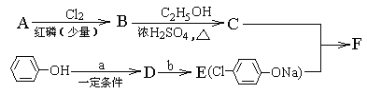
A. C2H4O2B. C3H6O2C. C4H8O2D. C5H10O2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】同分異構現象在有機物中廣泛存在,如圖為苯及其幾種同分異構體的鍵線式,下列有關說法中正確的是

A. b、c均與乙烯互為同系物
B. a和d的二氯代物均有3種
C. 4種有機物均能使酸性高錳酸鉀溶液褪色
D. a和b中所有原子可能共平面
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com