
【題目】常溫下,下列敘述正確的是( )
A.pH=a的氨水,稀釋10倍后,其pH=b,則a<b+1
B.在滴有酚酞溶液的氨水中,加入NH4Cl溶液恰好無色,則此時溶液的pH<7
C.向10mL0.1mol·L-1的CH3COOH溶液中滴加相同濃度的氨水,在滴加過程中,![]() 將減小
將減小
D.向10mLpH=11的氨水中加入10mLpH=3的H2SO4溶液,混合液pH=7
【答案】AC
【解析】
A.pH=a的強堿溶液稀釋10n倍,溶液的新pH=a-n(pH﹥7),一水合氨為弱堿,加水稀釋促進其電離,相比強堿而言,稀釋過程還產生一定的OH-,稀釋后溶液堿性比相同情況下的強堿強,則![]() 的氨水稀釋101倍后,其新pH﹥a-1,即b﹥a-1,則
的氨水稀釋101倍后,其新pH﹥a-1,即b﹥a-1,則![]() ,A正確;
,A正確;
B.酚酞的變色范圍為![]() ,所以在滴有酚酞試液的氨水中,加入稀鹽酸至溶液恰好無色,此時溶液的pH﹤8.2,B錯誤;
,所以在滴有酚酞試液的氨水中,加入稀鹽酸至溶液恰好無色,此時溶液的pH﹤8.2,B錯誤;
C.一水合氨的電離平衡Kb=![]() ,溫度不變則Kb不變,
,溫度不變則Kb不變,![]() 不變,向
不變,向![]() 溶液中滴加少量氨水,但是c(OH-)增大,所以
溶液中滴加少量氨水,但是c(OH-)增大,所以![]() 減小,C正確;
減小,C正確;
D.向![]() 的氨水中加入
的氨水中加入![]() 的
的![]() 溶液,由于一水合氨為弱堿,反應過程還會產生大量OH-,故混合液呈堿性,則混合液的
溶液,由于一水合氨為弱堿,反應過程還會產生大量OH-,故混合液呈堿性,則混合液的![]() ,D錯誤。
,D錯誤。
答案選AC。


科目:高中化學 來源: 題型:
【題目】X、Y、Z三種有機物互為同系物,下列有關說法錯誤的是( )
A.若X為![]() ,則Y不可能是
,則Y不可能是![]()
B.若X是甲醇、Y是乙醇,則Z一定能發生消去反應
C.若X為苯,Y為甲苯,則Z的相對分子質量一定不低于106
D.若X、Y均是飽和一元醛,則Z的分子式一定不是![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某廠以甘蔗為原料制糖,對產生的大量甘蔗渣按如圖所示轉化進行綜合利用(部分反應條件及產物沒有列出)。
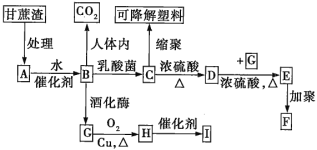
其中B是A水解的最終產物;C的分子式為C3H6O3,一定條件下2個C分子分子間脫去2分子水可生成一種六元環狀化合物;D可使溴水褪色;H的三聚物I也是一種六元環狀化合物。
提示:葡萄糖在乳酸菌作用下生成乳酸(![]() )。
)。
(1)C→D的反應類型為__,D→E的反應類型為__。
(2)寫出A→B反應的化學方程式:_。
(3)H分子中所含官能團的名稱是__,實驗室中常用于檢驗該官能團的試劑的名稱是_(只寫一種)。
(4)寫出下列物質的結構簡式:高分子化合物F__;六元環狀化合物I_。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】觀察如圖所示裝置,可發現電流計指針偏轉,M棒變粗,N棒變細.下表所列的M、N、P對應物質可構成該裝置的是( )
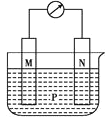
選項 | M | N | P |
A | 鋅 | 銅 | 稀硫酸 |
B | 銅 | 鐵 | 稀鹽酸 |
C | 銀 | 鋅 | 硝酸銀溶液 |
D | 鋅 | 鐵 | 硝酸鐵溶液 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:①2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1
②2H2(g)+O2(g)=2H2O(g) ΔH=-484kJ·mol-1
③CH4(g)+2O2(g)=2H2O(l)+CO2(g) ΔH=-890kJ·mol-1
(1)已知H—H鍵的鍵能為436kJ·mol-1,O=O鍵的鍵能為496kJ·mol-1,H—O鍵的鍵能為463kJ·mol-1,根據上述數據通過鍵能可直接計算出反應___(填反應序號)的焓變,由反應①②可得出反應比H2O(l)=H2O(g)的焓變ΔH=___。
(2)根據題干可計算出CO2(g)+4H2(g)=CH4(g)+2H2O(g)的焓變ΔH=___。
(3)在①②③三個熱化學方程式中,可表示燃燒熱的熱化學方程式的是___(填序號)。標準狀況下,取甲烷和氫氣的混合氣體11.2L,完全燃燒后恢復到常溫,放出的熱量為263.8kJ,則混合氣體中甲烷和氫氣的體積比為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知某油脂A,在稀硫酸作催化劑的條件下水解,生成脂肪酸和多元醇B,B和硝酸在濃硫酸作用下通過酯化反應生成有機物D。
(1)寫出油脂A在稀硫酸作催化劑的條件下水解的化學方程式:__。
(2)已知D由C、H、O、N四種元素組成,相對分子質量為227,C、H、N的質量分數分別為15.86%、2.20%和18.50%,則D的分子式是__,B→D的化學方程式是__。
(3)C是B和乙酸在一定條件下反應生成的化合物,相對分子質量為134,寫出C所有可能的結構簡式:__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知下列數據:
物質 | 熔點/℃ | 沸點/℃ | 密度/ |
乙醇 |
| 78.3 | 0.79 |
乙酸 | 16.6 | 117.9 | 1.05 |
乙酸乙酯 |
| 77 | 0.90 |
某學生在實驗室制取乙酸乙酯的主要步驟如下:
①配制![]() 濃硫酸、
濃硫酸、![]() 乙醇(含
乙醇(含![]() )和
)和![]() 乙酸的混合溶液。
乙酸的混合溶液。
②按如圖連接好裝置(裝置氣密性良好)并加入混合液,用小火均勻加熱![]() 。
。
③待試管乙收集到一定量產物后停止加熱,撤出試管乙并用力振蕩,然后靜置待分層。
④分離出乙酸乙酯,洗滌、干燥。
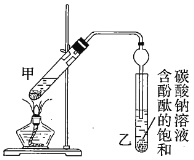
(1)配制①中混合溶液的方法為_______________________________;反應中濃硫酸的作用是____________________________;寫出制取乙酸乙酯的反應的化學方程式:____________________________(標出![]() )。
)。
(2)上述實驗中飽和碳酸鈉溶液的作用是________(填字母)。
A.中和乙酸和乙醇 B.中和乙酸并吸收乙醇
C.減少乙酸乙酯的溶解 D.加速酯的生成,提高其產率
(3)步驟②中需要小火均勻加熱,其主要原因是____________________________;步驟③所觀察到的現象是_______________________________________;欲將乙試管中的物質分離以得到乙酸乙酯,必須使用的儀器有___________;分離時,乙酸乙酯應從儀器_____________(填“下口放”或“上口倒”)出。
(4)該同學反復實驗,得出乙醇與乙酸的用量和得到的乙酸乙酯生成量如下表:
實驗 | 乙醇/ | 乙酸/ | 乙酸乙酯/ |
① | 2 | 2 | 1.33 |
② | 3 | 2 | 1.57 |
③ | 4 | 2 | x |
④ | 5 | 2 | 1.76 |
⑤ | 2 | 3 | 1.55 |
表中數據x的范圍是__________________;實驗①②⑤探究的是_____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質的性質比較,結論錯誤的是
A.硬度:金剛石>碳化硅>晶體硅
B.離子半徑:S2->Cl->Na+>O2-
C.熔點:NaF>NaCl>NaBr>NaI
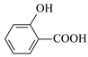
D.沸點:![]() >
>
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com