
分析 在25℃下,平衡時溶液中c(NH4+)=c(Cl-)=0.005mol/L,根據物料守恒得c(NH3•H2O)=(0.5a-0.005)mol/L,根據電荷守恒得c(H+)=c(OH-)=10-7mol/L,溶液呈中性,NH3•H2O的電離常數Kb=$\frac{c(O{H}^{-})c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$.
解答 解:反應平衡時溶液中c(NH4+)=c(Cl-),則溶質為NH4Cl 和NH3•H2O;
平衡時溶液中c(NH4+)=c(Cl-)=0.005mol/L,根據物料守恒得c(NH3•H2O)=(0.5a-0.005)mol/L,根據電荷守恒得c(H+)=c(OH-)=10-7mol/L,溶液呈中性,NH3•H2O的電離常數Kb=$\frac{c(O{H}^{-})c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$=$\frac{1{0}^{-7}×0.005}{0.5aa-0.005}$=$\frac{1{0}^{-9}}{a-0.01}$,
故答案為:NH4Cl 和NH3•H2O;$\frac{1{0}^{-9}}{a-0.01}$.
點評 本題考查了離子濃度大小比較、電離平衡常數計算,題目難度中等,明確溶液酸堿性,注意掌握電荷守恒、物料守恒的含義及應用方法,試題培養了學生的分析能力及靈活應用能力.


科目:高中化學 來源: 題型:選擇題
| A. | 手持試管給試管里的物質加熱 | |
| B. | 用天平稱量藥品時,用手直接取放砝碼 | |
| C. | 用pH試紙測定溶液的酸堿性時,一定要先把試紙用蒸餾水潤濕一下 | |
| D. | 兩端有大、小兩匙的藥匙,取用很少量的氧化銅粉末時應用小匙 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1:1:1 | B. | 1:2:7 | C. | 4:2:7 | D. | 2:4:7 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
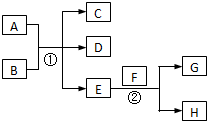 已知常溫下E為無色無味的液體,F為淡黃色粉末,G為常見的無色氣體(反應條件均已略去),請回答下列問題:
已知常溫下E為無色無味的液體,F為淡黃色粉末,G為常見的無色氣體(反應條件均已略去),請回答下列問題: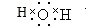 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
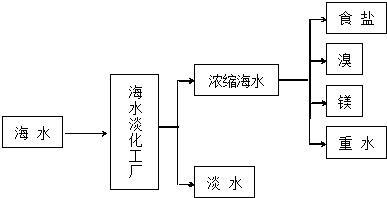
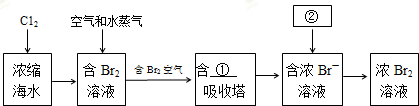
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
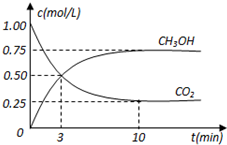 在體積為1L的密閉容器中,充入1mol CO2和3mol H2,在500oC下發生反應:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);△H=-49.0kJ/mol測得CO2和CH3OH(g)的濃度隨時間變化如圖所示.
在體積為1L的密閉容器中,充入1mol CO2和3mol H2,在500oC下發生反應:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);△H=-49.0kJ/mol測得CO2和CH3OH(g)的濃度隨時間變化如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 26g的苯和乙炔的混合物最多可以與2mol的氫氣發生加成 | |
| B. | 某溫度下,MgCO3的Ksp=4×10-6,則飽和溶液中含Mg2+數目為2×10-3NA | |
| C. | 標準狀況下,NA個NO分子和0.5NA個O2分子充分反應后氣體體積為22.4 L | |
| D. | 氫氣與氯氣反應生成標準狀況下22.4 L氯化氫,斷裂化學鍵總數為1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ,該化合物中含有極性共價鍵(填“極性”或“非極性”).
,該化合物中含有極性共價鍵(填“極性”或“非極性”).查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com