
| A. | 28g | B. | 56g | C. | 14g | D. | 無法計算 |
分析 鹽酸恰好使混合物完全溶解,鹽酸沒有剩余,向反應所得溶液加KSCN溶液無血紅色出現,說明溶液為FeCl2溶液,根據氯元素守恒可知n(FeCl2)=$\frac{1}{2}$n(HCl),用足量的CO在高溫下還原相同質量的混合物得到鐵,根據鐵元素守恒可知n(Fe)=n(FeCl2),據此結合m=nM計算得到的鐵的質量.
解答 解:鹽酸恰好使混合物完全溶解,鹽酸沒有剩余,向反應所得溶液加KSCN溶液無血紅色出現,說明溶液為FeCl2溶液,根據氯元素守恒可知n(FeCl2)=$\frac{1}{2}$n(HCl)=$\frac{1}{2}$×0.2L×5mol/L=0.5mol,用足量的CO在高溫下還原相同質量的混合物得到鐵,根據鐵元素守恒可知n(Fe)=n(FeCl2)=0.5mol,質量為0.5mol×56g/mol=28g,故選A.
點評 本題考查混合物計算,明確發生的反應是解題關鍵,注意守恒思想的應用,難度中等.


科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
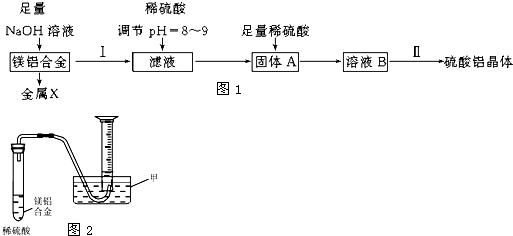
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,1.12 L CCl4含有C-Cl鍵的數目為0.2NA | |
| B. | 1 L 1 mol/L AlCl3溶液中含有NA個Al3+ | |
| C. | 常溫常壓下,4.4 g CO2與N2O的混合氣體中含有的原子總數為0.3NA | |
| D. | 80 mL 10 mol•L-1鹽酸與足量MnO2加熱反應,產生的Cl2分子數為0.2NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com