
【題目】鎢是熔點最高的金屬,也是重要的戰略物資。自然界中鎢礦石主要有黑鎢礦和白鎢礦兩種。其中,黑鎢礦主要成分是鐵和錳的鎢酸鹽(FeWO4、MnWO4) 以及少量雜質(含Si、P、As元素的化合物)。由黑鎢礦冶煉鎢的“黑鎢精礦高壓堿煮(燒破)一溶劑萃取一蒸發結晶法”工藝流程如下圖:

回答下列問題:
(1) 高壓堿煮法中,“高壓”的目的是_____________。
(2) 濾渣1的主要成分中含有的金屬元素為_______。
(3) 除最后 一步外,流程中鎢元素價態均未發生改變,則FeWO4中鐵元素的價態為_____。第一步黑鎢礦原料熔融時,FeWO4發生反應的化學方程式為________。
(4) H2SO4中和后溶液中還有SiO32-、AsO33-、AsO43-、PO43-等離子,則加入H2O2時發生反 應的離子方程式為_________。
(5) 鎢酸鈉溶液還含有NaOH、NaCl 和_____雜質。為了得到純凈的鎢酸,需要經過萃取和反萃取工業流程。該操作中使用到的玻璃儀器有_________。 向鎢酸鈉溶液中加入四辛基氧化銨有機萃取劑萃取分液,此時鎢元素處于_____層中(填“有機”或“無機”)。然后加入氨水反萃取、結晶得到仲鎢酸銨(NH4)6W7O2·7H2O,仲鎢酸銨加熱分解得到三氧化鎢的化學方程式為_________________________。
【答案】 增大氧氣的濃度,提高反應速率 Fe、 Mn。 +2 4FeWO4+8NaOH+O2![]() 4Na2WO4+2Fe2O3+4H2O(無加熱符號不扣分) AsO33-+H2O2=AsO43-+H2O Na2SO4 分液漏斗、燒杯 有機 (NH4)6W7O24·7H2O
4Na2WO4+2Fe2O3+4H2O(無加熱符號不扣分) AsO33-+H2O2=AsO43-+H2O Na2SO4 分液漏斗、燒杯 有機 (NH4)6W7O24·7H2O![]() 6NH3↑+ 7WO3 + 10H2O
6NH3↑+ 7WO3 + 10H2O
【解析】試題分析:(1)氧氣是反應物,增大壓強可以提高反應速率;(2)黑鎢礦主要成分是鐵和錳的鎢酸鹽,高壓堿煮,過濾后的溶液中含有鎢酸鈉,不含Fe、 Mn元素;(3) 鎢酸鈉中W元素的化合價是+6,根據化合價代數和等于0計算FeWO4中Fe元素的化合價; FeWO4與NaOH、O2加熱熔融生成Na2WO4、Fe2O3;(4) 根據流程圖,加入H2O2時AsO33-被氧化為AsO43-;(5)根據流程圖,鎢酸鈉溶液中含有硫酸根離子;萃取分液用到的玻璃儀器是分液漏斗、燒杯;向鎢酸鈉溶液中加入四辛基氧化銨有機萃取劑萃取分液,鎢元素處于有機層;仲鎢酸銨分解生成NH3、WO3 、H2O;
解析:(1)高壓堿煮法中,氧氣是反應物,“高壓”的目的是增大氧氣的濃度,提高反應速率;(2)黑鎢礦主要成分是鐵和錳的鎢酸鹽,高壓堿煮,過濾后的溶液是鎢酸鈉,不含Fe、 Mn元素,所以濾渣1的主要成分中含有的金屬元素為Fe、 Mn;(3) 鎢酸鈉中W元素的化合價是+6,根據化合價代數和等于0,FeWO4中Fe元素的化合價為+2;FeWO4與NaOH、O2加熱熔融生成Na2WO4、Fe2O3,反應方程式是4FeWO4+8NaOH+O2![]() 4Na2WO4+2Fe2O3+4H2O;(4) 根據流程圖,加入H2O2時AsO33-被氧化為AsO43-,反應的話離子方程式是AsO33-+H2O2=AsO43-+H2O;(5)根據流程圖,鎢酸鈉溶液中含有硫酸根離子,所以鎢酸鈉溶液還含有NaOH、NaCl和Na2SO4雜質;萃取分液用到的玻璃儀器是分液漏斗、燒杯;根據題意,向鎢酸鈉溶液中加入四辛基氧化銨有機萃取劑萃取分液,鎢元素處于有機層;仲鎢酸銨分解生成WO3 的方程式是(NH4)6W7O24·7H2O
4Na2WO4+2Fe2O3+4H2O;(4) 根據流程圖,加入H2O2時AsO33-被氧化為AsO43-,反應的話離子方程式是AsO33-+H2O2=AsO43-+H2O;(5)根據流程圖,鎢酸鈉溶液中含有硫酸根離子,所以鎢酸鈉溶液還含有NaOH、NaCl和Na2SO4雜質;萃取分液用到的玻璃儀器是分液漏斗、燒杯;根據題意,向鎢酸鈉溶液中加入四辛基氧化銨有機萃取劑萃取分液,鎢元素處于有機層;仲鎢酸銨分解生成WO3 的方程式是(NH4)6W7O24·7H2O![]() 6NH3↑+ 7WO3 + 10H2O;
6NH3↑+ 7WO3 + 10H2O;


科目:高中化學 來源: 題型:
【題目】綠礬(FeSO4·nH2O)在工農業生產中具有重要的用途。某化學興趣小組對綠礬的一些性質進行探究。請回答下列問題:
(1)在試管中加入少量綠礬樣品,加水溶解,滴加KSCN溶液,溶液顏色無明顯變化;再向試管中通入空氣,溶液逐漸變紅。請解釋變紅的原因________________________。
(2)為測定某綠礬中結晶水含量,按下圖組裝好儀器并檢查氣密性。將石英玻璃管(帶兩端開關K1和K2)(設整個為裝置A)稱重,記為80.120g。將樣品裝入石英玻璃管中,再次將裝置A稱重,記為 107.020g。按下圖連接好裝置進行實驗。
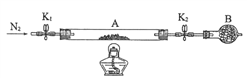
①儀器B的名稱是____________________。
②實驗操作步驟為: 第一步: 打開K1和K2,緩緩通入N2 ; 第二步:點燃酒精燈,小心加熱;第三步:熄滅酒精燈 ;第四步:冷卻到室溫 ; 第五步:關閉K1和K2 ; 第六步:稱量A 。 請問: 第一步緩緩通入N2 的目的是________________________。
重復上述操作步驟,直至A恒重,記為95.320g。
③計算綠礬化學式中結晶水n=________________(保留一位小數)。
(3)同學們查找資料可知,硫酸亞鐵在高溫下分解產物為Fe2O3 以及 SO2和SO3。為了驗證硫酸亞鐵分解的氣體產物,將已恒重的裝置A接入下圖所示的裝置中,打開K1和K2,緩緩通入N2,加強熱充分反應后,管中殘留固體為 _______ 色粉末。![]()
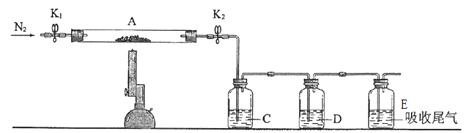
C、D中的溶液依次為________ 、________(填標號)。
a.品紅 b.NaOH c.BaCl2 d.濃硫酸
(4)“嚴謹不僅僅是一種生活態度,更是科學精神”。檢查裝置氣密性是化學實驗中的重要操作之一,在上述32題實驗裝置氣密性檢查的操作是_______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知下列氧化劑均能氧化+4價的硫元素,為了除去稀硫酸中混有的亞硫酸,應選用的最合理的氧化劑是( )
A.KMnO4
B.Ca(ClO)2
C.Cl2
D.H2O2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】香煙煙霧中往往含有CO和SO2氣體,下列關于這兩種氣體的說法正確的是( )
A.兩者都易溶于水
B.兩者都污染環境,危害健康
C.兩者都能使品紅溶液褪色
D.兩者都是形成酸雨的主要原因
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】As的原子結構示意圖為![]() ,下列關于As的描述不正確的是 ( )
,下列關于As的描述不正確的是 ( )
A. 位于第四周期,第ⅤA族 B. 屬于非金屬元素
C. 酸性:H3AsO4﹥H3PO4 D. 穩定性:AsH3﹤PH3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是人類從海水資源中提取某些重要化工原料的流程示意圖:
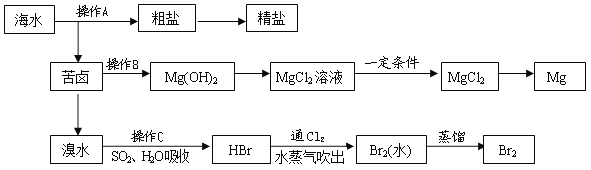
請回答下列問題:
(1)操作A是__________________和過濾(填實驗基本操作名稱)
(2)操作B需加入下列試劑中的一種,最合適的是________(選填編號)
A. 氫氧化鈉溶液 B. 澄清石灰水
C. 石灰乳 D. 碳酸鈉溶液
(3)向苦鹵中通入Cl2,發生反應的離子方程式是_____________________,用SO2水溶液吸收Br2 ,吸收率可達95%,有關反應的離子方程式為___________________。
(4)工業上由無水MgCl2制取鎂的化學方程式為____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某課題組為了深入探究二氧化硫的性質設計以下裝置進行了實驗。
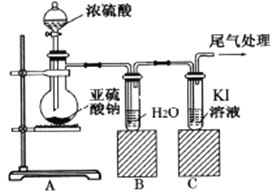
步驟一:檢驗裝置氣密性后向B、C中各加入20mL圖示液體。
步驟二 :打開A中活塞,反應進行10分鐘后關閉活塞。
步驟三:用pH計分別測量B、C 試管中溶液的pH。
結合上述實驗,回答以下問題:
(1) 甲同學認為兩瓶中pH大致相等,原因是二氧化硫溶于水后生成了酸性物質。該物質發生電離,其電離方程式為___________。
(2) 乙同學認為C瓶中pH可能更小,因為C中二氧化硫會像氧化硫化氫一樣與碘離子發生氧化還原反應。通過pH計測定,B瓶中pH為2.13,C瓶中pH為1.05。為了解釋該實驗現象,該同學提出進行多次平行實驗,目的是____________。測定結果如下:
第1次實驗 | 第2次實驗 | 第3 次實驗 | |
B 瓶中pH | 2.15 | 2.10 | 2. 17 |
C 瓶中pH | 1.10 | 1.12 | 1.09 |
實驗發現: C瓶中溶液的酸性始終比B瓶中的酸性強。
(3) 通過仔細觀察,C瓶中溶液從無色變成淺黃色同時出現黃色渾濁,繼續通入氣體溶液又逐漸變為無色。其中溶液變黃且出現渾濁的過程對應的離子方程式為________,為了檢驗產物,中間取出少許溶液加入______,溶液變藍,證明乙同學判斷正確;黃色溶液又逐漸變為無色對應的化學反應方程式為_______________。
(4) 最終結論:
①B瓶中溶液呈弱酸性是由于__________。
②C瓶中溶液呈強酸性是由于生成了_________,該過程中體現出二氧化硫哪些化學性質_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為研究銅與濃硫酸的反應,某化學興趣小組進行如下實驗.
實驗I:反應產物的定性探究
按如圖裝置(固定裝置已略去)進行實驗
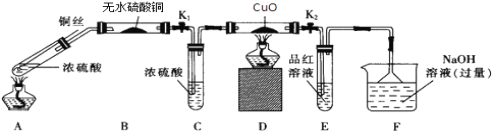
(1)A裝置的試管中發生反應的化學方程式是____________;B裝置的作用是________E裝置中的現象是_______;
(2)實驗過程中,能證明無氫氣生成的現象是________。
(3)F裝置的燒杯中發生反應的離子方程式是_____________________。
實驗Ⅱ:反應產物的定量探究
(4)為測定硫酸銅的產率,將該反應所得溶液中和后配制成250.00 mL溶液,取該溶液25.00mL加入足量KI溶液中振蕩,生成的I2恰好與20.00 mL 0.30 molL﹣1的Na2S2O3溶液反應,若反應消耗銅的質量為6.4g,則硫酸銅的產率為________。(已知2Cu2++4I﹣=2CuI+I2, 2S2O32﹣+I2=S4O62﹣+2I﹣)(注:硫酸銅的產率指的是硫酸銅的實際產量與理論產量的比值)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是
A. 大米富含淀粉
B. 加碘食鹽含有碘酸鉀(KIO3)
C. 人體必需的微量元素就是維生素
D. 人體必需的微量元素不都是金屬元素
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com