
| A. | 整個過程的反應速率由反應②決定 | B. | N2O2,N2O是該反應的催化劑 | ||
| C. | 當$\frac{1}{2}$v(NO)=v(N2)時,反應達到平衡 | D. | 該反應的活化能為665kJ•mol-3 |
分析 A、若總反應由一系列快慢懸殊的連續步驟組成,總反應速率就決定于其中最慢的一步;
B、根據催化劑為參加反應,但反應前后質量和化學性質不變來判斷;
C、根據正逆反應速率相等判斷;
D、根據NO與H2反應后生成1molN2和水蒸氣時,放出665kJ熱量,則該反應的焓變為-665kJ•mol-1.
解答 解:A、若總反應由一系列快慢懸殊的連續步驟組成,總反應速率就決定于其中最慢的一步,②N2O2+H2=N2O+H2O(慢),所以總反應的速率主要取決于三步反應中的②,故A正確;
B、因為催化劑為參加反應,在反應前后質量和化學性質不變,所以N2O2,N2O僅僅是反應的中間產物,并不是催化劑,故B錯誤;
C、當$\frac{1}{2}$v(NO)=v(N2)時,未指明正逆方向,故C錯誤;
D、因為NO與H2反應后生成1molN2和水蒸氣時,放出665kJ熱量,則該反應的焓變為-665kJ•mol-1,故D錯誤;
故選:A.
點評 本題主要考查了化學反應的原理,涉及到若總反應由一系列快慢懸殊的連續步驟組成,總反應速率就決定于其中最慢的一步,催化劑的判斷,平衡狀態的判斷等,難度不大.


 智慧小復習系列答案
智慧小復習系列答案科目:高中化學 來源: 題型:解答題
 A、B、C為短周期元素,在周期表中所處的位置如右圖所示.A、C兩元素的原子核外電子數之和等于B原子的質子數.B的最外層電子數是其電子層數兩倍.
A、B、C為短周期元素,在周期表中所處的位置如右圖所示.A、C兩元素的原子核外電子數之和等于B原子的質子數.B的最外層電子數是其電子層數兩倍. .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 L 2 mol•L-1的醋酸鈉溶液中CH3COO- 的數目小于2NA | |
| B. | 常溫常壓下,1.12 L O2氣體所含原子數為0.1NA | |
| C. | 將2 mol NO和1 mol O2混合后,體系中的分子總數為3NA | |
| D. | 1 mol羥基含有的電子數為10NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在金屬元素與非金屬元素的分界線附近可以尋找制備半導體材料的元素 | |
| B. | 在過渡元素中可以尋找制備催化劑及耐高溫和耐腐蝕的元素 | |
| C. | 在金屬元素區域可以尋找制備新型農藥材料的元素 | |
| D. | 周期表中位置靠近的元素性質相似 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

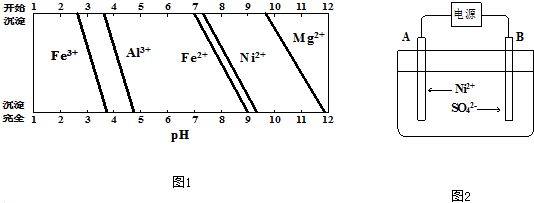
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 控制適合的條件,將反應AsO43-+2I-+2H+? AsO33-+I2+H2O 設計成如圖所示的原電池.下列判斷正確的是( )
控制適合的條件,將反應AsO43-+2I-+2H+? AsO33-+I2+H2O 設計成如圖所示的原電池.下列判斷正確的是( )| A. | 反應開始時,B池中石墨電極上發生氧化反應 | |
| B. | 反應開始時,A池中石墨電極上I-被還原 | |
| C. | 反應開始時,鹽橋中K+由左向右遷移 | |
| D. | 電流計讀數為零后,在B池中溶入Na3AsO3固體,B池中的石墨電極為正極 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 甲醇脫氧制取甲醛的原理為CH3OH(g)?HCHO(g)+H2(g),某科研小組在1L恒溶密閉容器中充入1molCH3OH,對該反應進行了一系列的研究,得到甲醇的平衡轉化率隨溫度的變化曲線如圖所示.
甲醇脫氧制取甲醛的原理為CH3OH(g)?HCHO(g)+H2(g),某科研小組在1L恒溶密閉容器中充入1molCH3OH,對該反應進行了一系列的研究,得到甲醇的平衡轉化率隨溫度的變化曲線如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
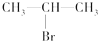 (主要產物),1mol某芳香烴A充分燃燒后可以得到8molCO2和4molH2O.該烴A在不同條件下能發生如下所示的一系列變化.
(主要產物),1mol某芳香烴A充分燃燒后可以得到8molCO2和4molH2O.該烴A在不同條件下能發生如下所示的一系列變化.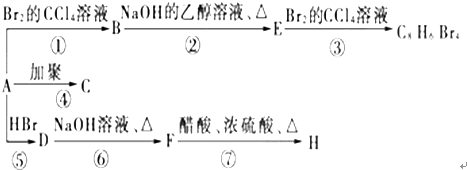
 ②的反應類型:消去反應
②的反應類型:消去反應 +CH3COOH$→_{△}^{濃H_{2}SO_{4}}$
+CH3COOH$→_{△}^{濃H_{2}SO_{4}}$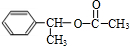 +H2O,反應類型:酯化(取代)反應
+H2O,反應類型:酯化(取代)反應查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 由H、N、O三種元素形成的化合物中一定含有共價鍵 | |
| B. | 正戊烷、異丁烷和丙烷屬于同系物,沸點依次升高 | |
| C. | 葡萄糖能發生銀鏡反應,蔗糖、麥芽糖也能發生銀鏡反應 | |
| D. | 用KSCN溶液檢驗Fe3+的實驗現象是產生血紅色沉淀 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com