
【題目】工業上以鉻鐵礦(主要成分為FeO和Cr2O3,含有Al2O3、SiO2等雜質)為主要原料生產化工原料紅礬鈉(主要成分為:Na2Cr2O7·2H2O),其主要工藝流程如下:

查閱相關資料得知:
i.常溫下,NaBiO3不溶于水,有強氧化性,在堿性條件下能將Cr3+轉化為CrO42-,自身被還原為Bi(OH)3固體。
ii.幾種金屬離子沉淀的pH:
物質 | 開始沉淀的pH | 完全沉淀的pH |
Fe(OH)3 | 2.7 | 3.7 |
Al(OH)3 | 3.4 | 4.4 |
Cr(OH)3 | 4.6 | 5.9 |
Fe(OH)2 | 7.5 | 9.7 |
Bi(OH)3 | 0.7 | 4.5 |
回答下列問題:
(1)加入過量硫酸之前先要將鉻鐵礦礦石粉碎,其目的是________________________。
(2)操作I、III、IV用到的主要玻璃儀器有玻璃棒和___________(填儀器名稱)。
(3)寫出④反應的化學方程式_____________________________________________。
(4)⑤中酸化是使CrO42-轉化為Cr2O72-![]() 寫出該反應的離子方程式_____________。
寫出該反應的離子方程式_____________。
(5)將溶液H經下列操作:蒸發濃縮,__________,過濾,洗滌,干燥即得紅礬鈉。
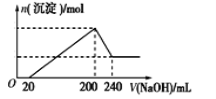
(6)取一定質量的固體D溶解于200 mL的稀硫酸中,向所得溶液中加入5.0 mol/L的NaOH溶液,生成沉淀的物質的量(n)與加入NaOH溶液的體積(V)關系如圖所示,則稀硫酸的濃度為_________,固體D中含鐵化合物的物質的量為___________。
【答案】增大反應物的接觸面積,加快反應速率,提高浸出率 漏斗、燒杯 3NaBiO3 + Cr2(SO4)3+ 7NaOH+ H2O = 2Na2CrO4 + 3Na2SO4 +3Bi(OH)3 2CrO42-+2H+ ![]() Cr2O72-+H2O 冷卻結晶 2.5mol·L-1 0.1mol
Cr2O72-+H2O 冷卻結晶 2.5mol·L-1 0.1mol
【解析】
(1)加入過量硫酸之前先要將鉻鐵礦礦石粉碎,其目的是增大反應物的接觸面積,加快反應速率,提高浸出率;綜上所述,本題答案是:增大反應物的接觸面積,加快反應速率,提高浸出率。
(2)操作I、III、IV均為過濾,則用到的主要玻璃儀器有玻璃棒和漏斗、燒杯;綜上所述,本題答案是:漏斗、燒杯。
(3)從流程可以看出:NaBiO3與Cr2(SO4)3在堿性環境下發生氧化還原反應,反應生成Bi(OH)3和Na2CrO4,反應的化學方程式3NaBiO3 +Cr2(SO4)3+7NaOH+ H2O = 2Na2CrO4 +3Na2SO4 +3Bi(OH)3;綜上所述,本題答案是:3NaBiO3 +Cr2(SO4)3+7NaOH+H2O = 2Na2CrO4 + 3Na2SO4 +3Bi(OH)3。
(4)在酸性條件下,CrO42-可以部分轉化為Cr2O72-,反應的離子方程式:2CrO42-+2H+ ![]() Cr2O72-+H2O ;綜上所述,本題答案是:2CrO42-+2H+
Cr2O72-+H2O ;綜上所述,本題答案是:2CrO42-+2H+ ![]() Cr2O72-+H2O。
Cr2O72-+H2O。
(5)從溶液中得到晶體的一般操作是:蒸發濃縮,冷卻結晶,過濾,洗滌,干燥;經過以上步驟就可以得到紅礬鈉;綜上所述,本題答案是:冷卻結晶。
(6)根據圖像可知加入氫氧化鈉時沒有立即產生沉淀,說明酸過量,首先發生酸堿中和,當沉淀不再發生變化時需要氫氧化鈉是180毫升,繼續加入氫氧化鈉沉淀開始減小,即氫氧化鋁開始溶解,溶解氫氧化鋁消耗的氫氧化鈉溶液體積是40毫升,則生成氫氧化鋁消耗的氫氧化鈉溶液的體積是120毫升,所以與鐵離子反應的氫氧化鈉溶液體積是60毫升,物質的量為0.06×5=0.3mol,根據方程式:Fe3++3OH-=Fe(OH)3↓可知,鐵離子的量為0.1mol;根據鐵元素守恒可知,固體D中含有鐵元素的化合物FeO的物質的量為0.1mol,當沉淀達到最大值時溶液中的溶質是硫酸鈉,則根據原子守恒可知硫酸鈉的物質的量為0.2×5/2=0.5mol;則硫酸的濃度為0.5/0.2=2.5mol/L;綜上所述,本題答案是:2.5mol·L-1 ;0.1mol。


 口算能手系列答案
口算能手系列答案科目:高中化學 來源: 題型:
【題目】元素周期表的形式多種多樣,如圖是扇形元素周期表的一部分(1~36號元素),對比中學常見元素周期表,思考扇形元素周期表的填充規律,推出圖中標記的11種元素,回答下列問題:
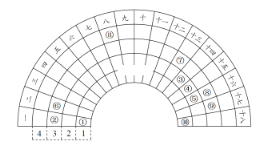
(1)⑤元素形成的簡單陰離子的結構示意圖為________。
(2)④的氣態氫化物的電子式為_____。
(3)在11種元素中,單質的化學性質最不活潑的是_______。(填化學式)
(4)⑧⑨兩種元素形成的最高價氧化物的水化物中,酸性較強的是________。(填化學式)
(5)③的單質可以和⑧的最高價氧化物的水化物的濃溶液反應,請寫出有關反應的化學方程式____________。
(6)⑦在元素周期表中的位置是________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某陰離子Rn- 的核外共有x個電子,核內有a個中子,則R的質量數為( )
A. a+x-n B. a+x+n C. a-x-n D. a-x+n
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,下列有關電解質溶液敘述錯誤的是
A. 某H2SO4溶液中c(OH-)/c(H+)=1.0×10-8,由水電離出的c(H+)=1×10-11mol·L-1
B. 將0.02mol·L-1鹽酸與0.02mol·L-1Ba(OH)2溶液等體積混合后溶液pH約為12
C. 將一定體積稀鹽酸與稀氨水混合,當溶質為NH3·H2O和NH4Cl時,溶液的pH一定大于7
D. 向0.1mol·L-1Na2CO3溶液中逐滴滴加0.1mol·L-1稀鹽酸,溶液中c(HCO)先增大后減小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于鋁的性質,錯誤的說法是( )
A.鋁的表面能形成致密的氧化膜,因此鋁難腐蝕
B.鋁能溶解于冷的濃硝酸氧化成為硝酸鋁
C.鋁能溶解于NaOH溶液生成偏鋁酸鈉和氫氣
D.鋁能在氯氣中燃燒,生成氯化鋁
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列指定反應的離子方程式正確的是
A. Ca(ClO)2溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O=CaSO4↓+H++Cl-+ HClO
B. 向FeCl2溶液加入足量NaClO溶液:6Fe2++3ClO-+3H2O=2Fe(OH)3↓+4Fe3++3Cl-
C. NH4HCO3溶液和過量的NaOH溶液混合:HCO![]() +OH-===CO
+OH-===CO![]() +H2O
+H2O
D. 向Fe(NO3)3溶液中加入足量的HI溶液:2Fe3++2I-= 2Fe2++I2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】草酸鐵晶體Fe2(C2O4)3·xH2O可溶于水,且能做凈水劑。為測定該晶體中鐵的含量,做了如下實驗:
步驟1:稱量5.6g草酸鐵晶體,配制成250 mL一定物質的量濃度的溶液。
步驟2:取所配溶液25.00 mL于錐形瓶中,先加足量稀H2SO4酸化,再滴加KMnO4溶液,反應為:2KMnO4+5H2C2O4+3H2SO4═ K2SO4+2MnSO4+10CO2↑+8H2O。向反應后的溶液加鋅粉,加熱至黃色剛好消失,過濾、洗滌,將過濾及洗滌所得溶液收集到錐形瓶中,此時溶液仍呈酸性。
步驟3:用0.0200 mol/LKMnO4溶液滴定步驟2所得溶液至終點,消耗KMnO4溶液V1 mL,滴定中MnO4-被還原成Mn2+。
重復步驟2、步驟3的操作2次,分別滴定消耗0.0200 mol/LKMnO4溶液為V2、V3 mL。
記錄數據如下表:
實驗編號 | KMnO4溶液的濃度(mol/L) | KMnO4溶液滴入的體積(mL) |
1 | 0.0200 | V1 = 20.02 |
2 | 0.0200 | V3 = 19.98 |
3 | 0.0200 | V2 = 23.32 |
請回答下列問題:
(1)草酸鐵溶液能做凈水劑的原因______________________________(用離子方程式表示)。
(2)步驟2加入酸性高錳酸鉀的作用_________________________________________________。
(3)加入鋅粉的目的是______________________________。
(4)步驟3滴定時滴定終點的判斷方法是_____________________________________________。
(5)在步驟3中,下列滴定操作使測得的鐵含量偏高的有______。
A.滴定管用水洗凈后直接注入KMnO4溶液
B.滴定管尖嘴內在滴定前有氣泡,滴定后氣泡消失
C.讀取KMnO4溶液體積時,滴定前平視,滴定結束后仰視讀數
D.錐形瓶在滴定時劇烈搖動,有少量液體濺出.
(6)實驗測得該晶體中鐵的含量為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關說法正確的是
A. 常溫下,苯是一種無色無味液體,不溶于水
B. 油脂屬于高分子化合物,熱值較大
C. 葡萄糖溶液中加入銀氨溶液,水浴加熱有銀鏡生成
D. 蛋白質遇濃硝酸,微熱產生藍色沉淀
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com