

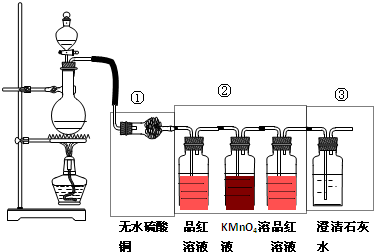
 CO2↑+2SO2↑+2H2O,一般檢驗含有水汽的混合氣體,水通常是第一個檢驗的,用無水硫酸銅,現象是固體變藍;根據檢驗S02和CO2時,就要先把S02檢驗了,用品紅溶液,現象是品紅溶液褪色,并除掉S02,用KMnO4溶液,同時用品紅溶液檢驗是否除盡,這樣石灰水變渾濁才能說明有CO2.
CO2↑+2SO2↑+2H2O,一般檢驗含有水汽的混合氣體,水通常是第一個檢驗的,用無水硫酸銅,現象是固體變藍;根據檢驗S02和CO2時,就要先把S02檢驗了,用品紅溶液,現象是品紅溶液褪色,并除掉S02,用KMnO4溶液,同時用品紅溶液檢驗是否除盡,這樣石灰水變渾濁才能說明有CO2.

科目:高中化學 來源: 題型:
| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
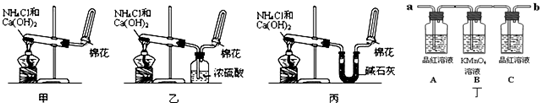
查看答案和解析>>
科目:高中化學 來源:不詳 題型:問答題
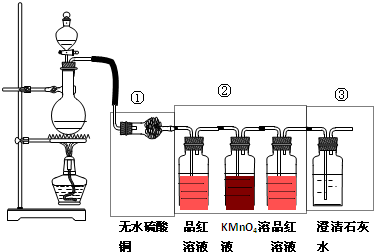
查看答案和解析>>
科目:高中化學 來源:不詳 題型:問答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com