
【題目】Na2S粗品含有雜質,其純化、含量測定方法如下。回答下列問題:
(1)粗品經水浸、過濾、__________________、洗滌、干燥等操作可以除去不溶性雜質,得到較純的Na2S固體。
(2)國標中采用如圖所示裝置測定Na2S樣品溶液中Na2CO3的百分含量(實驗前,吸收管1、吸收管2、參比管中均裝入組成相同的乙醇、丙酮混合溶液,該溶液吸收CO2后,顏色發生改變) 。

(步驟一)標定KOH標準溶液
準確稱取w g鄰苯二甲酸氫鉀(KC8H5O4,摩爾質量為M g/mol)置于錐形瓶中,加入適量蒸餾水、2滴指示劑,用待標定的KOH溶液滴定至終點,消耗v mL KOH溶液。
①標定過程中應該選用的指示劑名稱是______,理由是__________;
(已知鄰苯二甲酸的電離平衡常數為Ka1=1.1×10-3,Ka2=4.0×10-6)
②KOH溶液的準確濃度為_____mol/L(用含M、v、w的代數式表示)
(步驟二)往三頸燒瓶中先后加入100mL 樣品溶液、15 ml過氧化氫溶液(足量),連接好裝置,加熱并打開抽氣裝置;
(步驟三)上述反應完成后,從滴液漏斗中慢慢加入足量稀硫酸溶液,充分反應;
(步驟四)用裝置6中的KOH標準溶液滴定吸收管1中的溶液至與參比管中溶液相同的顏色,3 min內不變色為終點。
③過氧化氫的作用是______;堿石棉的作用是__________;
④如果抽氣速度過快,可能導致測定結果_________(填“偏高”、“偏低”或“無影響”);
⑤若步驟三中出現_______________________(填現象),說明實驗失敗,必須重新測定。
【答案】蒸發濃縮、冷卻結晶、過濾 酚酞 滴定終點為鄰苯二甲酸鉀的水溶液,呈堿性 ![]() 氧化除去S2- 除去空氣中的CO2 偏低 吸收管2中的溶液顏色發生明顯變化
氧化除去S2- 除去空氣中的CO2 偏低 吸收管2中的溶液顏色發生明顯變化
【解析】
(1)粗品經水浸、過濾、蒸發濃縮、冷卻結晶、過濾、洗滌、干燥等操作可以除去不溶性雜質,得到較純的Na2S固體。
(2)①根據滴定終點溶液的性質選擇指示劑;
②根據KC8H5O4+KOH= K2C8H4O4+H2O找到數量關系,進行計算;
③過氧化氫具有氧化性,為了實驗結果準確要防止空氣中的二氧化碳被吸收;
④抽氣過快反應不能完全進行;
⑤步驟四中只滴定吸收管1中的溶液,則要保證吸收管1可以吸收全部二氧化碳。
(1)粗品經水浸、過濾、蒸發濃縮、冷卻結晶、過濾、洗滌、干燥等操作可以除去不溶性雜質,得到較純的Na2S固體。故答案為:蒸發濃縮、冷卻結晶、過濾;
(2)①滴定終點為鄰苯二甲酸鉀的水溶液,存在鄰苯二甲酸根的水解,導致溶液呈堿性,所以選用酚酞做指示劑,故答案為:酚酞;滴定終點為鄰苯二甲酸鉀的水溶液,呈堿性;
②滴定過程發生反應KC8H5O4+KOH= K2C8H4O4+H2O,則反應中鄰苯二甲酸氫鉀的物質的量與氫氧化鉀物質的量相同,n(KC8H5O4)=![]() mol,則n(KOH)=
mol,則n(KOH)=![]() mol,濃度c=
mol,濃度c=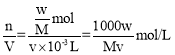 ,故答案為
,故答案為![]() ;
;
③過氧化氫具有氧化性,可以將硫離子氧化,以免生成硫化氫影響實驗結果;為了實驗結果準確要防止空氣中的二氧化碳被吸收,故答案為:氧化除去S2-;除去空氣中的CO2;
④抽氣過快二氧化碳不能完全被吸收,繼而使測量結果偏小,故答案為:偏小;
⑤步驟四中只滴定吸收管1中的溶液,則要保證吸收管1可以吸收全部二氧化碳,當吸收管2中顏色發生變化時,說明有二氧化碳在吸收管1中沒有完全被吸收,實驗失敗,故答案為:吸收管2中的溶液顏色發生明顯變化。


科目:高中化學 來源: 題型:
【題目】下列事實能說明醋酸是弱電解質的是 ( )
A. 醋酸能使石蕊溶液變紅
B. ![]() 時.
時.![]() 醋酸的pH約為3
醋酸的pH約為3
C. 向醋酸中加入氫氧化鈉溶液,溶液pH增大
D. 醋酸能與碳酸鈣反應產生![]() 氣體
氣體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】分離提純、溶液的配制和分析是化學家常用的研究物質的實驗方法,根據所學知識,回答下列問題:
Ⅰ.實驗室從海藻中提取碘的流程如圖:

(1)提取碘的過程中,操作③的名稱為___。
(2)“后期處理”中涉及的操作為___。
(3)在灼燒過程中,使用到的實驗儀器有___(除三腳架和酒精燈外)。
A.燒杯 B.蒸發皿 C.坩堝鉗 D.瓷坩堝 E.泥三角
Ⅱ.依據粗鹽提純的原理,除去硝酸鉀固體中少量的硝酸鎂、硫酸鎂雜質,按如圖步驟操作,回答下列問題:

(1)試劑A和B的化學式分別是___,___。
(2)操作Ⅱ為___,___,___。
Ⅲ.實驗室現需配制物質的量濃度為1mol/L的NaOH溶液480mL。
(1)實驗過程中用到的玻璃儀器有:燒杯、玻璃棒、___、___。
(2)要配制此溶液,需要稱量NaOH固體的質量為___。
(3)下列操作會使所配溶液濃度偏大的有___。
A.溶解固體溶質時,未冷卻到室溫即轉入容量瓶定容
B.容量瓶中原有少量蒸餾水
C.定容時仰視讀數
D.砝碼生銹但未脫落
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】隨著氮氧化物對環境及人類活動影響的日趨嚴重,如何消除大氣污染物中的氮氧化物成為人們關注的主要問題之一。
Ⅰ.利用NH3的還原性可以消除氮氧化物的污染,其中除去NO的主要反應如下:4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(l) △H<0
5N2(g)+6H2O(l) △H<0
(1)寫出一種可以提高NO的轉化率的方法:__________
(2)一定溫度下,在恒容密閉容器中按照n(NH3)︰n(NO) =2︰3充入反應物,發生上述反應。下列不能判斷該反應達到平衡狀態的是___________
A.c(NH3)︰c(NO) =2︰3 B.n(NH3)︰n(N2) 不變 C.容器內壓強不變 D.容器內混合氣體的密度不變 E.1molN—H鍵斷裂的同時,生成1molO—H鍵
(3)已知該反應速率v正=k正·c4(NH3)·c6 (NO),v逆=k逆·cx(N2)·cy(H2O) (k正、k逆分別是正、逆反應速率常數),該反應的平衡常數K=k正/k逆,則x=_____,y=_______。
(4)某研究小組將2molNH3、3molNO和一定量的O2充入2L密閉容器中,在Ag2O催化劑表面發生上述反應,NO的轉化率隨溫度變化的情況如圖所示:

①在5min內,溫度從420K升高到580K,此時段內NO的平均反應速率v(NO)=_______;
②在有氧條件下,溫度580K之后NO生成N2的轉化率降低的原因可能是___________。
Ⅱ.用尿素[(NH2)2CO]水溶液吸收氮氧化物也是一種可行的方法。NO和NO2不同配比混合氣通入尿素溶液中,總氮還原率與配比關系如圖。

(5)用尿素[(NH2)2CO]水溶液吸收體積比為1∶1的NO和NO2混合氣,可將N元素轉變為對環境無害的氣體。寫出該反應的化學方程式____。
(6)隨著NO和NO2配比的提高,總氮還原率降低的主要原因是________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】草酸是一種二元弱酸,可用作還原劑、沉淀劑等。某校課外小祖的同學設計利用C2H2氣體制取H2C2O42H2O。回答下列問題:
(1)甲組的同學以電石(主要成分CaC2,少量CaS及Ca3P2雜質等)為原料,并用如圖裝置制取C2H2。

①電石與水反應很快,為了減緩反應速率,裝置A中除用飽和食鹽水代替水之外,還可以采取的措施是____________________________ (寫一種即可)。
②裝置B中,NaClO將H2S、PH3 氧化為硫酸及磷酸,本身被還原為NaCl,其中PH3被氧化的離子方程式為________________________。
(2)乙組的同學根據文獻資料,用Hg(NO3)2作催化劑,濃硝酸氧化C2H2制取H2C2O4·2H2O。制備裝置如圖所示:

①裝置D中多孔球泡的作用是______________________。
②裝置D中生成H2C2O4的化學方程式為___________________________________。
③從裝置D中得到產品,還需經過__________________(填操作名稱)、過濾、洗滌及干燥。
(3)丙組設計了測定乙組產品中H2C2O4·2H2O的質量分數實驗。他們的實驗步驟如下:準確稱取m g產品于錐形瓶中,加入適量的蒸餾水溶解,再加入少量稀硫酸,然后用c mol/L酸性KMnO4標準溶液進行滴定至終點,共消耗標準溶液V mL。
①滴定時高錳酸鉀標準溶液盛放在滴定管中_____________(填“酸式”或“堿式”)。
②滴定過程中發現褪色速率開始很慢后逐漸加快,分析可能的原因是______________ 。
③產品中H2C2O4·2H2O的質量分數為_________________(列出含 m、c、V 的表達式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學實驗小組擬探究改進Fe(OH)2的制取方法。
方案1:
①實驗藥品:FeS固體、稀硫酸溶液、NaHCO3溶液;
②實驗裝置如圖1。
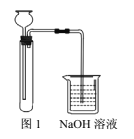
方案2:
①取一只試管,向其中加入一粒NaOH固體,再加入約2mL新制的FeSO4溶液;
②將試管置于酒精燈火焰上,對著有NaOH顆粒的部位小心加熱(不能使液體劇烈沸騰)。使沉淀自下至上慢慢增多,觀察下部沉淀顏色。
方案3:
①先在試管中滴入2~3 mL液體石蠟;
②用膠頭滴管小心往試管底部注入4~5 mL新制的FeSO4溶液;
③再往試管中投入1粒綠豆大小的金屬鈉,觀察反應現象。
回答下列問題:
(1)“方案1”中,后加入試管中的液體是______,NaOH溶液的作用是_______。
(2)“方案2”中,對著有NaOH顆粒的部位小心加熱的目的是________。
(3)“方案2”的沉淀中,上層沉淀的顏色是________,下層沉淀的顏色是________,發生此現象的原因是________。
(4)“方案3”中反應的化學反應方程式為________。
(5)“方案3”的實驗過程中間斷性的出現白色沉淀,其原因是_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,在一容積不變的密閉容器中,充入一定量HI氣體,發生如下可逆反應:
2HI(g)![]() H2(g)+I2(g)ΔH>0。下列說法正確的是( )
H2(g)+I2(g)ΔH>0。下列說法正確的是( )
A.若每消耗2n mol HI的同時生成n mol H2,表明該反應已達平衡
B.容器內的壓強不發生變化,表明該反應已達平衡
C.平衡時,若其他條件不變,再充入一定量HI,重新達平衡后,I2的百分含量增大
D.平衡時,若其他條件不變,升高溫度,混合氣體的顏色加深
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,改變醋酸溶液的pH[溶液中c(CH3COOˉ)與c(CH3COOH)之和始終為0.1mol·Lˉ1],溶液中H+、OHˉ、CH3COOˉ及CH3COOH濃度的對數值(lgc)與pH關系如圖所示。

下列說法錯誤的是
A. lgK(CH3COOH)=-9.26
B. 圖中①表示 CH3COOH濃度的對數值與pH的關系曲線
C. 0.1mol·Lˉ1CH3COOH溶液的pH約為2.88
D. 0.1mol·Lˉ1CH3 COONa溶液的pH約為8.87
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】探究草酸(H2C2O4)性質,進行如下實驗。(已知:H2C2O4是弱電解質)
實驗 | 裝置 | 試劑a | 現象 |
① |
| Ca(OH)2溶液(含酚酞) | 溶液褪色,產生白色沉淀 |
② | 少量NaHCO3溶液 | 產生氣泡 | |
③ | 酸性KMnO4溶液 | 紫色溶液褪色 | |
④ | C2H5OH和濃硫酸 | 加熱后產生有香味物質 |
由上述實驗所得草酸性質所對應的方程式不正確的是( )
A.H2C2O4有酸性:Ca(OH)2+ H2C2O4=CaC2O4↓+2H2O
B.酸性H2C2O4> H2CO3:NaHCO3+ H2C2O4=NaHC2O4+CO2↑+H2O
C.H2C2O4具有還原性:2![]() +5
+5![]() +16H+=2Mn2++10CO2↑+ 8H2O
+16H+=2Mn2++10CO2↑+ 8H2O
D.H2C2O4可發生酯化反應:HOOCCOOH+2C2H5OH![]() C2H5OOCCOOC2H5+2H2O
C2H5OOCCOOC2H5+2H2O
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com