
下圖是從NaCl或CsCl晶體結構圖中分割出來的部分結構圖,其中屬于從NaCl晶體中分割出來的結構圖是( )

A.圖①和圖③ B.圖②和圖③ C.圖①和圖④ D.只有圖④
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源:2015-2016學年黑龍江省高一下期中化學試卷(解析版) 題型:選擇題
分子式為C6H12,分子中具有3個甲基的烯烴共有( )
A.2種 B.3種 C.4種 D.5種
查看答案和解析>>
科目:高中化學 來源:2015-2016學年黑龍江省高二下期中化學試卷(解析版) 題型:填空題
I.氫能的存儲是氫能應用的主要瓶頸,配位氫化物、富氫載體化合物是目前所采用的主要儲氫材料。
(1)Ti(BH4)2是一種過渡元素硼氫化物儲氫材料。在基態Ti2+中,電子占據的最高能層符號為 ,該能層具有的原子軌道數為 。
(2)液氨是富氫物質,是氫能的理想載體,利用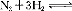 2NH3實現儲氫和輸氫。下列說法正確的是 。
2NH3實現儲氫和輸氫。下列說法正確的是 。
a.NH3分子中氮原子的軌道雜化方式為sp2雜化 b.電負性順序:C<N<O<F
c.由于氨分子間存在氫鍵,所以穩定性:NH3>PH3 d.[Cu(NH3)4]2+中N原子是配位原子
(3)已知NF3與NH3的空間構型相同,但NF3不易與Cu2+形成配離子,其原因是 。
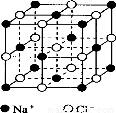
Ⅱ.氯化鈉是生活中的常用調味品,也是結構化學中研究離子晶體時常用的代表物,其晶胞結構如圖所示:
(1)設氯化鈉晶體中Na+與跟它最近鄰的Cl-之間的距離為r,則該Na+與跟它次近鄰的Cl-的個數為 ,該Na+與跟它次近鄰的Cl-之間的距離為 。
(2)已知在氯化鈉晶體中Na+的半徑為a pm,Cl-的半徑為b pm,它們在晶體中是緊密接觸的,則在氯化鈉晶體中離子的空間利用率為 (用含a、b的式子表示)。
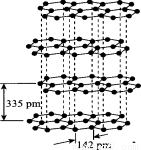
(3)硅與碳是同主族元素,其中石墨為混合型晶體,已知石墨的層間距為335 pm,C--C鍵長為142 pm,則石墨晶體密度約為 (列式并計算,結果保留三位有效數字,NA為6.02×1023 mol-)。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年黑龍江省高二下期中化學試卷(解析版) 題型:選擇題
根據表中給出的幾種物質的熔、沸點數據,判斷下列有關說法中錯誤的是( )
NaCl | MgCl2 | AlCl3 | SiCl4 | 單質B | |
熔點/ ℃ | 810 | 710 | 180 | 68 | 2 300 |
沸點/ ℃ | 1 465 | 1 418 | 160 | 57 | 2 500 |
A.SiCl4是分子晶體 B.單質B可能是原子晶體
C.AlCl3加熱能升華 D.NaCl的鍵的強度比MgCl2小
查看答案和解析>>
科目:高中化學 來源:2015-2016學年黑龍江省高二下期中化學試卷(解析版) 題型:選擇題
高溫下,超氧化鉀晶體(KO2)呈立方體結構。如圖為超氧化鉀晶體的一個晶胞(晶體中最小的重復單元)。則下列有關說法正確的是( )
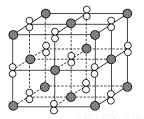
A. 與K+最近且距離相等的K+有6個
B. 超氧化鉀的化學式為KO2,每個晶胞含有1個K+和1個O2-
C. 晶體中與每個K+距離最近的O2-有6個
D. 晶體中,所有原子之間都以離子鍵相結合
查看答案和解析>>
科目:高中化學 來源:2015-2016學年黑龍江大慶市高一下期中化學試卷(解析版) 題型:填空題
甲醇可以與水蒸氣反應生成氫氣,反應方程式如下:
CH3OH(g)+H2O(g)  CO2(g)+3H2(g) ΔH>0
CO2(g)+3H2(g) ΔH>0
(1)一定條件下,向體積為2 L的恒容密閉容器中充入1 mol CH3OH(g)和3 mol H2O(g),20 s后,測得混合氣體的壓強是反應前的1.2倍,則用甲醇表示該反應的速率為________。
(2)判斷(1)中可逆反應達到平衡狀態的依據是(填序號)________。
①v正(CH3OH)=v正(CO2)
②混合氣體的密度不變
③混合氣體的平均相對分子質量不變
④CH3OH、H2O、CO2、H2的濃度都不再發生變化
(3)下圖中P是可自由平行滑動的活塞,關閉K,在相同溫度時,向A容器中充入1 mol CH3OH(g)和2 mol H2O(g),向B容器中充入1.2 mol CH3OH(g)和2.4 mol H2O(g),兩容器分別發生上述反應。已知起始時容器A和B的體積均為a L。試回答: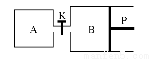
①反應達到平衡時容器B的體積為1.5a L,容器B中CH3OH的轉化率為________;A、B兩容器中H2O(g)的體積百分含量的大小關系為:B________A(填“>”“<”或“=”)。
②若打開K,一段時間后重新達到平衡,容器B的體積為________L(連通管中氣體體積忽略不計,且不考慮溫度的影響)。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年黑龍江大慶市高一下期中化學試卷(解析版) 題型:選擇題
下列依據熱化學方程式得出的結論正確的是( )
A.已知2SO2(g)+O2 2SO3(g) 為放熱反應,則SO2的能量一定高于SO3的能量
2SO3(g) 為放熱反應,則SO2的能量一定高于SO3的能量
B.已知C(石墨,s)═C(金剛石,s)△H>0,則金剛石比石墨穩定
C.已知H+(aq)+OH-(aq)=H2O(1)△H=﹣57.3kJ/mol,則任何酸堿中和的反應熱均為57.3 kJ
D.已知2C(s)+2O2 (g)═2 CO2(g)△H1 2C(s)+O2 (g)═2 CO (g)△H2 則△H1<△H2
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省高一下期中化學試卷(解析版) 題型:填空題
硝酸按是一種常用的化肥,其工業生產流程如下圖,請回答下列問題。
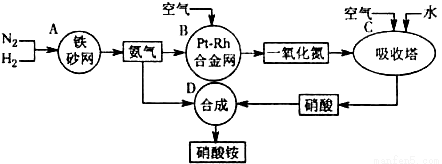
(1)寫出反應容器B中發生反應的化學方程式: 。
(2)吸收塔C中通入空氣的目的是 。C、D兩個反應容器中發生的反應,屬于氧化還原反應的是 (填反應容器代號)。
(3)濃硝酸一般保存在徐色試劑瓶里,并放置在陰涼處,用化學方程式解釋原因: 。
(4)3.04g銅鎂合金完全溶解于100mL密度為1.40g·mL-1、質量分數為63%的濃硝酸中得到NO2和N2O4的混合氣體2240mL(標準狀況),向反應后的溶液中加入2.00mol·L-1NaOH溶液,當金屬離子全部沉淀時,得到5.08g沉淀。則
① 加小Na0H 溶液的體積至少 mL。
② 該合金中銅與鎂的物質的量之比是 。
③ NO2和N2O4的混合氣體中,NO2的體積分數是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com