
 △H=-116kJ•mol-1
△H=-116kJ•mol-1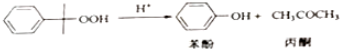 △H=-253k•mol-1
△H=-253k•mol-1
| 物質 | 相對分子質量 | 密度(g/cm-3) | 沸點/℃ |
| 異丙苯 | 120 | 0.8640 | 153 |
| 丙酮 | 58 | 0.7898 | 56.5 |
| 苯酚 | 94 | 1.0722 | 182 |
分析 用異丙苯氧化法生產苯酚和丙酮,由給予的反應信息,異丙苯與氧氣在反應器A中發生氧化反應生成 ,在蒸發器中分離出
,在蒸發器中分離出 ,未反應的異丙苯進行循環利用,
,未反應的異丙苯進行循環利用, 在分解釜中在濃硫酸作催化劑條件下分解得到
在分解釜中在濃硫酸作催化劑條件下分解得到 、
、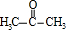 ,在中和釜中加入Z,目的是中和硫酸,且不能與苯酚反應,可以是碳酸氫鈉,然后用水洗滌,再經過蒸餾,由于丙酮的沸點低于苯酚,則T為丙酮、P為苯酚.
,在中和釜中加入Z,目的是中和硫酸,且不能與苯酚反應,可以是碳酸氫鈉,然后用水洗滌,再經過蒸餾,由于丙酮的沸點低于苯酚,則T為丙酮、P為苯酚.
(1)在反應器A發生信息中的反應①,應通入氧氣或空氣;
(2)由上述分析可知,反應①在A中發生,反應②在C中發生;
(3)濃硫酸起催化劑作用,濃硫酸腐蝕性強,會腐蝕設備,
(4)反應②的△H<0,為放熱反應,含有過氧化物,溫度過高,容易發生爆炸;
(5)加入的Z中和硫酸,且不能與苯酚反應;
(6)沸點越低越先蒸出,處于蒸餾塔的上部;
(7)由異丙苯最終得到苯酚和丙酮,原子利用率高.
解答 解:用異丙苯氧化法生產苯酚和丙酮,由給予的反應信息,異丙苯與氧氣在反應器A中發生氧化反應生成 ,在蒸發器中分離出
,在蒸發器中分離出 ,未反應的異丙苯進行循環利用,
,未反應的異丙苯進行循環利用, 在分解釜中在濃硫酸作催化劑條件下分解得到
在分解釜中在濃硫酸作催化劑條件下分解得到 、
、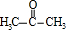 ,在中和釜中加入Z,目的是中和硫酸,且不能與苯酚反應,可以是碳酸氫鈉,然后用水洗滌,再經過蒸餾,由于丙酮的沸點低于苯酚,則T為丙酮、P為苯酚.
,在中和釜中加入Z,目的是中和硫酸,且不能與苯酚反應,可以是碳酸氫鈉,然后用水洗滌,再經過蒸餾,由于丙酮的沸點低于苯酚,則T為丙酮、P為苯酚.
(1)在反應器A發生信息中的反應①,故需要氧氣或空氣,
故答案為:氧氣或空氣;
(2)由上述分析可知,反應①在反應器中發生,即A裝置,反應②在分解釜中進行,即C裝置,
故答案為:A;C;
(3) 在濃硫酸作條件下分解得到
在濃硫酸作條件下分解得到 、
、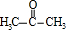 ,濃硫酸作作催化劑,濃硫酸腐蝕性強,容易腐蝕設備,
,濃硫酸作作催化劑,濃硫酸腐蝕性強,容易腐蝕設備,
故答案為:催化劑;腐蝕設備;
(4)反應②的△H<0,為放熱反應,有過氧化物存在,溫度過高會導致爆炸,反應溫度控制在50-60℃,
故答案為:放熱;溫度過高會導致爆炸;
(5)加入Z的目的是中和硫酸,且不能與苯酚反應,
a.NaOH能與硫酸、苯酚反應,故不選;
b.CaCO3為固體,且與硫酸反應生成的硫酸鈣微溶,會阻止碳酸鈣與硫酸的反應,故b不選;
c.NaHCO3能與硫酸反應,不與苯酚反應,故c選;
d.CaO能與苯酚反應,且與硫酸反應生成的硫酸鈣微溶,會阻止碳酸鈣與硫酸的反應,故d不選;
故選:c;
(6)由于丙酮的沸點低于苯酚,沸點越低越先蒸出,處于蒸餾塔的上部,則T為丙酮、P為苯酚,
故答案為:丙酮;苯酚;丙酮的沸點低于苯酚;
(7)由異丙苯最終得到苯酚和丙酮,整個過程原子利用率高,
故答案為:原子利用率高.
點評 本題考查有機物的制備實驗方案,涉及對化學工藝流程、裝置及試劑的分析評價等,關鍵是根據實驗目的與給予的反應信息理解工藝流程原理,是對學生綜合能力的考查,難度中等.


 每日10分鐘口算心算速算天天練系列答案
每日10分鐘口算心算速算天天練系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
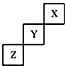
| A. | Y的單質的熔點比Z的低 | |
| B. | Y的最高正化合價為+5 | |
| C. | Z的氫化物的穩定性比Y的強 | |
| D. | X、Y、Z三種元素中,單質在常溫下均為氣態 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 一般具有良好的絕緣性 | |
| B. | 一般比同質量金屬強度大 | |
| C. | 均不溶于水,易溶于有機溶劑 | |
| D. | 有的高分子材料具有耐化學腐蝕、耐熱、耐磨、耐油、不透水等特點 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 晶體根據結構和性質只可分為分子晶體、原子晶體、離子晶體和金屬晶體四大類 | |
| B. | 任何晶體中都含有化學鍵,如離子鍵、共價鍵、金屬鍵、氫鍵等 | |
| C. | 含有陽離子的晶體一定是離子晶體 | |
| D. | 干冰和冰都屬于分子晶體 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
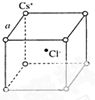 根據已學知識,請你回答下列問題:
根據已學知識,請你回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com