
將等物質的量的A、B混合于2 L的密閉容器中,發生如下反應3A(g)+B(g)  xC(g)+2D(g),經5 min后測得D的濃度為0.5 mol·L-1,c(A)∶c(B)=3∶5,用C的濃度變化表示的平均反應速率為0.1 mol·L-1·min-1。下列有關結論正確的是
xC(g)+2D(g),經5 min后測得D的濃度為0.5 mol·L-1,c(A)∶c(B)=3∶5,用C的濃度變化表示的平均反應速率為0.1 mol·L-1·min-1。下列有關結論正確的是
A.x的值為1
B.用B的濃度變化表示的平均反應速率為0.2 mol·L-1·min-1
C.反應開始前A的物質的量為3 mol
D.5 min時A的濃度為0.2 mol·L-1
 勵耘書業暑假銜接寧波出版社系列答案
勵耘書業暑假銜接寧波出版社系列答案科目:高中化學 來源:2015-2016學年吉林省高一入學摸底化學試卷(解析版) 題型:選擇題
在三個容積相同的密閉容器中分別充入Ne、H2、O2三種氣體,當它們的溫度和密度都相同時,這三種氣體的壓強(p)從大到小的順序是
A.p(Ne)>p(H2)>p(O2)
B.p(O2)>p(Ne)>p(H2)
C.p(H2)>p(O2)>p(Ne)
D.p(H2)>p(Ne)>p(O2)
查看答案和解析>>
科目:高中化學 來源:2016屆遼寧省高三上學期一模化學試卷(解析版) 題型:實驗題
硫酸銅在生產、生活中應用廣泛。某化工廠用含少量鐵的廢銅渣為原料生產膽礬的流程如下:

(1)寫出浸出時銅與稀硫酸、稀硝酸反應生成硫酸銅的化學方程式:______________。
(2)取樣檢驗是為了確認Fe3+是否除凈,你的檢驗方法是__________。
(3)濾渣c是_________。
(4)氣體a可以被循環利用,用化學方程式表示氣體a被循環利用的原理為2NO+O2===2NO2、_________。
(5)一定溫度下,硫酸銅受熱分解生成CuO、SO2氣體、SO3氣體和O2氣體,且n(SO3)∶n(SO2)=1∶2,寫出硫酸銅受熱分解的化學方程式:______________。
某同學設計了如下圖所示的實驗裝置分別測定生成的SO2、SO3氣體的質量和O2氣體的體積。此設計有不合理之處,請說明理由:______________。

查看答案和解析>>
科目:高中化學 來源:2016屆貴州省遵義市高三上學期第一次月考化學試卷(解析版) 題型:選擇題
298K時,在FeCl3溶液中加少量鋅粒后,Fe3+被還原成Fe2+ 。據此某學習小組設計如圖所示的原電池裝置。下列有關說法正確的是

A.正極電極反應為Zn-2e-=== Zn2+
B.左邊燒杯中溶液的紅色變淺
C.Pt電極上有氣泡出現
D.該電池的總反應為:3Zn+2Fe3+=== 3Zn2++2 Fe
查看答案和解析>>
科目:高中化學 來源:2016屆廣東省等六校高三第一次聯考化學試卷(解析版) 題型:選擇題
用NA表示阿伏加德羅常數的值,下列敘述正確的是
A.標準狀況下,22.4 LSO3含有NA個分子
B.6.4g氧氣和3.2g臭氧(O3)混合氣體所含有的氧原子數為0.6NA
C.過氧化鈉與CO2反應時,0.1mol過氧化鈉轉移的電子數為0.2NA
D.標準狀況下,2.24L Cl2與過量的稀FeCl2溶液反應,轉移電子總數為0.1NA
查看答案和解析>>
科目:高中化學 來源:2015-2016學年遼寧葫蘆島一中高二上期初考試化學試卷 (解析版) 題型:選擇題
下列敘述是小明做完銅、鋅原電池的實驗后得出的結論和認識,你認為正確的是
A.構成原電池正極和負極的材料必須是兩種金屬
B.由銅、鋅作電極與硫酸銅溶液組成的原電池中銅是負極
C.電子沿外導線由鋅流向銅,通過硫酸溶液被氫離子得到而放出氫氣
D.銅鋅原電池工作時,若有13 g鋅被溶解,電路中就有0.4 mol電子通過
查看答案和解析>>
科目:高中化學 來源:2015-2016學年黑龍江大慶鐵人中學高二上9月考化學試卷(解析版) 題型:選擇題
一定條件下的反應:PCl5(g)  PCl3(g)+Cl2(g)(△H>0)達到平衡后,下列情況使PCl5分解率降低的是
PCl3(g)+Cl2(g)(△H>0)達到平衡后,下列情況使PCl5分解率降低的是
A.溫度、體積不變,充入氬氣 B.體積不變,對體系加熱
C.溫度、體積不變,充入氯氣 D.溫度不變,增大容器體積
查看答案和解析>>
科目:高中化學 來源:2016屆山西省忻州市高三上學期第一次月考化學試卷(解析版) 題型:實驗題
(15分)高鐵酸鉀(K2FeO4)是一種集氧化、吸附、速凝于一體的新型多功能水處理劑。其生產流程如下:
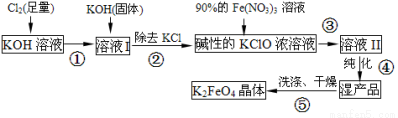

(1)配制KOH溶液時,是在每100 mL水中溶解61.6 g KOH固體(該溶液的密度為1.47 g/mL),它的物質的量濃度是 mol/L。
(2)在溶液I中加入KOH固體的目的是 (填編號)。
A.與溶液I中過量的Cl2繼續反應,生成更多的KclO
B.KOH固體溶解時會放出較多的熱量,有利于提高反應速率
C.為下一步反應提供堿性的環境
D.使副產物KClO3轉化為 KClO
(3)每制得59.4克K2FeO4,理論上消耗氧化劑的物質的量為 mol。從溶液II中分離出K2FeO4后,還得到副產品KNO3、KCl,寫出③中反應的離子方程式: 。
(4)高鐵酸鉀(K2FeO4)溶液中加入稀硫酸,溶液變為黃色,并有無色氣體產生,該反應的離子方程式是 。
(5)從環境保護的角度看,制備K2FeO4較好的方法為電解法,其裝置如圖2所示。電解過程中陽極的電極反應式為 。
查看答案和解析>>
科目:高中化學 來源:2014-2015學年廣東省佛山市高三上學期第一次月考化學試卷(解析版) 題型:選擇題
對于常溫下pH=3的乙酸溶液,下列說法正確的是
A.與等體積、pH=3的鹽酸比較,跟足量鋅粒反應產生的H2更多
B.加水稀釋到原體積的10倍后溶液pH變為4
C.加入少量乙酸鈉固體,溶液pH升高
D.溶液中粒子濃度大小關系為: c(H+)>c(CH3COOH) > c(CH3COO-)>c(OH-)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com