
2L容積不變的密閉容器中,加入1.0molA和2.2molB,進行如下反應:A(g)+2B(g)![]() C(g)+D(g),在不同溫度下,D的物質的量n(D)和時間t的關系如圖
C(g)+D(g),在不同溫度下,D的物質的量n(D)和時間t的關系如圖
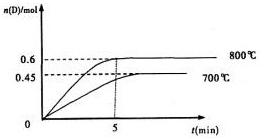
試回答下列問題:
(1)800℃時。0—5min內,以B表示的平均反應速率為 。
(2)能判斷該反應達到化學平衡狀態的標志是 。
A.容器壓強不變 B.混合氣體中c(A)不變
C.2v正(B)=v逆(D) D.c(A)=c(C)
E. 混合氣體的平均分子量不再改變 F. 混合氣體密度不變
G. A:B:C:D= 1:2:1:1
(3)利用圖中數據計算800℃時的平衡常數K= ,B的平衡轉化率為: 。該反應為 反應(填吸熱或放熱)。
(4)800℃時,另一2L容積不變的密閉容器中,測得某時刻各物質的量如下:
n(A)=2.2mol,n(B)=5.2mol,n(C)=1.8mol,n(D)=1.8mol,則此時該反應
進行(填“向正反應方向”“向逆反應方向”或“處于平衡狀態”)。
 應用題作業本系列答案
應用題作業本系列答案科目:高中化學 來源: 題型:
| c(CO2)?c(H2) |
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
| c(CO)?c(H2O) |
| 實驗組 | 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所需時間/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 3 |
| 2 | 650 | 1 | 2 | 0.8 | 1.2 | 5 |
| 3 | 950 | 1 | 2 | - | - | - |
查看答案和解析>>
科目:高中化學 來源: 題型:
| [CO]?[H2] |
| [H2O] |
| [CO]?[H2] |
| [H2O] |
| 實驗組 | 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所 需時間/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 高溫 |
| 高溫 |
| 高溫 |
| 實驗 組別 |
溫度℃ | 起始量/mol | 平衡/mol | 達平衡所 需時間/min | ||||
| H2O | CO | H2 | CO2 | H2 | CO2 | |||
| 1 | 650 | 2 | 4 | 0 | a | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0 | b | 0.4 | 1.6 | 3 |
| 高溫 |
| 組別 | 溫度 | 催化劑 | … |
| 1 | |||
| 2 | |||
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| 實驗組 | 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所需時間/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 6 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| 實驗組 | 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所需時間/min | ||
| CO | H2O | H2 | CO2 | |||
| 1 | 650 | 4 | 2 | 1.6 | 1.6 | 5 |
| 2 | 830 | 1 | 4 | 0.8 | 0.8 | 3 |
| 3 | 830 | a | b | c | d | t |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com