
| A. | 液氨中c(NH4+)與c(NH2-)的乘積總為一定值 | |
| B. | 液氨的電離達到平衡時,c(NH3)=c(NH4+)=c(NH2-) | |
| C. | 只要不加入其它物質,液氨中c(NH4+)與c(NH2-)總是相等 | |
| D. | 液氨中含有NH3、NH4+、NH2-、H2O、NH3•H2O等微粒 |
分析 A.液氨中 c(NH4+)與 c(NH2-)的乘積只與溫度有關;
B.液氨與水的電離相似,為微弱電離,所以液氨中主要存在NH3;
C.只要不破壞氨分子的電離平衡,液氨中存在c(NH4+ )=c(NH2-);
D.可逆反應中的各種微粒都共存.
解答 解:A.液氨中c(NH4+)與c(NH2-)的乘積只與溫度有關,與溶液的濃度無關,所以只要溫度一定,液氨中c(NH4+ )與c(NH2-)的乘積為定值,故A錯誤;
B.液氨與水的電離相似,為微弱電離,所以液氨中主要存在NH3,所以液氨的電離達到平衡時,c(NH3)>c(NH4+)=c(NH2-),故B錯誤;
C.根據2NH3?NH4++NH2-知,液氨電離出NH4+、NH2-的個數比為1:1,所以只要不加入其它物質,液氨中c(NH4+)與c(NH2-)總是相等,故C正確;
D.液氨電離中存在電離平衡,所以液氨中含有 NH3、NH4+、NH2-粒子,不含水分子,故D錯誤;
故選C.
點評 本題考查弱電解質的電離,為高頻考點,正確理解弱電解質電離特點是解本題關鍵,注意液氨中 c (NH4+ )與 c (NH2- )的乘積只與溫度有關,與溶液的濃度無關,易錯選項是A.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
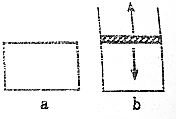 已知2N02?N2O4△H<0.將N02充入容易導熱的材料制成的容器a和b中進行反應,a的容積保持不變,b的上蓋可隨容器內氣體壓強的改變而上下移動,以保持容器內外壓強相等.當同溫同壓時,將等量的NO2充入“起始態”體積相同的容器a、b中,反應同時開始.
已知2N02?N2O4△H<0.將N02充入容易導熱的材料制成的容器a和b中進行反應,a的容積保持不變,b的上蓋可隨容器內氣體壓強的改變而上下移動,以保持容器內外壓強相等.當同溫同壓時,將等量的NO2充入“起始態”體積相同的容器a、b中,反應同時開始.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ②③⑤①⑥⑦④ | B. | ④⑥①③②⑤⑦ | C. | ④②⑤⑥①③⑦ | D. | ②⑥⑦④③⑤① |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 如圖為實驗室某濃鹽酸試劑瓶標簽上的有關數據,試根據標簽上的有關數據回答下列問題:
如圖為實驗室某濃鹽酸試劑瓶標簽上的有關數據,試根據標簽上的有關數據回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗步驟 | 實驗目的 |
| (滴定前的所有操作正確,已略去) 步驟1: ①用堿式滴定管量取20.00mL的氨水放入錐形瓶中,滴入2滴甲基橙. ②用酸式滴定管取0.1000mol/L鹽酸滴定氨水. ③當錐形瓶中的溶液由黃色變成橙色時,停止滴定,紀錄數據. ④重復滴定操作2~3次. | 測定氨水的準確濃度 |
| 步驟2:用pH計測定氨水的pH. | 測定氨水中c(OH-)濃度 |
| 步驟3:通過實驗數據計算氨水的電離常數K | |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
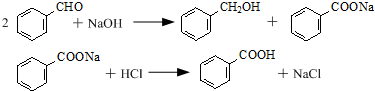
| 名稱 | 相對密度 | 熔點(℃) | 沸點(℃) | 溶解度 | |
| 水 | 乙醚 | ||||
| 苯甲醛 | 1.04 | -26 | 179.6 | 微溶 | 易溶 |
| 苯甲酸 | 1.27 | 122.1 | 249 | 25℃微溶,95℃可溶 | 易溶 |
| 苯甲醇 | 1.04 | -15.3 | 205.7 | 微溶 | 易溶 |
| 乙醚 | 0.71 | -116.3 | 34.6 | 不溶 | -- |

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com