
| A. | 此時水的轉化率為71.4% | |
| B. | 此時CO2的體積分數為20.4% | |
| C. | 若再向容器內通入5mol H2O,則達到新平衡時,H2O的轉化率升高 | |
| D. | 若從容器內移走5mol H2O,則達到新平衡時,CO的轉化率升高 |
分析 在密閉容器中將CO和水蒸氣的混合物加熱到800℃時,達到平衡狀態,設消耗一氧化碳物質的量為x:
CO+H2O?CO2+H2,
起始量(mol) 2 5 0 0
變化量(mol) x x x x
平衡量(mol)2-x 5-x x x
反應前后氣體物質的量不變,可以利用氣體物質的量代替平衡濃度計算平衡常數
平衡常數K=$\frac{{x}^{2}}{(2-x)(5-x)}$=1.
x=$\frac{10}{7}$,
結合濃度對平衡移動的影響解答該題.
解答 解:在密閉容器中將CO和水蒸氣的混合物加熱到800℃時,達到平衡狀態,設消耗一氧化碳物質的量為x:
CO+H2O?CO2+H2,
起始量(mol) 2 5 0 0
變化量(mol) x x x x
平衡量(mol)2-x 5-x x x
反應前后氣體物質的量不變,可以利用氣體物質的量代替平衡濃度計算平衡常數
平衡常數K=$\frac{{x}^{2}}{(2-x)(5-x)}$=1.
x=$\frac{10}{7}$,
A.水的轉化率為$\frac{\frac{10}{7}}{5}$×100%=28.6%,故A錯誤;
B.CO2的體積分數為$\frac{\frac{10}{7}}{7}$×100%=20.4%,故B正確;
C.加入水,雖然平衡正向移動,但轉化的比加入的少,轉化率反而降低,故C錯誤;
D.若從容器內移走5mol H2O,平衡逆向移動,則達到新平衡時,CO的轉化率降低,故D錯誤.
故選B.
點評 本題考查了化學平衡計算方法的分析應用,為高考常見題型,側重于學生的分析、計算能量的考查,題目主要是平衡常數概念的計算,題目較簡單.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯氣可以和澄清石灰水反應制造漂白粉 | |
| B. | 金屬鈉可以用來冶煉某些金屬 | |
| C. | 石灰石用于工業煉鐵和玻璃制造 | |
| D. | 二氧化硅可以用于制作光學鏡片,也可以制造光導纖維 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
| A. | 5個 | B. | 4個 | C. | 3個 | D. | 2個 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 如圖所示,圖Ⅰ是恒壓密閉容器,圖Ⅱ是恒容密閉容器.當其它條件相同時,在Ⅰ、Ⅱ中都分別加入2molX和2molY,開始時容器的體積均為VL,發生如下反應并達到平衡狀態:2X(?)+Y(?)?aZ(g).此時Ⅰ中X、Y、Z的物質的量之比為1:3:2.下列判斷不正確的是( )
如圖所示,圖Ⅰ是恒壓密閉容器,圖Ⅱ是恒容密閉容器.當其它條件相同時,在Ⅰ、Ⅱ中都分別加入2molX和2molY,開始時容器的體積均為VL,發生如下反應并達到平衡狀態:2X(?)+Y(?)?aZ(g).此時Ⅰ中X、Y、Z的物質的量之比為1:3:2.下列判斷不正確的是( )| A. | 物質Z的化學計量數a=1 | |
| B. | 若X、Y均為氣態,則在平衡時X的轉化率:Ⅰ>Ⅱ | |
| C. | 若Ⅱ中氣體的密度變化如圖Ⅲ所示,則X、Y中只有一種為氣態 | |
| D. | 若X為固態、Y為氣態,則Ⅰ、Ⅱ中從開始到平衡所需的時間:Ⅰ>Ⅱ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | A的平均反應速率為0.15mol/(L•min) | B. | B的轉化率為20% | ||
| C. | B的平衡濃度為0.5mol/L | D. | x的數值為2 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
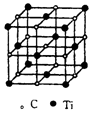 最近科學家們發現一種由鈦原子和碳原子構成的氣態團簇分子,如圖所示.頂點和面心的原子是鈦原子,棱的中心和體心的原子是碳原子,則它的化學式是( )
最近科學家們發現一種由鈦原子和碳原子構成的氣態團簇分子,如圖所示.頂點和面心的原子是鈦原子,棱的中心和體心的原子是碳原子,則它的化學式是( )| A. | TiC | B. | Ti6C7 | C. | Ti14C13 | D. | Ti13C14 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com