
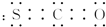 ,其分子呈直線形.
,其分子呈直線形. .
.
分析 I.(1)在基態硫原子中,其最外層電子排布為3s23p4,在周期表中第ⅡA族和第ⅤA族元素的第一電離能比同周期相鄰原子都大,據此答題;
(2)氧硫化碳(CSO)分子中碳、硫和碳、氧之間都有兩對共用電子對,碳是sp雜化,沒有孤電子對,據此判斷分子構型;
II.(3)基態V元素的價層電子排布式為3d34s2,結合泡利原、洪特規則畫出軌道表示式;
(4)采取sp2雜化的原子雜化軌道數目為3,而雜化軌道數目=σ鍵+孤對電子;V與N原子之間形成配位鍵;
(5)根據圖1可知,雜環上所有的原子可以共面,碳氧雙鍵上的所有原子共面,礬原子周圍及礬原子最多可以有5個原子共面,據此判斷;
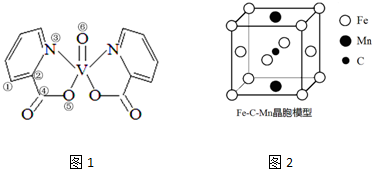
III.(6)根據晶胞結構,可知與上底面面心上的錳原子距離最近的鐵原子位于該底面的四個頂點及側面的面心,共有12個,
(7)根據晶胞的結構,利用均攤法計算晶胞中Fe、C、Mn原子數目,m=ρV計算晶胞棱長;
解答 解:I.(1)在基態硫原子中,其最外層電子排布為3s23p4,所以占據的最高能層符號為M,在周期表中第ⅡA族和第ⅤA族元素的第一電離能比同周期相鄰原子都大,所以在C、S、O、P、H中,第一電離能比同周期相鄰原子都大的元素是P,
故答案為:M;P;
(2)氧硫化碳(CSO)分子中碳、硫和碳、氧之間都有兩對共用電子對,其電子式為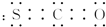 ,碳是sp雜化,沒有孤電子對,所以其分子呈直線形,
,碳是sp雜化,沒有孤電子對,所以其分子呈直線形,
故答案為: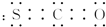 ;直線;
;直線;
II.(3)基態V元素的價層電子排布式為3d34s2,軌道表示式為 ,
,
故答案為: ;
;
(4)分子中C原子、N原子σ鍵均為3,均沒有孤電子對,雜化軌道數目均為3,均采取sp2雜化,故選①②③④,V與N原子之間形成配位鍵,1mol分子含有2mol配位鍵,即含有2NA個配位鍵,
故答案為:①②③④;2NA;
(5)根據圖1可知,雜環上所有的原子可以共面,碳氧雙鍵上的所有原子共面,礬原子周圍及礬原子最多可以有5個原子共面,所以同一平面內最多可具有的原子數是27,
故答案為:27;
III.(6)根據晶胞結構,可知與上底面面心上的錳原子距離最近的鐵原子位于該底面的四個頂點及側面的面心,共有12個,所以與一個錳(Mn)原子配位的Fe原子的數目為12,
故答案為:12;
(7)根據晶胞的結構,可知晶胞中Fe原子數為8×$\frac{1}{8}+4×\frac{1}{2}$=3,C原子數為1,Mn原子數目為$2×\frac{1}{2}$=1,根據m=ρV可知,晶胞棱長=$\root{3}{\frac{m}{ρ}}$=$\root{3}{\frac{\frac{3×56+12+55}{{N}_{A}}}{ρ}}$=$\root{3}{\frac{235}{{N}_{A}ρ}}$cm,
故答案為:$\root{3}{\frac{235}{{N}_{A}ρ}}$.
點評 本題是對物質結構與性質的考查,涉及核外電子排布、第一電離能、化學鍵、共線共面問題、晶胞結構及有關計算,掌握均攤法進行有關晶胞計算.


科目:高中化學 來源: 題型:選擇題
| A. | 微粒觀:二氧化碳是由碳原子和氧原子構成的 | |
| B. | 轉化觀:升高溫度可以將不飽和硝酸鉀溶液轉變為飽和 | |
| C. | 守恒觀:1g鎂與1g稀硫酸充分反應后所得的溶液質量為2g | |
| D. | 結構觀:金剛石和石墨由于結構中碳原子的排列方式不同,性質存在著較大的差異 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CO的摩爾質量是28g | |
| B. | 1mol CO中所含分子數為6.02×1023個 | |
| C. | 1 mol CO的質量是28 g/mol | |
| D. | 常溫常壓下,1 mol CO的體積為22.4 L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分子晶體中范德華力沒有方向性和飽和性,所以分子晶體一般都采取密堆積,但要受到分子形狀的影響 | |
| B. | 由于共價鍵的方向性和飽和性,原子晶體堆積的緊密程度大大降低 | |
| C. | 配位數就是配位鍵的數目 | |
| D. | 離子晶體一般都是非等徑球的密堆積 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鈉鋁合金 | B. | Na2O和Al2O3 | C. | 明礬和BaO | D. | MgO和SO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③ | B. | ③② | C. | ③① | D. | ②③ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 稀硫酸與氫氧化鋇溶液反應:SO42-+Ba2+═Ba SO4↓ | |
| B. | 稀H2SO4與鐵粉反應:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 石灰石溶于稀鹽酸:CO32-+2H+=+CO2↑+H2O | |
| D. | 氯化銅溶液與鐵粉反應:Cu2++Fe=Fe2++Cu |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com