
【題目】丙烯是一種重要的化工原料。可由丙烷催化脫氫制備。
主反應:①C3H8(g)=C3H6(g)+H2(g) ΔH1
副反應:②C3H8(g)=C2H4(g)+CH4(g)
③C2H4(g)+H2(g)=C2H6(g)
④C3H8(g)+H2(g)=C2H6(g)+CH4(g)
回答下列問題:
(1)已知:C3H8(g)+![]() O2(g)=C3H6(g)+H2O(g) ΔH2=-117kJ/mol
O2(g)=C3H6(g)+H2O(g) ΔH2=-117kJ/mol
H2(g)+![]() O2(g)=H2O(g) ΔH3=-242kJ/mol。反應①的ΔH1=___。
O2(g)=H2O(g) ΔH3=-242kJ/mol。反應①的ΔH1=___。
(2)某溫度下,在體積不變的密閉容器內發生反應①,起始總壓強為105Pa,平衡時總壓增加了20%。則C3H8的轉化率為___;該反應的平衡常數Kp=___Pa。若提高C3H8的平衡轉化率,可采取的措施有___(填標號)。
A.增大C3H8的濃度
B.提高溫度
C.恒容下通入惰性氣體
D.使用高效催化劑
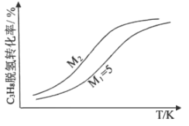
(3)工業生產中常采用恒壓下充入高溫水蒸氣的條件。如圖表示常壓下反應①C3H8的平衡轉化率與溫度及水烴比(M)的關系,M2___5(填“>”或“<”)。
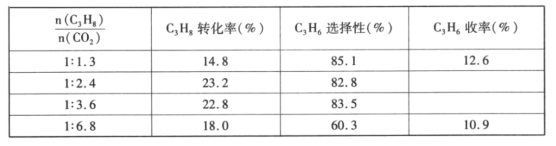
(4)已知高溫下C-C鍵斷裂反應比C-H鍵斷裂的脫氫反應容易發生,這將導致丙烯選擇性降低;同時高溫加劇催化劑表面積炭,導致催化劑迅速失活。在生產中充入CO2的作用之一是利于催化劑活性保持,其原因是___。反應氣中![]() 的配比對催化劑活性的影響如表所示。其中C3H6收率最高時
的配比對催化劑活性的影響如表所示。其中C3H6收率最高時![]() 的配比是___。
的配比是___。
【答案】+125kJ/mol 20% 5000 B > C+CO2=2CO有利于消除積炭 1:2.4
【解析】
反應C3H8(g)=C3H6(g)+H2(g)可由C3H8(g)+![]() O2(g)=C3H6(g)+H2O(g)與H2(g)+
O2(g)=C3H6(g)+H2O(g)與H2(g)+![]() O2(g)=H2O(g)相減得到;反應①反應前后氣體分子數增加的吸熱反應;恒壓下充入高溫水蒸氣,容器的體積增大,相當于減小壓強,壓強減小,平衡向氣體分子數增加的方向移動。
O2(g)=H2O(g)相減得到;反應①反應前后氣體分子數增加的吸熱反應;恒壓下充入高溫水蒸氣,容器的體積增大,相當于減小壓強,壓強減小,平衡向氣體分子數增加的方向移動。
(1)根據蓋斯定律,反應①的ΔH1=ΔH2-ΔH3=-117kJ/mol+242kJ/mol=+125kJ/mol。
(2)根據反應方程式,反應后增加的壓強與反應生成的C3H6、H2的壓強及反應了的C3H8的壓強相等,故C3H8的轉化率為20%;平衡時C3H6、H2壓強為20%![]() 105 Pa =2
105 Pa =2![]() 104 Pa,平衡時C3H8的壓強為105Pa-20%
104 Pa,平衡時C3H8的壓強為105Pa-20%![]() 105 Pa=8
105 Pa=8![]() 104 Pa,則平衡常數Kp=
104 Pa,則平衡常數Kp=![]() ;要提高C3H8的平衡轉化率,則平衡正向移動,該反應為吸熱反應,則提高溫度,C3H8的平衡轉化率增大;增大C3H8的濃度平衡雖正向移動但C3H8的平衡轉化率減小,故答案選B。
;要提高C3H8的平衡轉化率,則平衡正向移動,該反應為吸熱反應,則提高溫度,C3H8的平衡轉化率增大;增大C3H8的濃度平衡雖正向移動但C3H8的平衡轉化率減小,故答案選B。
(3) 恒壓下充入高溫水蒸氣,容器的體積增大,平衡正向移動,則溫度一定時,水烴比越大,C3H8的平衡轉化率越高,故M2>5。
(4)高溫會加劇催化劑表面積炭,導致催化劑迅速失活,加入CO2發生反應C+CO2=2CO,有利于消除積炭,保持催化劑活性;由表格數據可知,![]() 的配比是1:2.4,C3H6的選擇性大,C3H8轉化率高,則C3H6收率最高。
的配比是1:2.4,C3H6的選擇性大,C3H8轉化率高,則C3H6收率最高。


 奪冠訓練單元期末沖刺100分系列答案
奪冠訓練單元期末沖刺100分系列答案 新思維小冠軍100分作業本系列答案
新思維小冠軍100分作業本系列答案 名師指導一卷通系列答案
名師指導一卷通系列答案科目:高中化學 來源: 題型:
【題目】金幣、銀幣、銅幣等金屬貨幣在我國歷史上曾經發揮過重要作用,其中一些被收藏愛好者珍藏。在一位收藏家的家中,陳列了很多金屬貨幣。其中有些貨幣表面是黑色的,且有少量的綠色銹狀物。回答下列問題:
(1)該收藏家的這些貨幣是__________幣;
(2)貨幣表面的黑色物質是__________,形成這種物質的化學方程式為_____________;
(3)貨幣表面的綠色物質是____________,形成這種物質的化學方程式為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】異丁香酚可作為合成香料的原料,其結構簡式如下圖所示。下列有關敘述正確的是( )
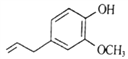
A. 異丁香酚屬于芳香族化合物,分子式為C10H14O2
B. 該物質能使酸性高錳酸鉀溶液褪色
C. 1mol該物質與足量H2發生加成反應,最多可消耗1molH2
D. 分子中所有原子有可能在同一平面上
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】科學家合成出了一種高效電解質(如圖所示),其中X、Y、Z、W、Q均為短周期元素,且原子序數依次增大,Z和Q位于同一主族,Y和W的原子序數之和與Q相等。下列說法正確的是
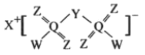
A.Q的氧化物對應水化物為強酸
B.該電解質陰離子中所有原子均滿足8電子穩定結構
C.元素非金屬性強弱的順序為W>Y>Z
D.X和Z形成的化合物溶于水呈堿性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】微信熱傳的“苯寶寶表情包”可看作是由苯衍生的物質配以相應文字形成的(如圖)。下列說法正確的是

A. 化合物(A)不能與乙醇發生反應
B. 化合物(B)分子式為C6H6Cl6
C. 化合物(B)可通過苯與Cl2發生加成反應制得
D. 1mol化合物(A)可與3molH2發生加成反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙醇能發生如下反應:
①CH3CH2OH+3O2![]() 2CO2+3H2O;
2CO2+3H2O;
②2Cu+O2 ![]() 2CuO,CH3CH2OH+CuO
2CuO,CH3CH2OH+CuO![]() CH3CHO+H2O+Cu。
CH3CHO+H2O+Cu。
由以上反應不能得出的結論是
A. 由反應①②可知,條件不同,乙醇與O2反應的產物不同
B. 由反應②可知,Cu是乙醇氧化生成乙醛的催化劑
C. 由反應①可知,乙醇燃燒時,碳碳鍵、碳氫鍵、氫氧鍵均斷裂
D. 由反應②可知,乙醇氧化為乙醛時,只斷開氫氧鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在石蠟油的分解實驗中,產物可使酸性高錳酸鉀溶液褪色,也可以使溴的四氯化碳溶液褪色。

請你根據實驗過程及現象探討下列問題:
(1)碎瓷片的作用是__。
(2)分解產物中的氣體是否都是烷烴__,你的依據是__。
(3)證明石蠟油分解產物中含有碳、氫元素的方法是__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】 CO2的資源化利用一直是化學家們關注的重要課題,中科院大連化學物理研究所設計了一種新型多功能復合催化劑,成功地實現了CO2直接加氫制取高辛烷值汽油:![]() (反應①),該研究成果被評價為“CO2催化轉化領域的突破性進展”。
(反應①),該研究成果被評價為“CO2催化轉化領域的突破性進展”。
(1)已知氫氣的燃燒熱為![]() ,若要利用
,若要利用![]() 的燃燒熱求a的值,則還需要知道一個反應的
的燃燒熱求a的值,則還需要知道一個反應的![]() ,該反應是________________________________。反應①在一定條件下具有自發性,則a_______________0(填“>”或“<”)。
,該反應是________________________________。反應①在一定條件下具有自發性,則a_______________0(填“>”或“<”)。
(2)向某密閉容器中按一定投料比充入![]() 、
、![]() ,控制條件使其發生反應:
,控制條件使其發生反應:![]() 。測得
。測得![]() 的平衡轉化率與溫度、壓強之間的關系如圖1所示:
的平衡轉化率與溫度、壓強之間的關系如圖1所示:
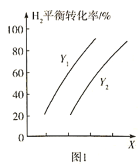
則X表示______________,![]() ___________
___________![]() (填“>”或“<”)。欲提高
(填“>”或“<”)。欲提高![]() 的平衡轉化率并提高單位時間內
的平衡轉化率并提高單位時間內![]() 的產量,可采取的措施是______________________(填兩種)。
的產量,可采取的措施是______________________(填兩種)。
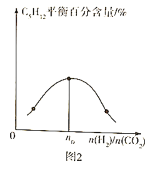
(3)控制一定溫度、催化劑,按不同投料比![]() 將反應物通入到某密閉容器中,測得平衡時
將反應物通入到某密閉容器中,測得平衡時![]() 的百分含量與投料比之間的關系如圖2所示,則
的百分含量與投料比之間的關系如圖2所示,則![]() ____________。
____________。
(4)在釕-銠雙金屬催化劑的作用下,CH3OH、CO2、H2可高效地轉化為乙酸,反應方程式為![]() 。一定溫度下,向某剛性容器中通入等物質的量的三種原料氣,測得體系中的總壓強與時間的關系如下表所示:
。一定溫度下,向某剛性容器中通入等物質的量的三種原料氣,測得體系中的總壓強與時間的關系如下表所示:
t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
p/kPa | 3 | 2.7 | 2.5 | 2.35 | 2.26 | 2.2 | 2.2 |
則反應開始到達到平衡的過程中,![]() ______________
______________![]() ______________
______________![]() 。
。
(5)碳捕捉技術的發展也有利于CO2在資源應用方面得到充分利用。常溫下,若某次用NaOH溶液捕捉空氣中的CO2所得溶液的pH=10,并測得溶液中![]() ,則
,則![]() _____________
_____________![]() 。
。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國擁有自主知識產權的銣(Rb)原子鐘,每3000萬年誤差僅1秒。Rb是第五周期第ⅠA族元素,下列關于37Rb的說法正確的是( )
A.元素的金屬性:K>Rb
B.中子數為50的Rb的核素:![]() Rb
Rb
C.與同周期元素53I的原子半徑比:Rb<I
D.最高價氧化物對應的水化物的堿性:KOH<RbOH
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com