
【題目】在一個容積為500mL的密閉容器中,充入5mol H2和2 mol CO。在一定溫度和一定壓強下,發生如下反應在:2H2(g) +CO(g)![]() CH3OH(g),經過5min后達到平衡狀態。若此時測得容器內壓強是起始時的
CH3OH(g),經過5min后達到平衡狀態。若此時測得容器內壓強是起始時的![]() ,求:(1)以H2的濃度變化表示的該反應的速率(2)達平衡時CO的轉化率(3)該溫度下的平衡常數K
,求:(1)以H2的濃度變化表示的該反應的速率(2)達平衡時CO的轉化率(3)該溫度下的平衡常數K
科目:高中化學 來源: 題型:
【題目】化合物X是一種香料,可采用乙烯與甲苯為主要原料,按下列路線合成:
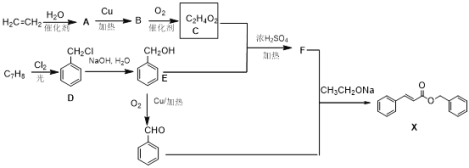
已知:RCOOH+R′OH![]() RCOOR′+H2O
RCOOR′+H2O
(1)A的化學名稱______________,X中含有的官能團名稱_______;
(2)X的分子式_______________,F的結構簡式_______________;
(3)乙烯到A的反應類型___________,由A 生成B的化學方程式_________,C和E反應生成F的化學方程式__________;
(4)除D外,D的同分異構體芳香族化合物有(不考慮立體異構)______種,其中核磁共振有三組峰,且峰面積之比為3:2:2的結構式為______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將3 mol A和1 mol B混合于一體積可變的密閉容器P中,以此時的溫度、壓強和體積作為起始條件,發生如下反應:
3A(g)+B(g) ![]() 2C(g)+D(g),達到平衡時C的濃度為w mol/L。回答下列問題:
2C(g)+D(g),達到平衡時C的濃度為w mol/L。回答下列問題:
(1)保持溫度和壓強不變,按下列四種配比充入容器P中有關物質,平衡后C的濃度仍為w mol/L的是_____。
A.6 mol A+2 mol B B.3 mol A+1 mol B+2 mol C
C.2 mol C+1 mol B+1 mol D D.1 mol C+2 mol D
(2)保持原起始溫度和體積不變,要使平衡后C的濃度仍為w mol/L,應按下列哪種配比向容器Q中充入有關物質_____。
A.3 mol A+1 mol B B.4 mol C+2 mol D
C.1.5 mol A+0.5 mol B+1 mol C+0.5 mol D D.無法判斷
(3)保持原起始溫度和體積不變,若仍按3 mol A和1 mol B配比在容器Q中發生反應,則平衡時C的濃度和w mol/L的關系是____。
A.大于w mol/L B.小于w mol/L C.等于w mol/L D.無法比較
(4)將2 mol C和2 mol D按起始溫度和壓強充入容器Q中,保持溫度和體積不變,平衡時C的濃度為v mol/L,則v和w的關系是_____。
A.v>w B.v<w C.v=w D.無法比較
(5)維持原起始溫度和體積不變,按下列哪種配比充入容器Q可使平衡時C的濃度為v mol/L ____。
A.1 mol C+0.5 mol D B.3 mol A+2 mol B
C.3 mol A+1 mol B+1 mol D D.以上均不能滿足條件
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將1 mol I2(g)和2 mol H2置于某2L密閉容器中,在一定溫度下發生反應:I2(g)+H2(g) ![]() 2HI(g)ΔH<0,并達到平衡。HI的體積分數w(HI)隨時間t變化如圖曲線(Ⅰ)所示。
2HI(g)ΔH<0,并達到平衡。HI的體積分數w(HI)隨時間t變化如圖曲線(Ⅰ)所示。
(1)達到平衡時,I2(g)的物質的量濃度為______________mol·L-1。
(2)若改變反應條件,在甲條件下w(HI)的變化如圖曲線(Ⅱ)所示,在乙條件下w(HI)的變化如圖曲線(Ⅲ)所示。則甲條件可能是______________,乙條件可能是______________。(填入下列條件的序號)
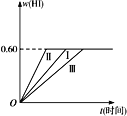
①恒容條件下,升高溫度 ②恒容條件下,降低溫度 ③恒溫條件下,縮小反應容器體積 ④恒溫條件下,擴大反應容器體積 ⑤恒溫恒容條件下,加入適當催化劑
(3)若保持溫度不變,在另一相同的2L密閉容器中加入a mol I2(g),b mol H2(g)和c molHI(g)(a、b、c均大于0),發生反應,達平衡時,HI的體積分數仍為0.60,則a、b、c的關系是_____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲醇是重要的化工原料,又可稱為燃料。利用合成氣(主要成分為CO、CO2和H2)在催化劑的作用下合成甲醇,發生的主反應如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g)![]() CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
回答下列問題:
(1)已知△H1=-99kJ·mol-1 ,△H3=+41kJ·mol-1,則△H2=_________kJ·mol-1。
(2)反應①的化學平衡常數K的表達式為____________;圖1中能正確反映平衡常數K隨溫度變化關系的曲線為_______(填曲線標記字母),其判斷理由是________。
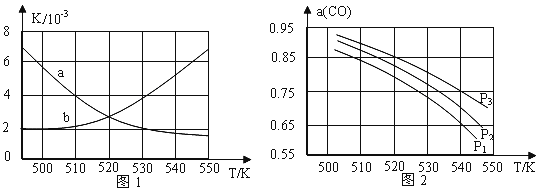
(3)若開始各氣體的物質的量一定時,體系中的CO平衡轉化率(α)與溫度和壓強的關系如圖2所示。則α(CO)值隨溫度升高而_____(填“增大”或“減小”);圖2中的壓強由大到小為_____________,其判斷理由是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物F是一種重要有機物,其合成路線如下:
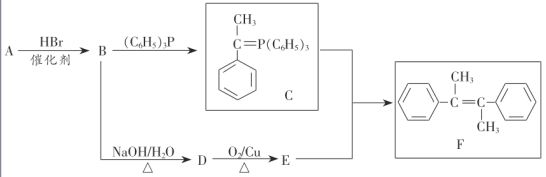
已知:①烴A的相對分子質量為104;
②E的核磁共振氫譜有4組吸收峰;
③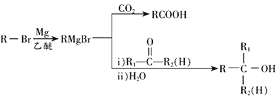
請回答以下問題:
⑴A的化學名稱為________,E中官能團名稱是________
⑵B→D的反應類型為________,F中共平面的碳原子最多有________個.
⑶D→E的化學方程式為________
⑷上述流程中可能得到一種與E互為同分異構體的副產物,該物質的結構簡式為________
⑸D的一種同分異構體X,能與FeCl3溶液發生顯色反應,則X共有________種.![]() 不含立體異構
不含立體異構![]()
⑹參照題干有關信息,設計一條由溴苯和乙醇為原料制備A的合成路線:________(其他無機試劑和溶劑任選)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:H2SO3的電離常數K1=1.3×10-2,K2=6.2×10-8,將amolL-1NaHSO3溶液與bmolL-1NaOH溶液等體積混合(a>0,b>0),混合所得溶液中微粒的物質的量濃度關系正確的是
A.a=b時:c(OH-)=c(H+)+c(HSO3-)
B.a=3b時:c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
C.當溶液pH=7時:c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)=c(H+)
D.若4c(Na+)=5c(SO32-)+5c(HSO3-)+5c(H2SO3),則a=4b
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】芳香烴A是基本有機化工原料,由A制備高分子E和醫藥中間體K的合成路線(部分反應條件略去)如下圖所示:
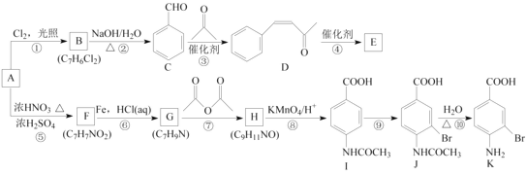
己知:①![]() ;
;
②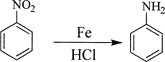
回答下列問題:
(1)A的名稱是________,I含有官能團的名稱是________。
(2)反應⑦的作用是________,⑩的反應類型是________。
(3)寫出反應②的化學方程式:____________________________________________________。
(4)D分子中最多有________個原子共平面。E的結構簡式為________。
(5)寫出一種同時符合下列條件的F的同分異構體的結構簡式:________。
①苯環上只有兩種不同化學環境的氫原子;
②既能與銀氨溶液反應又能與NaOH溶液反應。
(6)將由D為起始原料制備![]() 的合成路線補充完整。
的合成路線補充完整。
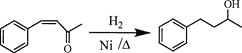 ________(無機試劑及溶劑任選)。
________(無機試劑及溶劑任選)。
合成路線流程圖示例如下:
CH3CHO![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在恒容密閉容器中發生反應:![]() ,正反應為吸熱反應,H2O和H2的物質的量隨時間的變化如圖所示,2min時僅改變一個條件,則改變的條件是( )
,正反應為吸熱反應,H2O和H2的物質的量隨時間的變化如圖所示,2min時僅改變一個條件,則改變的條件是( )
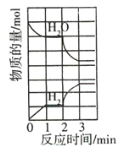
A.減小n(H2O)B.增大n(H2)
C.增大壓強(減小容器體積)D.升高溫度
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com