
【題目】如圖是一個化學過程的示意圖.請回答下列問題: 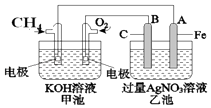
(1)甲池是裝置(填“原電池”或“電解池”),B(石墨)電極的名稱 是 .
(2)寫出電極反應式: 通入CH4的電極;A(Fe)電極 .
(3)甲池中反應的離子方程式為 .
(4)乙池中反應的化學方程式為 .
(5)若乙池溶液體積為500mL,且忽略電解過程中溶液體積的變化,當乙池中 A極的質量增加5.40g時: ①甲池中理論上消耗O2體積為(標準狀況下);
②乙池中所得溶液的pH= .
【答案】
(1)原電池;陽極
(2)CH4+10OH﹣﹣8e﹣═CO32﹣+7H2O; Ag++e﹣═Ag
(3)CH4+2O2+2OH﹣═CO32﹣+3H2O
(4)4AgNO3+2H2O ![]() 4Ag+O2↑+4HNO3
4Ag+O2↑+4HNO3
(5)280mL;1
【解析】解:(1)根據反應方程式知,甲裝置是一個燃料電池,所以甲是把化學能轉變為電能的裝置,是原電池;乙有外加電源,所以是電解池,
B(石墨)與原電池的正極相連,所以電極的名稱是陽極,所以答案是:原電池;陽極;(2)通入CH4的電極是原電池的負極發生氧化反應,電極反應式為:CH4+10OH﹣﹣8e﹣═CO32﹣+7H2O;A(Fe)電極是電解池的陰極銀離子發生還原反應,電極反應式為:Ag++e﹣═Ag,所以答案是:CH4+10OH﹣﹣8e﹣═CO32﹣+7H2O;Ag++e﹣═Ag;(3)甲池中反應的離子方程式為CH4+2O2+2OH﹣═CO32﹣+3H2O,所以答案是:CH4+2O2+2OH﹣═CO32﹣+3H2O;(4)乙池相當于惰性電極電解硝酸銀溶液,化學方程式為:4AgNO3+2H2O ![]() 4Ag+O2↑+4HNO3,所以答案是:4AgNO3+2H2O
4Ag+O2↑+4HNO3,所以答案是:4AgNO3+2H2O ![]() 4Ag+O2↑+4HNO3;(5)①鐵電極上析出銀,A(Fe)極的質量增加5.40g時轉移電子的物質的量=
4Ag+O2↑+4HNO3;(5)①鐵電極上析出銀,A(Fe)極的質量增加5.40g時轉移電子的物質的量= ![]() ×1=0.05mol,根據串聯電路中轉移電子相等,得甲池中理論上消耗O2體積=
×1=0.05mol,根據串聯電路中轉移電子相等,得甲池中理論上消耗O2體積= ![]() =280mL,所以答案是:280mL;
=280mL,所以答案是:280mL;
②4HNO3~轉移4mol的電子,所以轉移電子的物質的量為:0.05mol,所以生成硝酸的物質的量為0.05mol,c= ![]() =
= ![]() =0.1mol/L,所以PH=1,所以答案是:1.
=0.1mol/L,所以PH=1,所以答案是:1.


 53隨堂測系列答案
53隨堂測系列答案科目:高中化學 來源: 題型:
【題目】酸、堿、鹽均屬于電解質,它們的水溶液中存在各種平衡.
(1)氨水是中學常見的堿溶液 ①下列事實可證明NH3H2O是弱堿的是(填字母序號).
A.常溫下,0.1molL﹣1氨水pH為11
B.氨水能跟氯化亞鐵溶液反應生成氫氧化亞鐵
C.常溫下,0.1molL﹣1氯化銨溶液的pH為5
D. 銨鹽受熱易分解
②下列方法中,可以使氨水電離程度增大的是(填字母序號).
A.加入少量氯化鐵固體 B.通入氨氣
C.加入少量氯化銨固體 D.加水稀釋
(2)鹽酸和醋酸是中學常見酸 用0.1molL﹣1NaOH溶液分別滴定體積均為20.00mL、濃度均為0.1molL﹣1的鹽酸和醋酸溶液,得到滴定過程中溶液pH隨加入NaOH溶液體積而變化的兩條滴定曲線.
①滴定醋酸的曲線是(填“I”或“II”).
②滴定開始前,三種溶液中由水電離出的c(H+)最大的是 .
③V1和V2的關系:V1V2(填“>”、“=”或“<”).
④M點對應的溶液中,各離子的物質的量濃度由大到小的順序是 .
(3)常溫下將0.2mol/L HCl溶液與0.2mol/L氨水溶液等體積混合(忽略混合后溶液體積的變化),測得混合溶液的pH=6,求混合溶液中下列算式的精確計算結果(填具體數字): c(H+)﹣c(NH3﹒H2O)=mol/L.
(4)銨鹽和氯化銀是中學常見鹽 ①0.1molL﹣1的(NH4)2Fe(SO4)2溶液,與同濃度的(NH4)2SO4溶液相比較(填溶質的化學式)溶液中NH4+的濃度更大,其原因是
②含有足量AgCl固體的飽和溶液,AgCl在溶液中存在如下平衡:
AgCl(s)Ag+(aq)+Cl﹣(aq)
在25℃時,AgCl的Ksp=1.8×10﹣10 . 現將足量AgCl分別放入下列液體中:
①100mL蒸餾水
②100mL 0.3molL﹣1AgNO3溶液
③100mL 0.1molL﹣1 MgCl2溶液
充分攪拌后冷卻到相同溫度,Ag+濃度由大到小的順序為(填序號).
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、W、Q是原子序數依次增大的5種短周期主族元素。如圖轉化關系中所涉及的物質含有這五種元素的單質或化合物,其中反應①是置換反應,A為金屬單質,D為非金屬單質,原子核外最外層電子數D是A的2倍,F是一種最高價含氧酸,遇光或熱會分解。下列說法正確的是
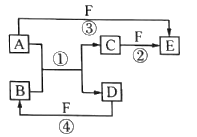
A. 簡單氫化物的沸點:Z>W
B. Y與W形成的化合物都可以和氫氧化鈉溶液反應
C. Y、Z、W元素中,原子半徑最小的是W
D. W與Q組成的常見化合物中可能含有極性共價鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】銅、磷及其化合物是非常重要的物質。
(1)Cu+的電子排布式____;
(2)在硫酸銅溶液中加入過量KCN,生成配合物[Cu(CN)4]2-。[Cu(CN)4]2-的配體為____,[Cu(CN)4]2-中C的雜化方式為____,則1個[Cu(CN)4]2-中含有的σ鍵的數目為____個;
(3)鋰—磷酸氧銅電池正極的活性物質是Cu4O(PO4)2,不溶于水,可通過Na3PO4、CuSO4和NH3·H2O反應制取。制取Cu4O(PO4)2的化學方程式為____;
(4)PCl5中P-Cl鍵長有198pm和206pm兩種。PCl5是非極性分子,可作為導電熔體,其原理為PCl5電離為一個陰離子和一個陽離子,其中陰離子為正八面體,陽離子為正四面體,寫出一種陽離子的等電子體的化學式____,PCl5的立體構型為____;
(5)金屬銅屬于面心立方晶體,銅的密度為ag·cm3,NA表示阿伏伽德羅常數,則銅的配位數____,銅的金屬半徑為___pm。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用如圖所示的裝置進行電解.通電一會兒,發現用NaCl溶液濕潤的淀粉KI試紙的C端變為藍色. 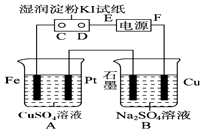
(1)E為電源的極,Fe為極.
(2)A中發生反應的離子方程式為 , B中發生反應的化學方程式為 .
(3)在B中觀察到的現象是
(4)若此電源為鉛蓄電池,電池總反應式為: Pb+PbO2+4H++2SO42﹣ ![]() PbSO4+2H2O
PbSO4+2H2O
則放電時:正極的電極反應式是;充電時:陰極的電極反應式是;當外電路通過1mol電子時,理論上負極板的質量增加g,此時若要使A池中的溶液復原,應加入g的CuO固體.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NaBH4燃料電池具有理論電壓高、能量密度大等優點。已知,能量密度=電池輸出電能/燃料質量,以該燃料電池為電源電解精煉銅的裝置如圖所示。下列說法不正確的是
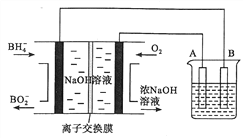
A. 離子交換膜應為陽離子交換膜,Na+由左極室向右極室遷移
B. 該燃料電池的負極反應式為BH4-+8OH--8e-=B![]() +6H2O
+6H2O
C. 若NaBH4 燃料電池的電壓為U伏,則此電池的能量密度為2.03×104UkJ·kg-1
D. 每消耗2.24 L O2(標準狀況)時,A電極的質量減輕12.8 g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知化學反應A2(g)+B2(g)═2AB(g)的能量變化如圖所示,判斷下列敘述中正確的是( ) 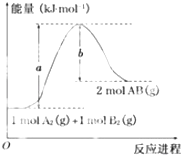
A.每生成2分子AB吸收b kJ熱量
B.斷裂1mol A﹣A和1mol B﹣B鍵,放出a kJ能量
C.該反應中反應物的總能量高于生成物的總能量
D.該反應熱△H=+(a﹣b)kJmol﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應A(g)+3B(g) =2C(g)+2D(g)在四種不同情況下的反應速率分別為:①v(A)=0.45 mol·L-1·s-1、②v(B)=0.6 mol·L-1·s-1、③v(C)=0.4 mol·L-1·s-1、④v(D)=0.45 mol·L-1·s-1,該反應進行的快慢順序為
A. ①>③=②>④ B. ①>②=③>④
C. ②>①=④>③ D. ①>④>②=③
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com