
【題目】2018年11月《物理評論快報》報道了艾姆斯實驗室制造的包含鈣、鉀、鐵和砷以及少量鎳的CaK(Fe1-xNix)4As4新型化合物材料,呈現出被稱為刺猬自旋新磁態。有助于更好理解磁性與非常規超導性之間的聯系。回答下列問題:
(1)基態鎳原子的電子排布式為[Ar]______________;上述材料中所含元素的基態原子中,未成對電子數最多的是___________(填元素符號)。
(2)鐵及其離子易形成配離子,如[Fe(CN)6]3-、[Fe(CN)6]4-、Fe(CO)5等。所包括的非金屬元素中第一電離能最大的是__________(填元素符號);
(3)K3AsO3可用于碘的微量分析。
①K+的焰色反應呈紫色,金屬元素能產生焰色實驗的微觀原因為____________。
②AsO33-的立體構型為________,寫出一種與其互為等電子體的分子________
(填化學式)。
(4)Ni與Ca處于同一周期,且核外最外層電子構型相同,但金屬Ni的熔點和沸點均比金屬Ca的高,其原因為___________。
(5)①金屬鎳的原子堆積方式如圖所示,則金屬鎳晶胞俯視圖為____。

A.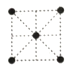 B.
B. C.
C. D.
D.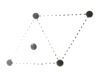
②某砷鎳合金的晶胞如圖所示,設阿伏加德羅常數的值為NA,該晶體的密度ρ=_____g·cm-3。
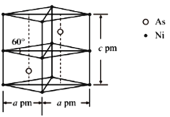
【答案】3d84s2 Fe N 電子從較高能級的激發態躍遷到較低能級的激發態乃至基態時,會以光的形式釋放能量 三角錐形 PCl3、PBr3、NF3、NCl3等(答一種即可) Ni的原子半徑較小,價層電子數目較多,金屬鍵較強 C ![]()
【解析】
(1)鎳是28號元素,根據構造原理寫出電子排布式,根據鈣、鉀、鐵和砷以及鎳的核外電子排布式,找出未成對電子數最多的;
(2)非金屬元素C、N、O、根據它們在周期表的位置,N的核外電子排布中,2p軌道為半充滿,N的第一電離能高于同周期相鄰的元素,判斷第一電離能的大小;
(3).①電子從較高能級的激發態躍遷到較低能級的激發態乃至基態時,會以光的形式釋放能量;
②AsO33-中As原子孤電子對數=![]() =1,價層電子對數=1+3=4,在VSEPR模型基礎上忽略孤對電子可得微粒空間構型;互為等電子體的微粒的原子總數相等、價電子總數也相等;
=1,價層電子對數=1+3=4,在VSEPR模型基礎上忽略孤對電子可得微粒空間構型;互為等電子體的微粒的原子總數相等、價電子總數也相等;
(4).金屬晶體熔沸點的高低與金屬鍵的強弱有關,金屬鍵的強弱與價層電子數目和金屬原子的半徑有關;
(5) ①鎳的原子堆積方式為面心立方最密堆積;②由晶胞結構可知,每個晶胞中含有2個Ni原子和2個As原子,計算晶胞的質量,晶體密度=晶胞質量÷晶胞體積。
(1)鎳是28號元素,根據構造原理寫出簡化的電子排布式[Ar] 3d84s2,
鈣、鉀、鐵和砷以及鎳的核外電子排布式:[Ar]4s2、[Ar]4s1、[Ar]3d64s2、[Ar]3d104s24p3、[Ar]3d84s2,未成對電子數分別為0、1、4、3、2,基態原子中,未成對電子數最多的是鐵,
故答案為:[Ar] 3d84s2;Fe;
(2)同周期從左到右,第一電離能呈現增大的趨勢,由于氮原子的2p能級為半充滿,較穩定,故C、N、O的第一電離能大小順序為C<O<N,第一電離能較大的元素為N,
故答案為:N;
(3)①金屬元素產生焰色反應的微觀原因為:電子從較高能級的激發態躍遷到較低能級的激發態乃至基態 時,會以光的形式釋放能量,產生焰色反應,
故答案為:電子從較高能級的激發態躍遷到較低能級的激發態乃至基態時,會以光的形式釋放能量;
②AsO33中As原子孤電子對數=![]() =1,價層電子對數=1+3=4,在VSEPR模型基礎上忽略孤對電子可得微粒空間構型為三角錐形;根據價電子總數和原子總數(氫等輕原子不計在內)相同的分子、離子或基團互為等電子體可知,用Cl原子替代O原子、1個單位負電荷可得與AsO33互 為等電子體的分子有PCl3等,進一步替換可得PBr3、NF3、NCl3等,
=1,價層電子對數=1+3=4,在VSEPR模型基礎上忽略孤對電子可得微粒空間構型為三角錐形;根據價電子總數和原子總數(氫等輕原子不計在內)相同的分子、離子或基團互為等電子體可知,用Cl原子替代O原子、1個單位負電荷可得與AsO33互 為等電子體的分子有PCl3等,進一步替換可得PBr3、NF3、NCl3等,
故答案為:三角錐形;PCl3、PBr3、NF3、NCl3等;
(4)Ca、Ni都屬于金屬晶體,Ni的原子半徑較小,價層電子數目較多,金屬鍵較強,故金屬Ni的熔點和沸點均比金屬Ca的高,
故答案為:Ni的原子半徑較小,價層電子數目較多,金屬鍵較強;
(5) ①鎳的原子堆積方式為面心立方最密堆積,故金屬鎳晶胞俯視圖為C,
答案為C;
②由晶胞結構可知,每個晶胞中含有Ni原子數目=8×![]() +4×
+4×![]() =2,含有2個As原子,晶胞的質量=2×
=2,含有2個As原子,晶胞的質量=2×![]() g,晶胞的體積V=a×10-10cm×a×10-10cm×
g,晶胞的體積V=a×10-10cm×a×10-10cm×![]() ×c×10-10cm=
×c×10-10cm=![]() ×10-30cm3,故晶胞的密度ρ=
×10-30cm3,故晶胞的密度ρ=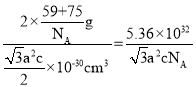 g·cm-3,
g·cm-3,
故答案為:![]() 。
。


 培優三好生系列答案
培優三好生系列答案 優化作業上海科技文獻出版社系列答案
優化作業上海科技文獻出版社系列答案科目:高中化學 來源: 題型:
【題目】氰化鈉![]() 是重要的化工原料,易溶于水,易水解生成氰化氫,劇毒物質。常用于電鍍、冶金、有機合成醫藥、絡合劑和掩蔽劑。
是重要的化工原料,易溶于水,易水解生成氰化氫,劇毒物質。常用于電鍍、冶金、有機合成醫藥、絡合劑和掩蔽劑。
![]() 裝氰化鈉
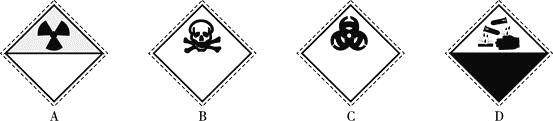
裝氰化鈉![]() 試劑瓶的標簽上應印有下列警示標記中的________
試劑瓶的標簽上應印有下列警示標記中的________![]() 填序號
填序號![]() 。
。
![]() 實驗室用NaCN固體配制NaCN溶液時,為避免其水解,應先將其溶于______________濃溶液,再用蒸餾水稀釋。
實驗室用NaCN固體配制NaCN溶液時,為避免其水解,應先將其溶于______________濃溶液,再用蒸餾水稀釋。
![]() 泄漏時用雙氧水處理以減輕環境污染,處理后生成一種酸式鹽和一種能使濕潤的紅色石蕊試紙變藍的氣體,該反應的離子方程式是__________________________________________。
泄漏時用雙氧水處理以減輕環境污染,處理后生成一種酸式鹽和一種能使濕潤的紅色石蕊試紙變藍的氣體,該反應的離子方程式是__________________________________________。
![]() 化學興趣小組利用:2NH
化學興趣小組利用:2NH![]() 反應原理制備NaCN并檢測其純度。
反應原理制備NaCN并檢測其純度。
實驗一:制備NaCN裝置如圖所示
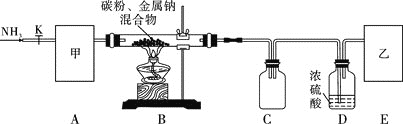
![]() 裝置C的作用是____________。甲可選取下列裝置中的________
裝置C的作用是____________。甲可選取下列裝置中的________![]() 填序號
填序號![]() 。
。

![]() 安裝好實驗儀器,檢查裝置氣密性,取一定量的碳粉與金屬鈉混合,放入硬質玻璃管內;接下來的操作正確的是________
安裝好實驗儀器,檢查裝置氣密性,取一定量的碳粉與金屬鈉混合,放入硬質玻璃管內;接下來的操作正確的是________![]() 填序號
填序號![]() 。
。
A.先打開活塞K,緩緩通入一段時間氨氣后再加熱硬質玻璃管
B.先加熱硬質玻璃管,再打開活塞K,緩緩通入氨氣
C.打開活塞K,一邊緩緩通入氨氣,同時加熱硬質玻璃管
![]() 上述裝置中乙處還需補充的實驗儀器或裝置有__________________。
上述裝置中乙處還需補充的實驗儀器或裝置有__________________。
實驗二:測定產品中氰化鈉的含量
![]() 已知: Ag
已知: Ag![]() ,Ag
,Ag![]() ,AgI呈黃色,且CN
,AgI呈黃色,且CN![]() 優先與Ag
優先與Ag![]() 反應。取制備好的產品
反應。取制備好的產品![]() ,配成
,配成![]() 溶液,取
溶液,取![]() 于錐形瓶中,并滴加
于錐形瓶中,并滴加![]() 滴KI溶液作指示劑,用
滴KI溶液作指示劑,用![]() 的標準AgNO
的標準AgNO![]() 溶液滴定3次,平均消耗AgNO
溶液滴定3次,平均消耗AgNO![]() 溶液的體積為
溶液的體積為![]() 。滴定終點的現象是____________________________________________________________,產品氰化鈉的純度為________
。滴定終點的現象是____________________________________________________________,產品氰化鈉的純度為________![]() 。
。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列事實不能用化學平衡移動原理解釋的是
A.收集氯氣可以用排飽和食鹽水的方法
B.在一定條件下,氫氣與碘蒸汽反應達平衡后,加壓,混合氣體顏色變深
C.可用濃氨水和氫氧化鈉固體快速制取氨氣
D.合成三氧化硫過程中使用過量的氧氣,以提高二氧化硫的轉化率
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組反應中,屬于可逆反應的一組是( )
A. 2H2O![]() 2H2↑+O2↑,2H2+O2
2H2↑+O2↑,2H2+O2![]() 2H2O
2H2O
B. NH3+CO2+H2O=NH4HCO3,NH4HCO3![]() NH3↑+H2O↑+CO2↑
NH3↑+H2O↑+CO2↑
C. H2+I2![]() 2HI,2HI
2HI,2HI![]() H2↑+I2↑
H2↑+I2↑
D. 2Ag+Br2![]() 2AgBr,2AgBr
2AgBr,2AgBr![]() 2Ag+Br2
2Ag+Br2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在溫度一定的條件下,N2(g)+ 3H2(g)![]() 2NH3(g)在密閉容器中反應并達到平衡時,混合氣體的平均摩爾質量為
2NH3(g)在密閉容器中反應并達到平衡時,混合氣體的平均摩爾質量為![]() ,N2與NH3的濃度均為c mol·L1。若將容器的體積壓縮為原來的1/2,當達到新的平衡時,下列說法中不正確的是
,N2與NH3的濃度均為c mol·L1。若將容器的體積壓縮為原來的1/2,當達到新的平衡時,下列說法中不正確的是
A.新的平衡體系中,N2的濃度小于2c mol·L1大于c mol·L1
B.新的平衡體系中,NH3的濃度小于2c mol·L1大于c mol·L1
C.新的平衡體系中,混合體的平均摩爾質量大于![]()
D.新的平衡體系中,氣體密度是原平衡體系的2倍
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】今有甲、乙、丙、丁、戊5種物質,在一定條件下,它們能按下圖方式進行轉化:
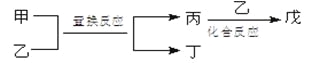
其推斷正確的是
選項 | 甲 | 乙 | 丙 | 丁 | 戊 |
A | NH3 | O2 | NO | H2O | NO2 |
B | Mg | CO2 | C | MgO | CO |
C | C | H2O | CO | H2 | HCOOH |
D | FeBr2 | Cl2 | FeCl2 | Br2 | FeCl3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】純過氧化氫(H2O2)是淡藍色的黏稠液體,可與水以任意比混合,水溶液俗稱雙氧水,為無色透明液體。實驗室常用過氧化氫制取氧氣,工業上過氧化氫是重要的氧化劑和還原劑,常用于消毒、殺菌、漂白等。某化學興趣小組的同學圍繞過氧化氫開展了調查研究與實驗,請你參與其中一起完成下列學習任務:
(1)過氧化氫中氧元素的化合價是__。
(2)實驗室中用過氧化氫制取氧氣的化學方程式為__。
(3)同學們用0.1000mol·L-1的酸性高錳酸鉀標準溶液滴定某試樣中過氧化氫的含量,反應原理為2MnO![]() +5H2O2+6H+=2Mn2++8H2O+5O2↑。
+5H2O2+6H+=2Mn2++8H2O+5O2↑。
①在該反應中,H2O2被__(填“氧化”或“還原”);酸性高錳酸鉀溶液應裝在__(填“酸式”或“堿式”)滴定管中。
②當滴入最后一滴酸性高錳酸鉀標準溶液,__即滴定到達終點。
③用移液管吸取25.00mL試樣置于錐形瓶中,重復滴定四次,每次消耗的KMnO4標準溶液體積如下表所示:
第一次 | 第二次 | 第三次 | 第四次 | |
體積(mL) | 17.10 | 18.10 | 18.00 | 17.90 |
則試樣中過氧化氫的濃度為___mol·L-1。
④若滴定前尖嘴中有氣泡,滴定后消失,則測定結果__(填“偏低”、“偏高”或“不變”)。
(4)同學們發現向滴加了酚酞的NaOH溶液中加入H2O2后,溶液中紅色消失。關于褪色原因:甲同學認為H2O2是二元弱酸,消耗了OH-使紅色消失;乙同學認為H2O2具有漂白性使溶液褪色。請設計一個簡單的實驗方案來判斷甲乙兩位同學的說法是否正確:__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,針對表中的①~⑩種元素,請用化學用語回答下列問題:
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ⑥ | ⑦ | ⑧ | |||||
3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
4 | ② | ④ |
(1)在③~⑦元素中,原子半徑最大的是__________(填元素符號);
(2)⑦元素的最高價氧化物對應的水化物與其氫化物能生成鹽M,M中含有的化學鍵類型有__________________;
(3)寫出元素①和⑧的單質在加熱條件下反應生成的化合物的電子式:_________。
(4
(5)①~⑨中元素最高價氧化物對應的水化物中酸性最強的是_____________(填物質化學式);呈兩性的氫氧化物是_________(填物質化學式),該化合物與NaOH溶液反應的離子方程式為___________。
(6)用電子式表示元素③與⑨形成化合物的過程_____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲、乙是由短周期元素組成的常見物質或微粒,在中學化學中有許多物質或微粒能滿足下列相互轉化關系:甲![]() 乙
乙![]() 甲.下列說法正確的是
甲.下列說法正確的是
A.甲有可能是![]() 也有可能是
也有可能是![]()
B.若乙為無色無味氣體,則甲一定是![]()
C.若甲是具有刺激性氣味的氣體,則甲、乙具有相同的電子數
D.若甲、乙均為離子,甲、乙兩種離子在同一溶液中一定不能大量共存
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com