
分析 ③Ba(OH)2與H2SO4反應生成硫酸鋇和水;
④Na2CO3與HCl反應生成氯化鈉、水和二氧化碳;
⑤CuSO4與NaOH溶液反應生成氫氧化銅、硫酸鈉.
解答 解:③Ba(OH)2與H2SO4反應生成硫酸鋇和水,反應的化學方程式為Ba(OH)2+H2SO4=BaSO4↓+H2O,故答案為:Ba(OH)2+H2SO4=BaSO4↓+H2O;
④Na2CO3與HCl反應生成氯化鈉、水和二氧化碳,反應的化學方程式為Na2CO3+2HCl=2NaCl+H2O+CO2↑,故答案為:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
⑤CuSO4與NaOH溶液反應生成氫氧化銅、硫酸鈉,反應的化學方程式為2NaOH+CuSO4=Cu(OH)2↓+Na2SO4,
故答案為:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.
點評 本題考查化學方程式的書寫,為高頻考點,側重于元素化合物知識的考查,注意把握相關物質的性質,難度不大.


 永乾教育寒假作業快樂假期延邊人民出版社系列答案
永乾教育寒假作業快樂假期延邊人民出版社系列答案科目:高中化學 來源: 題型:選擇題
| A. | ①②③④ | B. | ②③①④ | C. | ②①③④ | D. | ①②④③ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CO2屬于溫室氣體 | |
| B. | 太陽能電池可將太陽能轉化為電能 | |
| C. | 太陽能、風能和生物能源屬于新能源 | |
| D. | 乙醇屬不可再生能源,乙醇燃燒不會產生溫室氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ④⑤ | B. | ①② | C. | ①②③⑤ | D. | ①②③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1molC2H6中含有6 NA個共價鍵 | |
| B. | 7.8 g Na2O2中含有的陽離子數和陰離子數均為0.2NA | |
| C. | 14.0g由C2H4和C3H6組成的混合氣體原子總數為3NA | |
| D. | 5.6g金屬鐵與足量鹽酸反應時失去的電子數是0.3NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Mg | B. | Mg | C. | $\frac{M}{6.02×1{0}^{23}}$g | D. | Mg |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鍋爐水垢中的CaSO4經飽和碳酸鈉溶液浸泡可轉化為CaCO3 | |
| B. | 常溫下,在含有Ag+和Cl-的溶液中,Ag+和Cl-濃度之積是個常數 | |
| C. | 當醋酸達到電離平衡后,改變某條件電離平衡向正反應方向移動,則溶液的導電能力一定變強 | |
| D. | 將濃度為0.1 mol/L的HF溶液加水不斷稀釋,溶液$\frac{c({F}^{-})}{c({H}^{+})}$始終保持增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
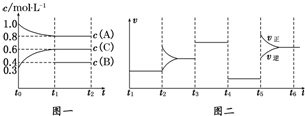
| t1~t2 | t2~t3 | t3~t4 | t4~t5 | t5~t6 |
| K1 | K2 | K3 | K4 | K5 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com