
| A. | 44.8 L氟化氫氣體分解成22.4 L的氫氣和22.4 L的氟氣吸收546.6 kJ熱量 | |
| B. | 1 mol氫氣與1 mol氟氣反應生成2 mol液態氟化氫放出的熱量大于546.6 kJ | |
| C. | 相同條件下,1 mol氫氣與1 mol氟氣的能量總和高于2 mol氟化氫氣體的能量 | |
| D. | 2 mol H-F鍵的鍵能比1 mol H-H鍵和1 mol F-F 鍵的鍵能之和大546.6 kJ |
分析 A、熱化學方程式的正逆兩個過程的焓變符號相反,數值相等;
B、液態氟化氫的能量比氣態氟化氫的能量低,根據反應熱與能量關系判斷;
C、反應物總能量大于生成物的總能量為放熱反應,反應物總能量小于生成物的總能量為吸熱反應;
D、根據化學反應的焓變和鍵能之間的關系來回答.
解答 解:A、由熱化學方程式可知44.8L即2mol氟化氫氣體分解成22.4L極1mol的氫氣和22.4L即1mol的氟氣吸收546.6 kJ熱量,化學計量數表示物質的量,不是體積,故A錯誤;
B、液態氟化氫的能量比氣態氟化氫的能量低,根據能量守恒,1mol氫氣與1mol氟氣反應生成2mol液態氟化氫放出的熱量大于546.6 kJ,故B正確;
C、反應為放熱反應,在相同條件下,1mol氫氣與1mol氟氣的能量總和大于2mol氟化氫氣體的能量,故C正確;
D、舊鍵的斷裂吸收能量,新鍵的生成釋放能量,該反應是放熱反應,所以2molH-F鍵的鍵能比1molH-H鍵和1molF-F鍵的鍵能之和大546.6kJ,故D正確.
故選A.
點評 本題考查學生對熱化學方程式的理解、反應熱與能量關系,難度不大,注意反應物總能量大于生成物的總能量為放熱反應,反應物總能量小于生成物的總能量為吸熱反應.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 氯氣通入石灰乳中,制取漂白粉 | |
| B. | 自來水廠可用明礬對水進行消毒殺菌 | |
| C. | 實驗室保存氯化鐵溶液時加少量鹽酸,目的是防止Fe3+水解 | |
| D. | 常溫下濃硝酸與鋁、鐵均不反應,可用鋁或鐵制的容器存放濃硝酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
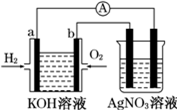 化學在能源開發與利用中起著十分關鍵的作用.氫氣是一種新型的綠色能源,又是一種重要的化工原料.
化學在能源開發與利用中起著十分關鍵的作用.氫氣是一種新型的綠色能源,又是一種重要的化工原料.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,46gNO2與N2O4的混合氣體中含有的原子數為3NA | |
| B. | 15.6g Na2O2與過量CO2反應時,轉移的電子數為0.4NA | |
| C. | 常溫常壓下,11.2L二氧化硫中所含的氧原子數等于NA | |
| D. | 1L1mol•L-1的Na2CO3溶液中含有NA個CO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
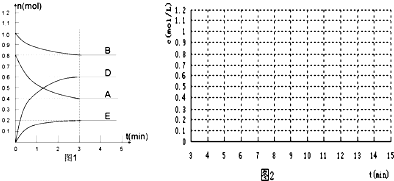
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 碳 | 氮 | Y | ||
| 鋁 | X | 硫 | Z |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
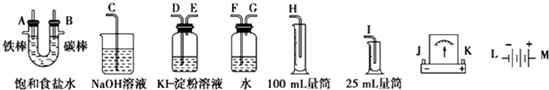
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com