
【題目】某同學設計如下實驗裝置用于制取純凈的無水FeCl3.
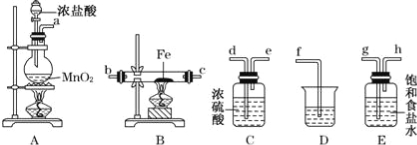
(1)圖中盛放濃鹽酸的實驗儀器的名稱為 ,A中發生反應的化學方程式為
(2)各裝置的正確連接順序為:a → → → → → → c → (填字母代號),
(3)裝置E的作用是 ,裝置C的作用是 。
(4)裝置D中所發生反應的離子方程式為 .
(5)裝置A中,如果反應產生氯氣的體積為2.24L(標準狀況),則反應中被氧化的HCl的質量為 ___________。
【答案】(1)分液漏斗;MnO2+4HCl(濃) ![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)a →g→h→d→e→b→c→f;
(3)除去氯氣中的HCl;干燥Cl2;
(4)Cl2+H2O![]() H++Cl-+HClO;(5)7.3g。
H++Cl-+HClO;(5)7.3g。
【解析】
試題分析:該實驗目的是用Cl2和Fe反應制取FeCl3 固體,實驗室用濃鹽酸和MnO2加熱制取Cl2,因為要制取純凈干燥的FeCl3,所以生成的Cl2必須是干燥、純凈的,濃鹽酸、水都具有揮發性,所以生成的Cl2中含有HCl、H2O,用飽和食鹽水除去HCl、用濃硫酸干燥Cl2,氯氣有毒,不能直接排空,應該用堿液吸收Cl2。(1)圖中盛放濃鹽酸的實驗儀器的名稱為分液漏斗,實驗室用濃鹽酸和MnO2加熱制取Cl2,二者反應生成氯化錳、氯氣和水,反應方程式為MnO2+4HCl(濃) ![]() MnCl2+Cl2↑+2H2O;(2)各裝置的正確連接順序為氣體制備裝置、洗氣裝置、干燥裝置、氯化鐵制備裝置、尾氣處理裝置,所以其連接順序是a→g→h→d→e→b→c→f;(3)裝置E的作用是吸收揮發出的HCl,裝置C的作用是干燥氣體,防止得不到干燥的氯化鐵,故答案為:除去氯氣中的氯化氫;干燥氯氣;(4)裝置D中氯氣和水反應生成鹽酸、次氯酸和水,反應的離子方程式為Cl2+H2O
MnCl2+Cl2↑+2H2O;(2)各裝置的正確連接順序為氣體制備裝置、洗氣裝置、干燥裝置、氯化鐵制備裝置、尾氣處理裝置,所以其連接順序是a→g→h→d→e→b→c→f;(3)裝置E的作用是吸收揮發出的HCl,裝置C的作用是干燥氣體,防止得不到干燥的氯化鐵,故答案為:除去氯氣中的氯化氫;干燥氯氣;(4)裝置D中氯氣和水反應生成鹽酸、次氯酸和水,反應的離子方程式為Cl2+H2O![]() H++Cl-+HClO;(5)裝置A中,如果反應產生氯氣的體積為2.24L(標準狀況),其物質的量n(Cl2)=2.24L÷22.4L/mol=0.1mol,根據Cl原子守恒計算反應中被氧化的n(HCl)=2n(Cl2)=2×0.1mol=0.2mol,被氧化HCl的質量是m(HCl)=n·M=0.2mol×36.5g/mol=7.3g。
H++Cl-+HClO;(5)裝置A中,如果反應產生氯氣的體積為2.24L(標準狀況),其物質的量n(Cl2)=2.24L÷22.4L/mol=0.1mol,根據Cl原子守恒計算反應中被氧化的n(HCl)=2n(Cl2)=2×0.1mol=0.2mol,被氧化HCl的質量是m(HCl)=n·M=0.2mol×36.5g/mol=7.3g。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】NaCN為劇毒無機物。某興趣小組查資料得知,實驗室里的NaCN溶液可用Na2S2O3溶液進行解毒銷毀,他們開展了以下三個實驗,請根據要求回答問題:
實驗Ⅰ.硫代硫酸鈉晶體(Na2S2O3·5H2O)的制備:
已知Na2S2O3·5H2O對熱不穩定,超過48℃即開始丟失結晶水。現以Na2CO3和Na2S物質的量之比為2∶1的混合溶液及SO2氣體為原料,采用如圖裝置制備Na2S2O3·5H2O。

(1)將Na2S和Na2CO3按反應要求的比例一并放入三頸燒瓶中,注入150 mL蒸餾水使其溶解,在蒸餾燒瓶中加入Na2SO3固體,在分液漏斗中注入____________(填以下選擇項的字母),并按下圖安裝好裝置,進行反應。
A.稀鹽酸 B.濃鹽酸 C.70%的硫酸 D.稀硝酸
(2)pH小于7會引起Na2S2O3溶液的變質反應,會出現淡黃色渾濁。反應約半小時,當溶液pH接近或不小于7時,即可停止通氣和加熱。如果通入SO2過量,發生的化學反應方程式為________________;
實驗Ⅱ.產品純度的檢測:
(3)已知:Na2S2O3·5H2O的摩爾質量為248 g/mol;2Na2S2O3+I2=2NaI+Na2S4O6。取晶體樣品a g,加水溶解后,滴入幾滴淀粉溶液,用0.010 mol/L碘水滴定到終點時,消耗碘水溶液v mL。①滴定終點的現象是 ;②該樣品純度是______________________;
(4)滴定過程中可能造成實驗結果偏低的是___________________;
A.錐形瓶未用Na2S2O3溶液潤洗
B.錐形瓶中溶液變藍后立刻停止滴定,進行讀數
C.滴定終點時仰視讀數
D.滴定管尖嘴內滴定前無氣泡,滴定終點發現氣泡
實驗Ⅲ.有毒廢水的處理:
(5)興趣小組的同學在采取系列防護措施及老師的指導下進行以下實驗:
向裝有2 mL 0.1 mol/L 的NaCN溶液的試管中滴加2 mL 0.1mol/L 的Na2S2O3溶液,兩反應物恰好完全反應,但無明顯現象,取反應后的溶液少許滴入盛有10 mL 0.1 mol/L FeCl3溶液的小燒杯,溶液呈現血紅色,請寫出Na2S2O3解毒的離子反應方程式____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溶液僅含如表離子中的5種(不考慮水的電離及離子的水解)且各種離子物質的量均為1 mol。
陽離子 | Na+ Mg2+ Fe3+ Al3+ Fe2+ |
陰離子 | OH- CO |
①若向溶液中加入KSCN溶液無明顯變化;
②若向原溶液中加入稀鹽酸,有無色氣體生成,該無色氣體遇空氣變成紅棕色,且溶液中陰離子種類不變。
請推斷:
(1)原溶液中含有的陽離子是________; 含有的陰離子是________________。
(2)向原溶液中加入足量稀鹽酸發生反應的離子方程式為____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以黃鐵礦為原料制硫酸產生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等。實驗室模擬工業以硫酸渣制備鐵紅(Fe2O3),過程如下:
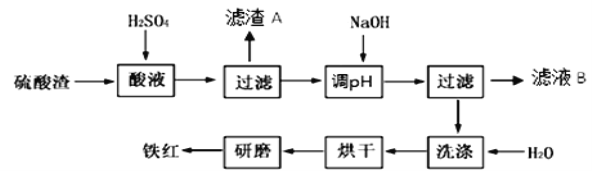
(1)硫酸渣的成分中既能與酸又能與堿反應的是 ,寫出酸溶過程Fe2O3與稀硫酸反應的離子反應方程式: 。
(2)生產過程中,為了確保鐵紅的純度,氧化過程需要調節溶液的pH的范圍是
(部分陽離子以氫氧化物形式沉淀時溶液的pH見下表)
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
開始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 |
完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 |
(3)濾渣A的主要成分為 ,濾液B含有的主要物質有 。
(4)如何證明洗滌環節充分洗凈 。
(5)已知硫酸渣質量為a kg,假設鐵紅制備過程中鐵元素損耗25%,最終得到鐵紅的質量為b kg,則原來硫酸渣中鐵元素質量分數為 。(用題中所給數據計算并用最簡整數比表示結果)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】醋是重要的調味品,我國勞動人民在很早以前就知道酒在空氣中能“酸敗成醋”,該過程的實質是
A、酒中的乙醇揮發,使乙醇的含量降低
B、酒中的乙醇被氧化成乙醛
C、酒中的乙醇被氧化成乙酸
D、酒中的雜質腐敗成酸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關說法正確的是:
A.在酒精燈加熱條件下,Na2CO3、NaHCO3固體都能發生分解
B.Fe(OH)3膠體無色、透明,能發生丁達爾現象
C.H2、SO2、CO2三種氣體都可用濃硫酸干燥
D.SiO2既能和氫氧化鈉溶液反應有能和氫氟酸反應,所以是兩性氧化物
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com