
反應N2O4(g)  2NO2(g) ΔH=+57 kJ·mol-1,在溫度為T1、T2時,平衡體系中NO2的體積分數隨壓強變化曲線如圖所示。下列說法正確的是
2NO2(g) ΔH=+57 kJ·mol-1,在溫度為T1、T2時,平衡體系中NO2的體積分數隨壓強變化曲線如圖所示。下列說法正確的是
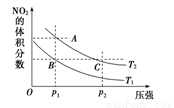
A.A、C兩點的反應速率:A>C
B.由狀態B到狀態A,可以用加熱的方法
C.A、C兩點混合氣體的平均相對分子質量:A>C
D.B、C兩點的反應速率:B=C
科目:高中化學 來源:2016屆黑龍江省高三上期中測試化學試卷(解析版) 題型:選擇題
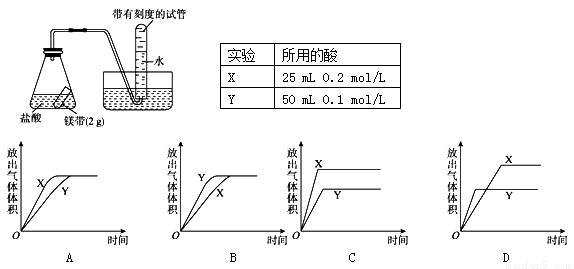
用如圖所示的實驗裝置進行實驗X及Y時,每隔半分鐘分別測定放出氣體的體積。下列選項中正確表示實驗X及Y的結果的是
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山東壽光中學高一上10月月考化學試卷(解析版) 題型:選擇題
下列因素與氣體的體積關系不大的是
A.溫度 B.壓強 C.分子大小 D.分子間平均距離
查看答案和解析>>
科目:高中化學 來源:2015-2016學年甘肅省高一上期中測試化學試卷(解析版) 題型:選擇題
下列敘述中正確的是
A.能電離出氫離子的化合物叫做酸
B.能電離出氫氧根離子的化合物叫做堿
C.鹽電離出的陽離子只能是金屬陽離子
D.由金屬離子和酸根離子組成的化合物屬于鹽
查看答案和解析>>
科目:高中化學 來源:2015-2016學年西藏拉薩中學高二上第一次月考化學試卷(解析版) 題型:填空題
紅磷P(s)和Cl2(g)發生反應生成PCl3(g)和PCl5(g)。反應過程和能量關系如下圖所示(圖中的ΔH表示生成1 mol產物的數據)。

根據上圖回答下列問題:
(1)P和Cl2反應生成PCl3的熱化學方程式是_______________________
(2)PCl5分解成PCl3和Cl2的熱化學方程式是_______________________
(3)P和Cl2分兩步反應生成1 mol PCl5的ΔH3=__________________,P和Cl2一步反應生成1 mol PCl5的ΔH4_____________ΔH3(填“大于”、“小于”或“等于”)。
查看答案和解析>>
科目:高中化學 來源:2016屆吉林省長春市高三上學期期中測試化學試卷(解析版) 題型:填空題
(15分)Ⅰ.下面的虛線框中每一列、每一行相當于周期表的每一族和每一周期,但它的列數和行數都多于元素周期表。

I.請在下面的虛線框中用實線畫出周期表第一至第六周期的輪廓,并畫出金屬與非金
屬的分界線。(要求:左上角的第一個格是第一周期第IA族元素)
II.X、Y、Z、M、N為短周期的五種主族元素,其中X、Z同主族,Y、Z同周期,M與X,Y既不同族,也不同周期。X原子最外層電子數是核外電子層數的三倍,Y的最高化合價與其最低化合價的代數和等于6。N是短周期主族元素中原子半徑最大的非金屬元素。
(1)請寫出下列元素的元素符號:X____________,Y____________,M____________。
(2)請寫出N元素在周期表中的位置 周期、 主族;與N同族的短周期元素L,其最高價氧化物的電子式為 ;N的最高價氧化物與NaOH溶液反應離子方程式: 。
(3)Y與Z的最高價氧化物的水化物的酸性強弱 (用化學式表示)Y與Z相比,非金屬性較強的元素是________________,可以證明該結論的實驗是(用化學方程式表示) 。
(4)L和M 按1:4的原子個數組成的化合物甲與 X的常見氣態單質乙以及NaOH溶液構成原電池,如圖,試分析:

①閉合K,寫出左側A電極的反應式
②閉合K,當A電極消耗1.6g化合物甲時(假設過程中無任何損失),則右側裝置中電極上放出的氣體在標準狀況下的體積為 升
查看答案和解析>>
科目:高中化學 來源:2016屆山東省滕州市高三上學期10月月考化學試卷(解析版) 題型:選擇題
下列敘述正確的是
A.在原電池的負極和電解池的陰極上都發生氧化反應
B.用惰性電極電解CuSO4溶液,陰陽兩極產物的物質的量之比為1:2
C.使用了合適的催化劑,能改變化學反應速率,但不改變化學平衡常數
D.電解質溶液導電的過程就是電解過程,是化學變化
查看答案和解析>>
科目:高中化學 來源:2015-2016學年甘肅蘭州一中高二上期中測試理科化學試卷(解析版) 題型:選擇題
可逆反應2SO2(g)+O2(g) 2SO3(g)從正方向開始,并達到了平衡,此時SO2和O2的物質的量之比為2∶1;若采取某種措施,導致SO2和O2又消耗了一些,并再次達到平衡,下列說法正確的是
2SO3(g)從正方向開始,并達到了平衡,此時SO2和O2的物質的量之比為2∶1;若采取某種措施,導致SO2和O2又消耗了一些,并再次達到平衡,下列說法正確的是
A.新平衡體系中,SO2和O2物質的量之比仍為2∶1
B.平衡向正反應方向移動,原因是正反應速率增大,逆反應速率減小
C.新平衡體系與舊平衡體系比較,SO3的濃度肯定增大
D.若采取的措施是縮小容器的容積,則新舊平衡中SO2和O2的轉化率之比都是1∶1
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河南洛陽高級中學高二上9月月考化學試卷(解析版) 題型:選擇題
已知:C(s)+H2O(g)===CO(g)+H2(g) ΔH=a kJ·mol-1 2C(s)+O2(g)===2CO(g) ΔH=-220 kJ·mol-1 H—H、O=O和O-H鍵的鍵能分別為436 kJ·mol-1、496 kJ·mol-1和462 kJ·mol-1,則a為
A.-118 B.+130 C.-332 D.+350
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com