
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | |||||
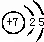 ,③與①所形成的化合物的結構式為:
,③與①所形成的化合物的結構式為: .
. .
.分析 由元素在周期表中位置,可知①為H、②為C、③為N、④為O、⑤為Na、⑥為Al、⑦為Cl,結合對應單質、化合物的性質以及元素周期率知識解答該題.
解答 解:由元素在周期表中位置,可知①為H、②為C、③為N、④為O、⑤為Na、⑥為Al、⑦為Cl,
(1)元素③為N元素,原子核外有2個電子層,最外層電子數為5,原子結構示意圖為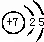 ,③與①所形成的化合物為氨氣,氨氣是氮原子和氫原子之間通過共價單鍵形成的三角錐形結構,結構式為:
,③與①所形成的化合物為氨氣,氨氣是氮原子和氫原子之間通過共價單鍵形成的三角錐形結構,結構式為: ,故答案為:
,故答案為: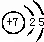 ;
; ;
;
(2)H原子只有1個電子層,其原子半徑最小,故答案為:H;
(3)②與④最高價化合物為CO2,二氧化碳是氧原子和碳原子之間通過共價鍵形成的共價化合物,形成過程為 ,
,
故答案為: ;
;
(4)金屬性Na>Mg,金屬性越強,最高價氧化物對應水化物的堿性越強,故NaOH>Al(OH)3,故答案為:NaOH>Al(OH)3;
(5)元素O的氫化物為水,氯氣與水反應生成鹽酸和次氯酸,氧化物不能拆,單質不能拆,此反應的離子方程式為Cl2+H2O=H++Cl-+HClO,
故答案為:Cl2+H2O=H++Cl-+HClO;
(6)③、④都是較活潑的非金屬元素,反應4NH3+3O2$\frac{\underline{\;點燃\;}}{\;}$2N2+6H2O中氧化劑是氧氣、氧化產物是氮氣,說明氧氣的氧化性大于氮氣,則非金屬性:N<O,
故答案為:4NH3+3O2$\frac{\underline{\;點燃\;}}{\;}$2N2+6H2O.
點評 本題考查元素的推斷以及原子結構、物質的性質等知識,題目難度不大,本題注意有關電子式和反應的離子的方程方程式的書寫,加強化學用語的學習.


科目:高中化學 來源: 題型:選擇題
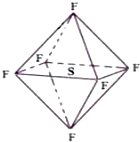 六氟化硫分子呈正八面體形(如圖所示),在高電壓下仍有良好的絕緣性,在電器工業方面有著廣泛的用途,但逸散到空氣中會引起溫室效應,下列有關六氟化硫的推測正確的是( )
六氟化硫分子呈正八面體形(如圖所示),在高電壓下仍有良好的絕緣性,在電器工業方面有著廣泛的用途,但逸散到空氣中會引起溫室效應,下列有關六氟化硫的推測正確的是( )| A. | 六氟化硫易燃燒生成二氧化硫 | |
| B. | 六氟化硫中各原子均達到8電子穩定結構 | |
| C. | 六氟化硫分子中的S-F鍵都是σ鍵,且鍵長、鍵能都相等 | |
| D. | 六氟化硫分子是極性分子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
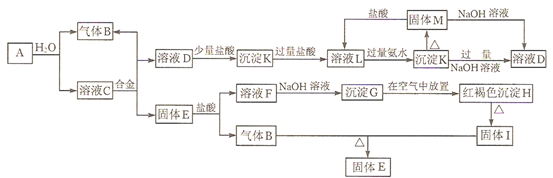
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | SO42-、SO32-至少含有一種 | |
| B. | 沉淀B的化學式為BaCO3 | |
| C. | 肯定存在的陰離子有CO32-、HCO3-、Cl-,還有SO42-、SO32-至少含有一種 | |
| D. | 肯定沒有的離子是Br- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲同學認為氯化銨由N、H、Cl三種元素組成 | |
| B. | 乙同學認為一個氯化銨分子中含有一個NH4+和一個Cl- | |
| C. | 丙同學認為氯化銨由NH4+和Cl-構成 | |
| D. | 丁同學認為氯化銨中陰、陽離子個數比為1:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C2H6與C4H10一定互為同系物 | |
| B. | C2H4與C4H8一定互為同系物 | |
| C. | 分子量相同的兩種物質一定互為同分異構體 | |
| D. | 分子中含有羥基的物質一定是醇 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該電池的正極為鋅 | |
| B. | 電池正極反應式為:MnO2+e-+H2O═MnO(OH)+OH- | |
| C. | 該電池反應中二氧化錳起催化劑作用 | |
| D. | 當 0.l mol Zn 完全溶解時,流經電解液的電子數目為 1.204×l023 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①⑤⑦ | B. | ④⑥⑦ | C. | ②③⑤ | D. | ③④⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com