
| 操 作 | 現 象 |
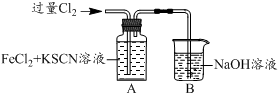 | I.A中溶液變紅 II.稍后,溶液由紅色變為黃色 |
 .
.分析 (1)B裝置是用來吸收氯氣尾氣的,根據元素守恒和電荷守恒可以寫出離子方程式;
(2)Fe2+被Cl2氧化生成Fe3+,Fe3+與SCN-反應生成紅色的硫氰化鐵溶液,呈紅色,據此答題;
(3)①A中黃色溶液于試管中,加入NaOH溶液,有紅褐色沉淀生成,應當是氫氧化鐵固體,所以原溶液中應當有Fe3+,據此答題;
(4)①根據SCN-的電子式為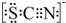 可知,SCN-中碳顯+4價,硫顯-2價,氮顯-3價,碳已經是最高正價了,不能再被氧化了,據此答題;
可知,SCN-中碳顯+4價,硫顯-2價,氮顯-3價,碳已經是最高正價了,不能再被氧化了,據此答題;
②加入用鹽酸酸化的BaCl2溶液,產生白色沉淀,說明白色沉淀為硫酸鋇,即溶液中有硫酸根離子,其中硫顯+6價,而原來SCN-中硫顯-2價,所以被氧化的元素為硫元素,據此答題;
③利用硝酸根離子在酸性條件下有強氧化性,遇到銅被還原,生成一氧化氮,在空氣中被 氧化成紅棕色的二氧化氮氣體,可以檢驗硝酸根離子的存在,據此答題;
④SCN-與Cl2反應的化學方程式可以計算出電子轉移的物質的量.
解答 解:(1)B裝置是用來吸收氯氣尾氣的,根據元素守恒和電荷守恒可以寫出離子方程式為:Cl2+2OH-═Cl-+ClO-+H2O,
故答案為:Cl2+2OH-═Cl-+ClO-+H2O;
(2)氯氣具有強氧化性,則Fe2+被Cl2氧化生成Fe3+,Fe3+與SCN-反應生成紅色的硫氰化鐵溶液,呈紅色,
故答案為:Fe2+被Cl2氧化生成Fe3+,Fe3+與SCN-反應生成紅色的硫氰化鉀,所以溶液變紅;
(3)①A中黃色溶液于試管中,加入NaOH溶液,有紅褐色沉淀生成,應當是氫氧化鐵固體,所以原溶液中應當有Fe3+,
故答案為:Fe3+;
(4)①根據SCN-的電子式為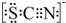 可知,SCN-中碳顯+4價,硫顯-2價,氮顯-3價,碳已經是最高正價了,不能再被氧化了,
可知,SCN-中碳顯+4價,硫顯-2價,氮顯-3價,碳已經是最高正價了,不能再被氧化了,
故答案為:SCN-中的碳元素是最高價態+4價;
②加入用鹽酸酸化的BaCl2溶液,產生白色沉淀,說明白色沉淀為硫酸鋇,即溶液中有硫酸根離子,其中硫顯+6價,而原來SCN-中硫顯-2價,所以被氧化的元素為硫元素,
故答案為:硫元素;
③利用硝酸根離子在酸性條件下有強氧化性,遇到銅被還原,生成一氧化氮,在空氣中被 氧化成紅棕色的二氧化氮氣體,可以檢驗硝酸根離子的存在,據此可知實驗方案為:取足量銅粉于試管中,加入A中黃色溶液和一定量的稀鹽酸,加熱,觀察到試管上方有紅棕色氣體生成,證明A中存在,SCN-中氮元素被氧化成NO3-,
故答案為:取足量銅粉于試管中,加入A中黃色溶液和一定量的稀鹽酸,加熱,觀察到試管上方有紅棕色氣體生成,證明A中存在,SCN-中氮元素被氧化成NO3-;
④SCN-與Cl2反應生成硫酸根和硝酸根還有二氧化碳,所以它們反應的化學方程式為:SCN-+8Cl2+9H2O=NO3-+SO42-+CO2+Cl-+18H+,該反應中電子轉移數目為16,則由方程式可知,每生成1mol二氧化碳要轉移16mol電子,
故答案為:16.
點評 本題是實驗方案的設計與評價,題目難度中等,試題綜合性較強,涉及到了離子的檢驗、氧化還原的離子方程式的書寫、實驗步驟的設計、化學計算等知識點,熟練掌握元素化合物的基礎知識及實驗基本操作要求為解答關鍵.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 ),其分子中相鄰的C和N原子相比,N原子吸引電子能力更強(填“強”或“弱”),從原子結構角度解釋原因:C和N原子在同一周期(或電子層數相同),N原子核電荷數更大,原子半徑更小,原子核對外層電子的吸引力更強.
),其分子中相鄰的C和N原子相比,N原子吸引電子能力更強(填“強”或“弱”),從原子結構角度解釋原因:C和N原子在同一周期(或電子層數相同),N原子核電荷數更大,原子半徑更小,原子核對外層電子的吸引力更強.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 銅的金屬活動性比鐵差,可在海輪外殼上裝若干銅塊以減緩其腐蝕 | |
| B. | 銨鹽受熱易分解,實驗室常加熱硝酸銨與氫氧化鈣的混合物制取氨氣 | |
| C. | 氯化鐵有氧化性,工業上用FeCl3溶液蝕刻銅箔制造電路板 | |
| D. | 氨水具有弱堿性,可與飽和氯化鐵溶液反應制得氫氧化鐵膠體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 時間/s | 0 | 20 | 40 | 60 | 80 | 100 |
| c(NO2)/mol•L-1 | 0.00 | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
| A. | 升高溫度該反應的平衡常數K減小 | |
| B. | 20~40 s 內,v(N2O4)=0.004 mol•L-1•s1 | |
| C. | 反應達平衡時,吸收的熱量為0.30 Q kJ | |
| D. | 100 s 時再通入0.40 mol N2O4,達新平衡時N2O4的轉化率增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在任何條件下,等物質的量的乙烯(C2H4)和CO所含的分子數目相等 | |
| B. | 等物質的量的N2和CO在標準狀況下的體積均為22.4L | |
| C. | 同溫同壓下,等體積的物質所含分子數目一定相等 | |
| D. | 1molHCl中所含的分子數目和1L1mol/L鹽酸中所含的分子數目相同 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com