
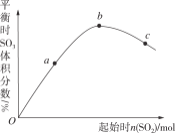
【題目】在一定溫度下,改變反應物中n(SO2),對反應2SO2(g)+O2(g)2SO3(g) ΔH<0的影響如圖所示,下列說法正確的是( )
A.反應bc點均為平衡點,a點未達到平衡且向正反應方向進行
B.abc三點的平衡常數(shù)Kb>Kc>Ka
C.上述圖象可以得出SO2的含量越高得到的混合氣體中SO3的體積分數(shù)越高
D.abc三點中,a點時SO2的轉化率最高
【答案】D
【解析】
A. 圖像的橫坐標是起始時n(SO2),縱坐標是平衡時SO3的體積分數(shù),因此,曲線是平衡線,線上的每個點均為平衡點,A項錯誤;
B. 對于一個指定的反應,其平衡常數(shù)只受溫度的影響,上述反應在一定溫度下進行,因此,a、b、c三點的平衡常數(shù)相等,B項錯誤;
C. 由圖像知,隨起始時n(SO2)的增大,平衡時SO3的體積分數(shù)先逐漸增大、后又逐漸減小,C項錯誤;
D. 增加一種反應物的用量,可以提高另一反應物的轉化率,而本身轉化率降低,因此a、b、c三點中,n(SO2)逐漸增大,平衡時SO2的轉化率逐漸減小,a點時SO2的轉化率最高,D項正確;
答案選D。


科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A.硫酸氫鈉溶液中,c(Na+)>c(SO42-)B.醋酸鈉溶液中,c(Na+)>c(CH3COO-)
C.碳酸鈉溶液中,c(HCO3-)>c(OH--)D.碳酸氫鈉溶液中,c(CO32-)>c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一密閉容器中,當反應aA(g) ![]() bB(g)+cC(g)達到平衡后,保持溫度不變,將容器體積增加一倍,最終測得A的物質的量的濃度為原來的55%,則
bB(g)+cC(g)達到平衡后,保持溫度不變,將容器體積增加一倍,最終測得A的物質的量的濃度為原來的55%,則
A. 平衡向正反應方向移動 B. a>b+c
C. 物質B的質量分數(shù)增大 D. 以上判斷都錯誤
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學組裝了如圖所示的電化學裝置,則下列說法正確的是( )

A.圖中甲池為原電池裝置,Cu電極發(fā)生還原反應
B.實驗過程中,甲池左側燒杯中NO3-的濃度不變
C.若甲池中Ag電極質量增加5.4g時,乙池某電極析出1.6g金屬,則乙中的某鹽溶液可能是AgNO3溶液
D.若用銅制U形物代替“鹽橋”,工作一段時間后取出U型物稱量,質量不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A.在中和熱的測定實驗中,將氫氧化鈉溶液迅速倒入盛有鹽酸的量熱計中,立即讀出并記錄溶液的起始溫度,充分反應后再讀出并記錄反應體系的最高溫度
B.500℃,30MPa下,將0.5molN2和1.5molH2置于密閉容器中充分反應生成NH3(g),放熱19.3kJ,其熱化學方程式為:N2(g)+3H2(g)![]() 2NH3(g) H=-38.6kJ/mol
2NH3(g) H=-38.6kJ/mol
C.分光光度計可以用來測定某些化學反應的反應速率
D.甲烷的標準燃燒熱為890.3kJ/mol,則甲烷燃燒的熱化學方程式可表示為:CH4(g)+2O2(g)=CO2(g)+2H2O(g) H=-890.3kJ/mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組的同學設計了如圖所示的裝置,完成下列問題:
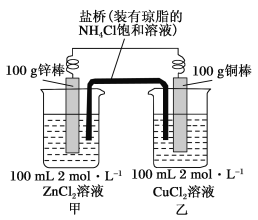
(1)反應過程中,_____棒質量減少,當一電極質量增加2 g,另一電極減輕的質量_____(填“大于”、“小于”或“等于”)2g,正極的電極反應為_______。
(2)鹽橋的作用是向甲、乙兩燒杯中提供NH![]() 和Cl-,使兩燒杯溶液中保持電荷守恒。
和Cl-,使兩燒杯溶液中保持電荷守恒。
①反應過程中Cl-將進入______(填“甲”或“乙”)燒杯。
②當外電路中轉移0.2 mol電子時,乙燒杯中濃度最大的陽離子是______。
查看答案和解析>>
科目:高中化學 來源: 題型:
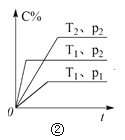
【題目】下列敘述與下圖對應的是( )
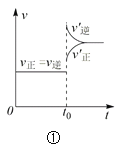
A.對于達到平衡狀態(tài)的N2(g) + 3H2(g) 2NH3(g),圖①表示在t0時刻充入了一定量的NH3,平衡逆向移動
B.由圖②可知,p2 > p1,T1 > T2滿足反應:2A(g) + B(g) 2C(g) ΔH < 0
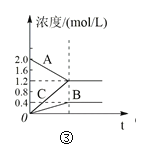
C.圖③表示的反應方程式為2A = B + 3C
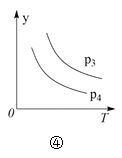
D.對于反應2X(g) + 3Y(g) 2Z(g) ΔH < 0,圖④y軸可以表示Y的百分含量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】隨著材料科學的發(fā)展,金屬釩及其化合物得到了越來越廣泛的應用,并被譽為“合金的維生素”。為回收利用含釩催化劑(含有V2O5、VOSO4及不溶性殘渣),科研人員最新研制了一種離子交換法回收釩的新工藝,回收率達91.7%以上。部分含釩物質在水中的溶解性如下表所示:
物質 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
溶解性 | 可溶 | 難溶 | 難溶 | 易溶 |
該工藝的主要流程如下。

請回答下列問題:
經過熱重分析測得:NH4VO3在焙燒過程中,固體質量的減少值(縱坐標)隨溫度變化的曲線如圖所示。則NH4VO3在分解過程中_________。

A.先分解失去H2O,再分解失去NH3 B.先分解失去NH3,再分解失去H2O
C.同時分解失去H2O和NH3 D.同時分解失去H2、N2和H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在容積不變的密閉容器中存在如下反應2SO2(g)+O2(g) ![]() 2SO3(g) ΔH <0,某學習小組研究了其他條件不變時,改變某一條件對上述反應的影響,下列分析正確的是 ( )
2SO3(g) ΔH <0,某學習小組研究了其他條件不變時,改變某一條件對上述反應的影響,下列分析正確的是 ( )
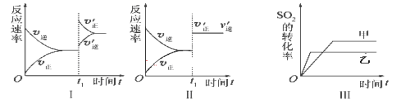
A.圖Ⅰ表示的是t1時刻增大O2的濃度對反應速率的影響
B.圖Ⅱ表示的是t1時刻加入催化劑后對反應速率的影響
C.圖Ⅲ表示的是壓強對化學平衡的影響,且乙的壓強較高
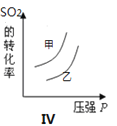
D.圖IV表示的是溫度、壓強對平衡的影響,且甲的溫度比乙的高
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com