
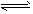 N2+2CO2將有害的污染物轉化為可參與大氣循環的N2和CO2。在某溫度下用氣體傳感器測得不同時間的NO和CO濃度如下表
N2+2CO2將有害的污染物轉化為可參與大氣循環的N2和CO2。在某溫度下用氣體傳感器測得不同時間的NO和CO濃度如下表
科目:高中化學 來源: 題型:閱讀理解
| ||
| ||
 N2+2CO2 將有害的污染物轉化為可參與大氣循環的N2和CO2.
N2+2CO2 將有害的污染物轉化為可參與大氣循環的N2和CO2.| 時間/h | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol?L-1 | 1.00×10-3 | 4.5×10-4 | 2.5×10-4 | 1.5×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol?L-1 | 3.6×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
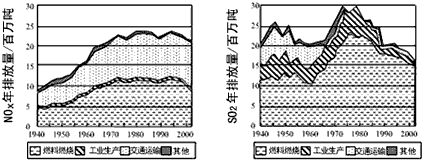
 (2011?太原二模)現已確認,CO、SO2和NOx的排放是造成大氣污染的重要原因.
(2011?太原二模)現已確認,CO、SO2和NOx的排放是造成大氣污染的重要原因.查看答案和解析>>
科目:高中化學 來源:2011年浙江省杭州市蕭山區高考化學模擬試卷(二十二)(解析版) 題型:填空題

 N2+2CO2 將有害的污染物轉化為可參與大氣循環的N2和CO2.
N2+2CO2 將有害的污染物轉化為可參與大氣循環的N2和CO2.| 時間/h | 1 | 2 | 3 | 4 | 5 | |
| c(NO)/mol?L-1 | 1.00×10-3 | 4.5×10-4 | 2.5×10-4 | 1.5×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol?L-1 | 3.6×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
查看答案和解析>>
科目:高中化學 來源:同步題 題型:填空題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com