
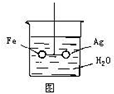
 如圖,在銀圈和鐵圈的聯接處吊著一個絕緣的細絲,使之平衡,然后小心地從燒杯中央滴入CuSO4溶液.
如圖,在銀圈和鐵圈的聯接處吊著一個絕緣的細絲,使之平衡,然后小心地從燒杯中央滴入CuSO4溶液.分析 鐵圈和銀圈連接浸入硫酸銅溶液中,該裝置構成了原電池,鐵較活潑的金屬作負極,銀較不活潑的金屬作正極,根據正負極上發生的電極反應判斷反應現象.
解答 解:(1)依據金屬活動順序可知鐵的活潑性強于銀,鐵圈和銀圈的連接處吊著一根絕緣的細絲,使之平衡.小心地從燒杯中央滴入CuSO4溶液后,該裝置構成了原電池,鐵較活潑的金屬作負極,失去電子,發生氧化反應生成鐵離子,質量減小;銀較不活潑的金屬作正極,銅離子在正極得到電子發生還原反應生成銅,在銀圈上析出,所以鐵圈向上傾斜,銀圈向下傾斜,
故答案為:銀圈表面析出紅色固體,銀圈向下傾斜;
(2)產生上述現象的原因是:鐵、銀、硫酸銅構成原電池,鐵不斷失電子而減少,銀上不斷析出銅,質量增加,所以銀圈逐漸向下傾斜;
故答案為:鐵、銀、硫酸銅構成原電池,鐵不斷失電子而減少,銀上不斷析出銅,質量增加,所以銀圈逐漸向下傾斜.
點評 本題以鐵的化學性質考查了原電池原理,為高頻考點,題目難度不大,把握鐵圈、銀圈相連與原電池原理即可解答.


 智趣寒假作業云南科技出版社系列答案
智趣寒假作業云南科技出版社系列答案科目:高中化學 來源: 題型:解答題
 如圖所示裝置為在直流電的作用下電解200molNaCl溶液圖,其中A、B為石墨電極,a、b為電源的兩極,當接通電源,通電一段時間后,B電極產生能使濕潤的淀粉碘化鉀試紙變藍的氣體224mL(標準狀況),則:
如圖所示裝置為在直流電的作用下電解200molNaCl溶液圖,其中A、B為石墨電極,a、b為電源的兩極,當接通電源,通電一段時間后,B電極產生能使濕潤的淀粉碘化鉀試紙變藍的氣體224mL(標準狀況),則:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
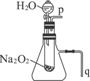 教材中有一個演示實驗:用脫脂棉包住約0.2g Na2O2粉末,置于石棉網上,可觀察到脫脂棉燃燒起來.
教材中有一個演示實驗:用脫脂棉包住約0.2g Na2O2粉末,置于石棉網上,可觀察到脫脂棉燃燒起來.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
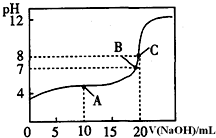 (1)pH=13的CH3COONa溶液加水稀釋100倍后,pH>11(填“>”“=”或“<”),原因是醋酸根離子水解溶液顯堿性,CH3COO-+H2O?CH3COOH+OH-,加水稀釋后醋酸根離子的水解程度增大,氫氧根離子濃度略有增大,則溶液的pH>11(用離子方程式和必要的文字說明);pH相等的NaOH溶液與CH3COONa溶液,分別加熱到相同的溫度后CH3COONa溶液的pH>NaOH溶液的pH(填“>”“=”或“<”);
(1)pH=13的CH3COONa溶液加水稀釋100倍后,pH>11(填“>”“=”或“<”),原因是醋酸根離子水解溶液顯堿性,CH3COO-+H2O?CH3COOH+OH-,加水稀釋后醋酸根離子的水解程度增大,氫氧根離子濃度略有增大,則溶液的pH>11(用離子方程式和必要的文字說明);pH相等的NaOH溶液與CH3COONa溶液,分別加熱到相同的溫度后CH3COONa溶液的pH>NaOH溶液的pH(填“>”“=”或“<”);查看答案和解析>>
科目:高中化學 來源: 題型:解答題
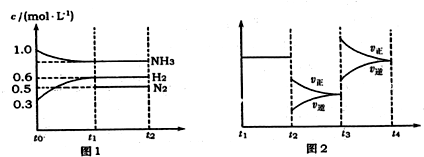
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
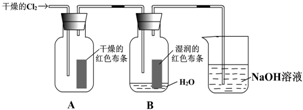
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
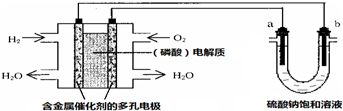
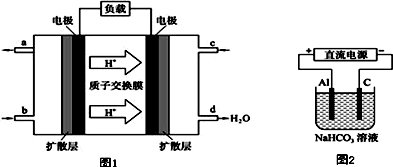
| A. | 電池工作時,正極反應式為:O2+4H++4e-═2H2O | |
| B. | 電解時,當陰極逸出amol氣體,同時有W克Na2SO4﹒10H2O 析出,保持溫度不變,剩余溶液中的硫酸鈉的質量分數是$\frac{71W}{161(W+36a)}$×100% | |
| C. | 電解時,電子流動路徑是:負極→外電路→陰極→溶液→陽極→正極 | |
| D. | 忽略能量損耗,當電池中消耗0.01g O2時,b 極周圍會產生0.02g H2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com