
在常溫條件下,下列對醋酸的敘述中,不正確的是
A.pH=5.6的CH3COOH與CH3COONa混合溶液中:c(Na+)<c(CH3COO-)
B.將pH=a的醋酸稀釋為pH=a+1的過程中,c(CH3COOH)/c(H+)變小
C.濃度均為0.1 mol·L-1的CH3COOH和CH3COONa溶液等體積混合后:
c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)]
D.等體積pH=a的醋酸與pH=b的NaOH溶液恰好中和時,存在a+b=14
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源:2016-2017學年吉林省高一上月考二化學卷(解析版) 題型:選擇題
如圖兩瓶體積相等的氣體,在同溫同壓時瓶內氣體的關系一定正確的是
A.所含原子數相等 B.氣體密度相等
C.氣體質量相等 D.摩爾質量相等
查看答案和解析>>
科目:高中化學 來源:2016-2017學年安徽省高二上期中化學卷(解析版) 題型:計算題
一定溫度下的密閉容器中存在如下反應:A(g)+B(g) C(g)+D(g),已知A和B的起始濃度均為3mol·L-1,經測定該反應在該溫度下的平衡常數K=1,試判斷:
C(g)+D(g),已知A和B的起始濃度均為3mol·L-1,經測定該反應在該溫度下的平衡常數K=1,試判斷:
(1)達到平衡時,A的轉化率為多少?(3分)
(2)當A的起始濃度仍為3mol·L-1,B的起始濃度為6mol·L-1,求:平衡時A的體積分數?(3分)
查看答案和解析>>
科目:高中化學 來源:2016-2017學年安徽省高二上期中化學卷(解析版) 題型:選擇題
500 mL KNO3 和Cu(NO3)2的混合溶液中c(NO3-)=3mol/L,用石墨作電極電解此溶液,當通電一段時間后,兩極均收集到11.2 L氣體(標準狀況),假定電解后溶液體積仍為500 mL,下列說法正確的是
和Cu(NO3)2的混合溶液中c(NO3-)=3mol/L,用石墨作電極電解此溶液,當通電一段時間后,兩極均收集到11.2 L氣體(標準狀況),假定電解后溶液體積仍為500 mL,下列說法正確的是
A.上述電解過程中共轉移1 mol電子  B.原混合溶液中c (K+)為1mol/L
B.原混合溶液中c (K+)為1mol/L
C.電解得到的Cu的物質的量為0.25mol D.電解后溶液中c(H+)為1mol/L
查看答案和解析>>
科目:高中化學 來源:2017屆河北省高三上期中化學試卷(解析版) 題型:填空題
【化學―選修2:化學與技術】以硫鐵礦(主要成分為FeS2)為原料制取硫酸,其礦渣可用來煉鐵。生產工藝示意圖如下:
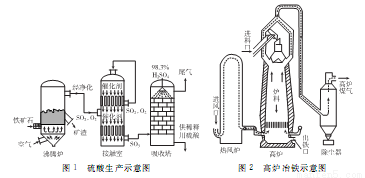
(1)配平煅燒硫鐵礦的反應方程式:______FeS2+________O2→_____Fe2O3+______SO2。實際生產中向沸騰爐通入的空氣量要大于鍛燒硫鐵礦所需空氣量.其目的是____________________。接觸室和熱風爐中都裝有熱交換器,可用反應的余熱將通入的氣體加熱,這樣做的好處是_____________________。
(2)生產硫酸時,吸收塔中用98.3%的硫酸吸收而不用水吸收SO3的原因是______________。用含FeS280%的硫鐵礦生產硫酸,如果煅燒時有5%的硫損失,SO2轉變成SO3的轉化率為80%,那么生產98%的濃硫酸3噸,則需要這種硫鐵礦___________噸。
(3)CO還原Fe2O3的冶鐵過程中,反應物、生成物和溫度之間的關系如圖所示.
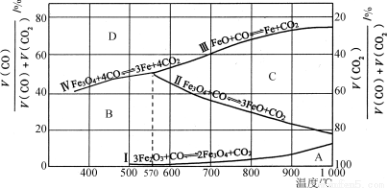
(圖中Ⅰ、Ⅱ、Ⅲ、Ⅳ四條曲線是四個化學反應平衡時的氣相組成對溫度作圖得到的;A、B、C 、D四個區域分別是Fe2O3、Fe3O4、FeO、Fe穩定存在的區域)
、D四個區域分別是Fe2O3、Fe3O4、FeO、Fe穩定存在的區域)
①冶煉高爐產生的高爐煤氣的主要成分有__________和剩余的CO。
②據圖分析,下列說法正確的是________(填字母)。
a.溫度低于570 ℃時,Fe2O3還原焙燒的產物中不含FeO
b.溫度越高,Fe2O3還原焙燒得到的 固體物質組成中Fe元素的質量分數越高
固體物質組成中Fe元素的質量分數越高
c.Fe2O3還原焙燒過程中及時除去CO2有利于提高Fe的產率
③800℃時,混合氣體中CO2體積分數為40%時,Fe2O3用CO還原焙燒反應的化學方程式為____________。
查看答案和解析>>
科目:高中化學 來源:2017屆河北省高三上期中化學試卷(解析版) 題型:選擇題
下列有關說法正確的是( )
A.鋅與稀硫酸反應時加入少量硫酸銅,反應加快的主要原因是Cu2+水解增大了H+濃度
B.鉛蓄電池放電時的負極和充電時的陰 極均發生氧化反應
極均發生氧化反應
C.電解法精煉銅時,以粗銅作陰極,純銅作陽極
D.鍍鋅鐵鍍層破損后鋅仍能減緩鐵腐蝕,其原理為犧牲陽極的陰極保護法
查看答案和解析>>
科目:高中化學 來源:2017屆河北省高三上期中化學試卷(解析版) 題型:選擇題
在溶液中加入足量Na2O2后仍能大量共存的離子組是( )
A.K+、AlO2-、Cl-、SO42-
B.H+、Ba2+、Cl-、NO3-
C.Ca2+、Fe2+、NO3-、HCO3-
D.Na+、Cl-、CO32-、SO32-
查看答案和解析>>
科目:高中化學 來源:2017屆甘肅省高三上月考三化學試卷(解析版) 題型:填空題
近來會寧縣區的空氣污染指數居高不下,霧霾天氣嚴重,據分析霾中含有硫和氮的氧化物,如SO2、NOx等。
(1)NOx是汽車尾氣中的主要污染物之一。
①NOx形成的酸雨被稱為硝酸型酸雨,硝酸型酸雨中含有的主要離子有 ;濃硝酸發黃的原因(用化學方程式解釋) 。
②汽車發動機工作時高溫電火花會引發N2和O2反應,反應的化學方程式是 。
(2)因SO2的大量排放形成的酸雨被稱為硫酸型酸雨,我國的酸雨主要是硫酸型酸雨。取硫酸型酸雨樣品置于空氣中,一段時間后發現該酸雨的酸性增強了,你認為原因是: (用化學方程式表示) 。
(3)為減少SO2的排放,常采取一些有效措施:
①在含硫煤中加入生石灰可以起到固硫的作用,燃燒過程中,硫元素轉化成其最高價態的化合物,該化合物的化學式是 。
②下列物質中,可用于吸收煙氣中的SO2的最佳溶液是 (填序號)。
a.Na2CO3 b.H2SO4 c.NaHSO3 d.NH3·H2O
(4)取某空氣樣本用蒸餾水處理制成待測液,其中所含的離子及其濃度如下:
離子 | K+ | Na+ | NH4+ | H+ | SO42- | NO3- | Cl- |
濃度/mol·L-1 | 4×10-6 | 6×10-6 | 2×10-5 | a | 4×10-5 | 3×10-5 | 2×10-5 |
根據表中數據計算: a= mol/L。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省高一上11月月考化學卷(解析版) 題型:填空題
(1)在常溫下,發生下列幾種反應:
①16H++10Z-+2XO4-=2X2++5Z2+8H2O ②2A2++B2=2A3++2B- ③2B-+Z2=B2+2Z-
根據上述反應,XO4-、Z2、B2、A3+ 氧化性從強到弱的順序為:________________。
(2)已知某化學反應的反應物和產物如下:
Al+NaNO3+H2O→Al(OH)3+N2↑+NaAlO2.
配平方程式并用單線橋法標出此反應的電子轉移方向和數目
(3) 有下列6種物質:K2SO4、K2SO3、I2、H2SO4、H2O、KIO3組成一個氧化還原反應,已知在反應中K2SO3失去電子,請回答下列問題:
①將這6種物質分別填入下面對應的橫線上,組成一個未配平的化學方程式:
_________+H2SO4+_________→_________+_________+_________(填化學式)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com