
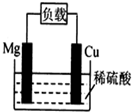
| A. | 電池反應為:Mg+2H+=Mg2++H2↑ | B. | 鎂棒發生還原反應 | ||
| C. | 電子從銅棒經外電路流向鎂棒 | D. | 銅棒為負極 |
分析 該裝置中,鎂易失電子作負極,銅作正極,負極上鎂失電子發生氧化反應,電極反應式為Mg-2e-=Mg2+,正極上氫離子放電,正極上電極反應式為:2H++2e-=H2↑,電子從負極沿導線流向正極.
解答 解:A.負極上電極反應式為Mg-2e-=Mg2+,正極上電極反應式為:2H++2e-=H2↑,所以電池反應式為Mg+2H+=Mg2++H2↑,故A正確;
B.鎂作負極,鎂失電子發生氧化反應,故B錯誤;
C.鎂作負極,銅作正極,電子從鎂沿導線流向銅,故C錯誤;
D.該裝置中,鎂易失電子作負極,Cu作正極,故D錯誤;
故選A.
點評 本題考查了原電池原理,根據電極上得失電子判斷正負極,再結合電極反應類型、電子流向來分析解答,熟記原電池原理,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 2 mol KClO3 | B. | 1 mol KCl | C. | 2 mol MgCl2 | D. | 2 mol NaCl |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 鈉 | 鉀 | 鈉鉀合金(質量比1:3) | |
| 熔點/℃ | 97.9 | 63.5 | <-10 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 不移動 | B. | 平衡左移 | C. | 平衡右移 | D. | 無法確定 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
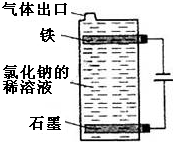 (1)按如圖電解氯化鈉的稀溶液可制得漂白液,寫出該電解池中發生反應的總反應方程式:NaCl+H2O$\frac{\underline{\;電解\;}}{\;}$NaClO+H2↑;
(1)按如圖電解氯化鈉的稀溶液可制得漂白液,寫出該電解池中發生反應的總反應方程式:NaCl+H2O$\frac{\underline{\;電解\;}}{\;}$NaClO+H2↑;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入氯化鋇溶液有白色沉淀生成,再加稀硝酸,沉淀不消失,一定含有SO42- | |
| B. | 觀察鉀元素焰色反應的操作是:將鉑絲放在稀鹽酸中洗滌后灼燒至無色,然后再用鉑絲蘸取固體氯化鉀,置于煤氣燈的火焰上進行灼燒,透過藍色鈷玻璃進行觀察 | |
| C. | 待檢液加入NaOH 溶液并加熱,有能使濕潤的紅色石蕊試紙變藍的氣體生成,則原溶液中一定含有NH4+ | |
| D. | 取少量久置的Na2SO3 樣品于試管中加水溶解,再加入足量鹽酸有氣體產生,然后加入BaCl2 溶液有白色沉淀產生,說明Na2SO3 樣品已部分被氧化 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
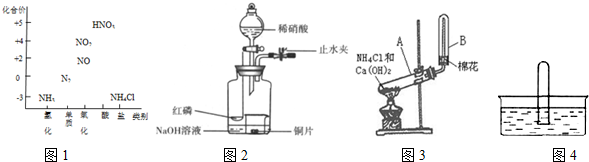
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
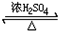 CH3COOC2H5+H2O、酯化反應(取代反應).
CH3COOC2H5+H2O、酯化反應(取代反應).查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com