
【化學——選修5:有機化學】3-羥基丁酸 (3-hydroxybutyrate)也稱為β-羥基丁酸 (beta-hydroxybutyrate),在工業中可用于合成可生物降解的塑料,如聚3-羥基丁酸(PHB);3-羥基丁酸也可以用于制取3-羥基丁酸乙酯(中國規定為允許使用的食品用香料)。
(3-hydroxybutyrate)也稱為β-羥基丁酸 (beta-hydroxybutyrate),在工業中可用于合成可生物降解的塑料,如聚3-羥基丁酸(PHB);3-羥基丁酸也可以用于制取3-羥基丁酸乙酯(中國規定為允許使用的食品用香料)。
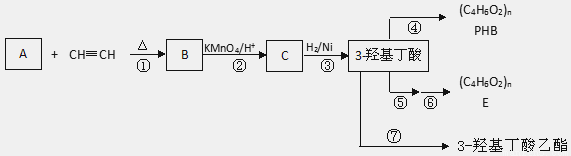
已知:i. 共軛二烯烴(如異戊二烯)與含有碳碳叁鍵的有機物作用時能形成環狀化合物:

ii. 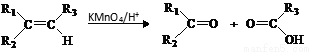
iii. 步驟②只有一種產物;E的結構中含有甲基
(1)A分子結構簡式 _____________ ;理論上B也可以由1,3-丁二烯與烴F來合成,則F的名稱(系統命名法):_________ ;C中含有的官能團的名稱是_________ 。
(2)寫出反應類型:③_____________, ⑤_____________。
(3)寫出PHB結構簡式___ ;它與E___ (填“互為”或“不互為” )同分異構體。
(4)寫出反應⑦的化學方 程式 。
程式 。
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源:2016屆海南省高三考前模擬理綜化學試卷(解析版) 題型:選擇題
設 N A 表示阿伏加德羅常數,下列說法中正確的是( )
A.標準狀況下,l L 甲醇完全燃燒后生成的 CO 2 分子個數約為(1/22.4)N A
B.N A個H 2分子的質量約為2g,它所占的體積約為 22.4L
C.標準狀況下,22.4L CO2與CO的混合氣體中含有的碳原子數為N A
D.500mL 0.5mol/L 的Ca(ClO)2溶液中,含有ClO-的數目為0.5NA
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山東省高二6月月考化學試卷(解析版) 題型:選擇題
下列物質中,既能導電又屬于強電解質的一組物質是
A.熔融MgCl2、熔融NaOH B.液氨、石灰水
C.石墨、食醋 D.稀硫酸、蔗糖
查看答案和解析>>
科目:高中化學 來源:2015-2016學年內蒙古赤峰二中高二6月月考化學試卷(解析版) 題型:選擇題
向CuSO4溶液中逐滴加入過量KI溶液,觀察到產生白色沉淀,溶液變為棕色。再向反應后的混合物中不斷通入SO2氣體,溶液逐漸變成無色.則下列分析中正確的是( )
A.白色沉淀是CuI2,棕色溶液含有I2
B.滴加KI溶液時,轉移1 mol電子時生成1 mol白色沉淀
C.通入SO2時,SO2與I2反應,I2作還原劑
D.上述實驗條件下,物質的氧化性:Cu2+>SO2>I2
查看答案和解析>>
科目:高中化學 來源:2015-2016學年內蒙古赤峰二中高二6月月考化學試卷(解析版) 題型:選擇題
NA代表阿伏加德羅常數的值。下列敘述正確的是
A.46g乙醇中存在的共價鍵總數為7NA
B.1mol -OH和1molOH-所含電子數均為9NA
C.密閉容器中1molNO與1molO2充分反應后的原子數為4NA
D.標準狀況下,22.4L庚烷完全燃燒生成二氧化碳分子數為7NA
查看答案和解析>>
科目:高中化學 來源:2015-2016學年遼寧葫蘆島一中等五校高二6月聯考化學卷(解析版) 題型:實驗題
某興趣小組探究SO2氣體還原Fe3+、I2,他們使用的藥品和裝置如下圖所示:
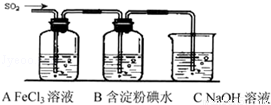
(1)SO2與Fe3+反應的還原、氧化產物分別是 、 (填離子符號)。
(2)下列實驗方案可以用于在實驗室制取所需SO2的是 。
A.Na2SO3溶液與HNO3
B.Na2SO3固體與濃硫酸
C.固體硫在純氧中燃燒
D.銅與熱濃H2SO4
(3)裝置C的作用是 。
(4)如果有280mL SO2氣體(已折算為標態)進入C裝置中,則C中,50mL NaOH溶液的濃度至少為 mol/L才能達到目的。
(5)在上述裝置中通入過量的SO2為了驗證A中SO2與Fe3+發生了氧化還原反應,他們取A中的溶液,分成三份,并設計了如下實驗:
方案①:往第一份試液中加入KMnO4溶液,紫紅色褪去。
方案②:往第一份試液加入KSCN溶液,不變紅,再加入新制的氯水,溶液變紅。
 方案③:往第二份試液加入用稀鹽酸酸化的BaCl2,產生白色沉淀。
方案③:往第二份試液加入用稀鹽酸酸化的BaCl2,產生白色沉淀。
上述方案不合理的是 ,原因是 。
(6)能表明I﹣的還原性弱于SO2的現象是 ,寫出有關離子方程式: 。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年遼寧葫蘆島一中等五校高二6月聯考化學卷(解析版) 題型:選擇題
設NA為阿伏加德羅常數的數值。下列說法正確的是
A.1mol•L ﹣1的NaClO溶液中含有ClO﹣的數目為NA
B.常溫常壓下,分子總數為NA的NO2和CO2混合氣體中含有的氧原子數為2NA
C.標準狀況下,11.2 L CH3CH2OH 中含有的氫原子數目為3NA
D.室溫下,1L pH=13的Ba(OH)2溶液中,OH﹣離子數目為0.2NA
pH=13的Ba(OH)2溶液中,OH﹣離子數目為0.2NA
查看答案和解析>>
科目:高中化學 來源:2015-2016學年湖北沙市高一下第六次半月考化學卷(解析版) 題型:填空題
隨原子序數的遞增,八種短周期元素(用字母x等表示)原子半徑的相對大小、最高正價或最低負價的變化如圖所示。根據判斷出的元素回答問題:


(1)f在元素周期表的位置是____________________________。
(2)比較d、e常見離子的半徑大小______>______(用化學式表示,下同);比較g、h的最高價氧化物對應的水化物的酸性強弱___________>____________。
(3)任選上述元素組成一種四原子共價化合物,寫出其電子式______________________。
(4)上述元素可組成鹽R:zx4f(gd4)2,向盛有10 mL 1 mol·L-1 R溶液的燒杯中滴加1 mol·L-1 NaOH溶液,沉淀物質的量隨NaOH溶液體積變化如圖所示。
① 寫出m段反應的離子方程式_______________________________。
② 若在R溶液中改加20 mL 1.2 mol·L-1 Ba(OH)2溶液,充分反應后,溶液中產生沉淀的物質的量為___________mol。
查看答案和解析>>
科目:高中化學 來源:2016屆河南省高三三模理綜化學試卷(解析版) 題型:選擇題
室溫下,將0.05 mol Na2CO3固體溶于水配成100mL溶液,向溶液中加入下列物質。有關結論正確的是
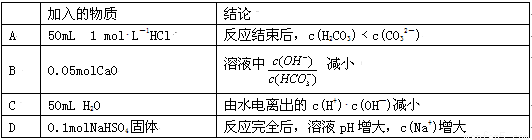
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com