


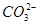 +7H2O 不變 ②1.9
+7H2O 不變 ②1.9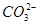 ,由此可寫出此電極的電極反應式。在電解過程中,由于
,由此可寫出此電極的電極反應式。在電解過程中,由于 沒有參與放電,且陽離子交換膜不允許陰離子自由通過,因此根據質量守恒可得陰極區Na2SO4的物質的量不變。
沒有參與放電,且陽離子交換膜不允許陰離子自由通過,因此根據質量守恒可得陰極區Na2SO4的物質的量不變。

 名師金手指領銜課時系列答案
名師金手指領銜課時系列答案科目:高中化學 來源:不詳 題型:填空題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.2H++2e-=H2↑ | B.Fe2++2e-=Fe |
| C.2H2O+O2+4e-=4OH- | D.Fe3++e-=Fe2+ |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.放電時,OH-向負極方向移動 |
| B.放電時,正極反應式為Zn+2OH--2e-=ZnO+H2O |
| C.充電時,Zn發生氧化反應 |
| D.充電時,陰極反應為O2+2H2O+4e-=4OH- |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.純銀器表面在空氣中因化學腐蝕漸漸變暗 |
| B.當鍍錫鐵制品的鍍層破損時,鍍層仍能對鐵制品起保護作用 |
| C.在海輪外殼連接銀塊保護外殼不受腐蝕是采用了犧牲陽極的陰極保護法 |
| D.可將地下輸油鋼管與外加直流電源的正極相連以保護它不受腐蝕 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 2Ni(OH)2
2Ni(OH)2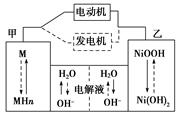
 Cu2O+H2↑
Cu2O+H2↑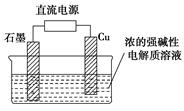
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.銅片作原電池的負極,碳棒作原電池的正極,氯化鈉作電解質溶液 |
| B.銅鋅合金在潮濕的空氣中發生電化學腐蝕 |
| C.用銅片作陰、陽電極,電解硫酸鈉水溶液 |
| D.用銅片作陰、陽電極,電解硫酸銅水溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com