
已知:TiO2(s)+2Cl2(g)===TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
2C(s)+O2(g)===2CO(g) ΔH=-221 kJ·mol-1
則反應TiO2(s)+2Cl2(g)+2C(s)=TiCl4(l)+2CO(g) ΔH為
A.—162 kJ·mol-1 B.+81 kJ·mol-1
C.+162 kJ·mol-1 D.-81 kJ·mol-1
 開心練習課課練與單元檢測系列答案
開心練習課課練與單元檢測系列答案科目:高中化學 來源:2011-2012學年寧夏銀川一中高二上學期期末考試化學試卷 題型:單選題
已知:TiO2(s)+2Cl2(g)===TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
2C(s)+O2(g)===2CO(g) ΔH=-221 kJ·mol-1
則反應TiO2(s)+2Cl2(g)+2C(s)=TiCl4(l)+2CO(g) ΔH為
| A.—162 kJ·mol-1 | B.+81 kJ·mol-1 |
| C.+162 kJ·mol-1 | D.-81 kJ·mol-1 |
查看答案和解析>>
科目:高中化學 來源:2012-2013學年四川成都棠湖中學外語實驗學校高二5月月考化學卷(帶解析) 題型:填空題
碳化硅(SiC) 、氧化鋁(Al2O3) 和氮化硅(Si3N4)是優良的高溫結構陶瓷,在工業生產和科技領域有重要用途。宇宙火箭和導彈中,大量用鈦代替鋼鐵。
(1)Al的離子結構示意圖為 ;
Al與NaOH溶液反應的離子方程式為
(2)氮化硅抗腐蝕能力很強,但易被氫氟酸腐蝕,氮化硅與氫氟酸反應生成四氟化硅和一種銨鹽,
其反應方程式為
(3)工業上用化學氣相沉積法制備氮化硅,其反應如下:
3SiCl4(g) + x N2(g) + 6 H2(g)  Si3N4(s) + 12 HCl(g) △H<0
Si3N4(s) + 12 HCl(g) △H<0
在恒溫、恒容時,分別將0.3mol SiCl4(g)、0.2mol N2(g)、0.6mol H2(g)充入2 L密閉容器內,進行上述反應,5 min達到平衡狀態,所得HCl(g)為0.3mol/L、 N2為0.05 mol/L
① H2的平均反應速率是
② 反應前與達到平衡時容器內的壓強之比=
③ 系數 x =
(4)已知:TiO2(s)+2Cl2(g)===TiCl4(l)+O2(g) ΔH1=+140 kJ·mol-1
C(s)+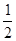 O2(g)=== CO(g) ΔH2 =-110 kJ·mol-1
O2(g)=== CO(g) ΔH2 =-110 kJ·mol-1
寫出TiO2和焦炭、氯氣反應生成TiCl4和CO氣體的熱化學方程式:
。
查看答案和解析>>
科目:高中化學 來源:2014屆四川成都棠湖中學外語實驗學校高二5月月考化學卷(解析版) 題型:填空題
碳化硅(SiC) 、氧化鋁(Al2O3) 和氮化硅(Si3N4)是優良的高溫結構陶瓷,在工業生產和科技領域有重要用途。宇宙火箭和導彈中,大量用鈦代替鋼鐵。
(1)Al的離子結構示意圖為 ;
Al與NaOH溶液反應的離子方程式為
(2)氮化硅抗腐蝕能力很強,但易被氫氟酸腐蝕,氮化硅與氫氟酸反應生成四氟化硅和一種銨鹽,
其反應方程式為
(3)工業上用化學氣相沉積法制備氮化硅,其反應如下:
3SiCl4(g) + x N2(g) + 6 H2(g)  Si3N4(s) + 12
HCl(g) △H<0
Si3N4(s) + 12
HCl(g) △H<0
在恒溫、恒容時,分別將0.3mol SiCl4(g)、0.2mol N2(g)、0.6mol H2(g)充入2 L密閉容器內,進行上述反應,5 min達到平衡狀態,所得HCl(g)為0.3mol/L、 N2為0.05 mol/L
① H2的平均反應速率是
② 反應前與達到平衡時容器內的壓強之比=
③ 系數 x =
(4)已知:TiO2(s)+2Cl2(g)===TiCl4(l)+O2(g) ΔH1=+140 kJ·mol-1
C(s)+ O2(g)===
CO(g) ΔH2 =-110
kJ·mol-1
O2(g)===
CO(g) ΔH2 =-110
kJ·mol-1
寫出TiO2和焦炭、氯氣反應生成TiCl4和CO氣體的熱化學方程式:
。
查看答案和解析>>
科目:高中化學 來源:2014屆浙江省高一下學期期中考試實驗班化學試卷(解析版) 題型:填空題
I.已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) △H=+140kJ·mol-1
2C(s)+O2(g)=2CO(g) △H=-221kJ·mol-1
寫出TiO2和焦炭、氯氣反應生成液態TiCl4和CO氣體的熱化學方程式: 。
II.將一定量純凈的氨基甲酸銨固體置于特制的密閉真空容器中(假設容器體積不變,固體試樣體積忽略不計),在恒定溫度下使其達到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)
則可以判斷該分解反應已經達到平衡狀態的是 。
A.2v正(NH3)=v逆(CO2) B.密閉容器中總壓強不變
C.密閉容器中混合氣體的密度不變 D.密閉容器中氨氣的體積分數不變
III.以丙烷為燃料制作新型燃料電池,電解質是熔融碳酸鹽。電池的一極通入O2和CO2,電極反應式為:O2+2CO2+4e-=2CO32-;另一極通入丙烷,電極反應式為 ;放電時,CO32-移向電池的 (填“正”或“負”)極。
IV.如圖裝置所示,C、D、E、F都是惰性電極,甲、乙中溶液的體積和物質的量濃度都相同(假設通電前后溶液體積不變),A、B為外接直流電源的兩極。將直流電源接通后,F極附近呈紅色。

⑴若甲、乙裝置中的C、D、E、F電極均只有一種單質生成時,對應單質的物質的量之比為 。
⑵現用丙裝置作“銅的電解精煉”,則H應該是 。(填“純銅”或“粗銅”)。
⑶上圖甲裝置電解CuSO4溶液一段時間后,向所得溶液中加入0.2mol Cu(OH)2后,恰好使溶液恢復到電解前的濃度。則乙裝置中,若不考慮Cl2的溶解及與堿的反應,此裝置共產生氣體 L(標準狀況)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com